Даурицина - Википедия - Dauricine
 | |
| Имена | |
|---|---|
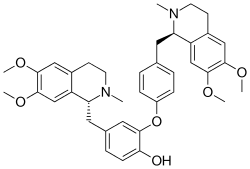
| Название ИЮПАК 4-{[(1р) -6,7-диметокси-2-метил-1,2,3,4-тетрагидроизохинолин-1-ил] метил} -2- (4 - {[(1р) -6,7-диметокси-2-метил-1,2,3,4-тетрагидроизохинолин-1-ил] метил} фенокси) фенол | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.208.622 |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C38ЧАС44N2О6 | |
| Молярная масса | 624.778 г · моль−1 |
| Плотность | 1,186 г / мл |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Даурицин это растение метаболит, химически классифицируется как фенол, ароматический эфир, и изохинолин алкалоид.[1] Выделен из азиатской лозы. Мениспермум даурикум, широко известный как азиатский лунный семя, и североамериканский виноград Мениспермум Canadense, широко известный как канадское семя луны.[2] Ученым Тецудзи Каметани и Кейитиро Фукумото из Японии приписывают то, что они первыми синтезировали даурицин в 1964 году, используя как Реакция Арндта-Эйстерта и Реакция Бишлера-Наперальского сделать так.[3] Даурицин изучен in vitro за его способность подавлять рост раковых клеток[4][5][6][7] и блокировать сердечную трансмембранную Na+, К+, а Са2+ ионные токи.[8]
Рекомендации
- ^ «ЧЕБИ: 4331 - даурицин». ЧЭБИ. Получено 30 мая 2015.
- ^ Каметани, Тетсудзи; Фукумото, Кейитиро (1964). «Полный синтез (±) -даурицина». Буквы Тетраэдра. 5 (38): 2771–2775. Дои:10.1016 / S0040-4039 (00) 71728-X.
- ^ Манске, Р.Х.Ф. (1967). Алкалоиды: химия и физиология V9. Нью-Йорк: Academic Press. п. 141. ISBN 9780080865331. Получено 30 мая 2015.
- ^ Ян, Чжэнфэн; Ли, Чэнхай; Ван, Сю; Чжай, Чуньянь; Йи, Чжэнфан; Ван, Лэй; Лю, Бишэн; Ду, Бинг; Ву, Хуэйхуэй; Го, Сичжи; Лю, Минъяо; Ли, Дали; Ло, Цзянь (2010). «Даурицин индуцирует апоптоз, подавляет пролиферацию и инвазию посредством ингибирования сигнального пути NF-kappaB в раковых клетках толстой кишки». J. Cell. Физиол. 225 (1): 266–75. Дои:10.1002 / jcp.22261. PMID 20509140. S2CID 5501319.
- ^ Джин, Хуа; Дай, Джиею; Чен, Сяоянь; Лю, Цзя; Чжун, Дафан; Гу, Янсонг; Чжэн, Цзян (2009). «Легочная токсичность и метаболическая активация даурицина у мышей CD-1». Журнал фармакологии и экспериментальной терапии. 332 (3): 738–46. Дои:10.1124 / jpet.109.162297. PMID 20008063. S2CID 21824941.
- ^ Тан, Сюй-дон; Чжоу, Синь; Чжоу, Кэ-юань (2009). «Даурицин подавляет накопление белка альфа-фактора, индуцируемого инсулиноподобным фактором роста I, индуцируемого гипоксией, и экспрессию фактора роста эндотелия сосудов в клетках рака груди человека». Акта Фармакол Син. 30 (5): 605–16. Дои:10.1038 / aps.2009.8. ЧВК 4002832. PMID 19349962.
- ^ Ван, Цзюнь; Ли, Юань; Зу, Сюн-Бин; Чен, Мин-Фэн; Ци, Ли (2012). «Даурицин может подавлять активность пролиферации опухолевых клеток мочевыводящих путей». Азиатский Pac J Trop Med. 5 (12): 973–76. Дои:10.1016 / S1995-7645 (12) 60185-0. PMID 23199717.
- ^ Цянь, JQ (2002). «Сердечно-сосудистые фармакологические эффекты производных бисбензилизохинолина алкалоидов». Акта Фармакол Син. 23 (12): 1086–92. PMID 12466045.
