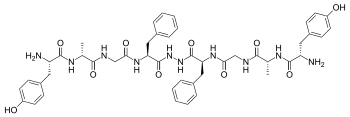
Бифалин - Biphalin
 | |
 | |
| Клинические данные | |
|---|---|
| Код УВД |
|
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| ChemSpider | |
| Панель управления CompTox (EPA) | |
| Химические и физические данные | |
| Формула | C46ЧАС56N10О10 |
| Молярная масса | 909.014 г · моль−1 |
| 3D модель (JSmol ) | |
| |
| |
Бифалин это димерный энкефалин эндогенный пептид (Tyr-D-Ala-Gly-Phe-NH)2 состоит из двух тетрапептидов, полученных из энкефалины, соединенные "хвост к хвосту" гидразид мост.[1] Присутствие двух различных фармакофоров придает бифалину высокое сродство к обоим. μ и δ опиоидные рецепторы (с ЭК50 примерно 1-5 нМ как для μ-, так и для δ-рецепторов), поэтому он имеет обезболивающее Мероприятия.[2]Бифалин представляет собой значительную антиноцицептивный профиль. Фактически, при введении интрацеребровентрикулярно у мышей эффективность бифалина почти в 7 раз выше, чем у сверхмощного алкалоид агонист, эторфин и в 7000 раз больше, чем морфий; бифалин и морфин оказались равносильными после внутрибрюшинный администрация. Необычайная активность этого соединения in vivo сочетается с небольшими побочными эффектами, в частности, не дает зависимость при хроническом употреблении.[3] По этим причинам было предпринято несколько попыток получить больше информации о взаимосвязи структура-активность (SAR ). Результаты ясно показывают, что, по крайней мере, для μ-рецептора привязка, наличие двух фармакофоров не обязательно;[2] Тюр1 незаменим для обезболивающего действия, при замене Phe в положении 4 и 4 'с неароматическими, но липофильный аминокислоты не сильно меняют связывающие свойства[2] и, как правило, обнаружено, что положения 4,4 'важны для создания аналогов бифалина с повышенной эффективностью и модифицированной селективностью μ / δ.[4][5] Гидразидный линкер не является основным для активности или связывания, и он может быть удобно заменен различными конформационно ограниченными циклоалифатическими диаминовыми линкерами.[6]
Рекомендации
- ^ Флиппен-Андерсон, Джудит (март 2002 г.). «Кристаллическая структура сульфата бифалина: мультирецепторный опиоидный пептид». Журнал исследований пептидов. 59 (3): 123–33. Дои:10.1034 / j.1399-3011.2002.01967.x. PMID 11985706.
- ^ а б c Липковски, Анджей (сентябрь 1999 г.). «Биологическая активность фрагментов и аналогов сильнодействующего димерного опиоидного пептида бифалина». Письма по биоорганической и медицинской химии. 9 (18): 2763–66. Дои:10.1016 / S0960-894X (99) 00464-3. PMID 10509931.
- ^ Хоран, Питер (июнь 1993). «Антиноцицептивный профиль бифалина, аналог димерного энкефалина». Журнал фармакологии и экспериментальной терапии. 265 (3): 1446–54. PMID 8389867.
- ^ Ли, Гуйген (март 1998 г.). «Модификации 4,4'-остатков и исследования SAR бифалина, очень мощного пептида, активного в отношении опиоидных рецепторов». Письма по биоорганической и медицинской химии. 8 (5): 555–60. Дои:10.1016 / S0960-894X (98) 00065-1. PMID 9871617.
- ^ Моллика, Адриано (май 2011 г.). «Новые мощные аналоги бифалина, содержащие п-фтор-L-фенилаланин в положениях 4,4 'и негидразиновые линкеры». Аминокислоты. 40 (5): 1503–11. Дои:10.1007 / s00726-010-0760-7. ЧВК 5689474. PMID 20924622.
- ^ Моллика, Адриано (май 2005 г.). «Синтез и биологическая оценка новых аналогов бифалина с негидразиновыми линкерами». Письма по биоорганической и медицинской химии. 15 (10): 2471–5. Дои:10.1016 / j.bmcl.2005.03.067. PMID 15863299.
