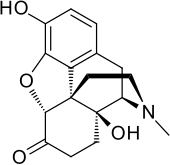
Оксиморфон - Oxymorphone
 | |
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Numorphan, Numorphone, Opana, другие |
| Другие имена | 14-гидроксидигидроморфинон |
| AHFS /Drugs.com | Монография |
| MedlinePlus | a610022 |
| Беременность категория |
|
| Маршруты администрация | Внутрь, буккально, сублингвально, интраназально, внутривенно, эпидурально, подкожно, внутримышечно |
| Код УВД | |
| Легальное положение | |
| Легальное положение | |
| Фармакокинетический данные | |
| Биодоступность | внутрь: 10% Буккальный: 28% Сублингвально: 37,5% Интраназально: 43%[2] IV, IM и ИТ: 100%[3] |
| Связывание с белками | 10%[3] |
| Метаболизм | Печень (CYP3A4, глюкуронизация )[3] |
| Устранение период полураспада | 7–9 часов[3] Продолжительность действия: 6-8 часов перорально, 4-6 часов парентерально. |
| Экскреция | Моча, кал[3] |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭМБЛ | |
| Панель управления CompTox (EPA) | |
| ECHA InfoCard | 100.000.873 |
| Химические и физические данные | |
| Формула | C17ЧАС19NО4 |
| Молярная масса | 301.342 г · моль−1 |
| 3D модель (JSmol ) | |
| |
| |
| (проверять) | |
Оксиморфон, продается под торговыми марками Numorphan и Опана среди прочего, это опиоид болеутоляющее средство. Обезболивание после инъекции начинается примерно через 5–10 минут, после перорального приема - примерно через 30 минут и длится примерно 3-4 часа для таблеток с немедленным высвобождением и 12 часов для таблеток с пролонгированным высвобождением.[4] Период полувыведения оксиморфона при внутривенном введении намного быстрее, и поэтому препарат чаще всего используется перорально.[5] Нравиться оксикодон, который метаболизируется в оксиморфон, оксиморфон имеет высокий потенциал злоупотребления.[6]
Он был разработан в Германия в 1914 г. Он был запатентован в 1955 г. и разрешен к применению в медицине в 1959 г.[7] В июне 2017 г. FDA спросил Endo Pharmaceuticals удалить свой продукт с рынка США.[8] Отчасти это было из-за опиоидная эпидемия в США, а также тот факт, что изменение рецептуры 2012 года не смогло остановить незаконное введение препарата. В ответ Endo через месяц добровольно удалила Opana ER с рынка.[9] Общие версии оксиморфона с расширенным выпуском, например, произведенные Амнеал Фармацевтические препараты, по-прежнему доступны в США.[10]
Медицинское использование
Оксиморфон немедленного высвобождения показан для облегчения умеренной и сильной боли, например, для лечения острой послеоперационной боли.[11] Для любого хронического лечения боли клиницисты должны рассматривать длительное использование только в том случае, если есть значительная клиническая польза от терапии пациента, которая перевешивает любой потенциальный риск. В качестве лечения первой линии при хронической боли используются немедикаментозные и неопиоидные препараты.[12]
Таблетки оксиморфона с расширенным высвобождением показаны для лечения хронической боли и только для людей, которые уже регулярно принимают сильнодействующие опиоиды в течение длительного периода. Таблетки с оксиморфоном с немедленным высвобождением рекомендуются от прорывной боли для людей с расширенной версией. По сравнению с другими опиоидами оксиморфон обладает аналогичной обезболивающей эффективностью.[13]
В Соединенных Штатах это контролируемое вещество из Списка II с ACSCN из 9652.[14]
Доступность
Бренды и формы
Оксиморфон продается под одной торговой маркой производителя, Endo Pharmaceuticals, под торговыми марками Opana и Opana ER. Opana ER была снята производителем с продажи в 2017 году, поэтому она больше не доступна.[15] Однако варианты IR (немедленная версия) и ER (расширенная версия) доступны под общим названием Oxymorphone и Oxymorphone ER, предоставляемые множеством различных брендов.
Оксиморфон также доступен в виде инъекций для стационарного применения, доступен для внутривенного введения (внутривенный ), Я (внутримышечный ), и подкожный инъекция.
IR и ER представляют лекарственные формы с модифицированным высвобождением, которые изменяют скорость всасывания лекарства после приема внутрь.
Лекарственные формы для перорального применения
Оксиморфон выпускается в разных дозах.
| ИК-планшет[16] | ER 12-часовой планшет [17] |
|---|---|
| 5 мг | 5 мг |
| 10 мг | 7,5 мг |
| 10 мг | |
| 15 мг | |
| 20 мг | |
| 30 мг | |
| 40 мг |
Особые группы населения
Пациенты, уже страдающие от истощения, имеют гораздо более высокий риск угнетения дыхания. В этой группе пациентов следует рассмотреть неопиоидные анальгетики.
Пожилые пациенты гораздо более чувствительны к побочным эффектам, таким как падения, когнитивные нарушения и запоры, и их следует контролировать. Снижение функции почек, связанное со старением, приводит к уменьшению клиренса препарата, что приводит к узким терапевтическим окнам и увеличению опасности передозировки. Если оксиморфон абсолютно показан, этой группе населения следует назначать меньшие начальные дозы.
Если беременные женщины принимают оксиморфон в течение длительного периода, существует риск неонатального синдрома отмены у новорожденных. Оксиморфон проникает через плаценту и несет риск врожденных дефектов, замедленного роста плода, мертворождения и преждевременных родов. Дети матерей, которые физически зависимы от оксиморфона, имеют более высокий риск подобной зависимости. Из-за этих серьезных рисков применение оксиморфона среди этой группы населения крайне не рекомендуется. Количество переноса оксиморфона в грудное молоко неизвестно, и женщинам рекомендуется взвешивать риски и преимущества перед кормлением грудью при приеме этого лекарства.[18]
Побочные эффекты
Основные побочные эффекты оксиморфона аналогичны другим опиоидам; наиболее частыми побочными эффектами являются запор, тошнота, рвота, головокружение, сухость во рту и сонливость. Этот препарат вызывает сильную зависимость, как и другие опиоиды, и может привести к химической зависимости и абстиненции.[19]
Передозировка
Как и другие опиоиды, передозировка оксиморфона характеризуется угнетением дыхания, сонливостью, переходящей в ступор или кому, скелетными мышцами. слабое место, холодная и липкая кожа, а иногда медленный пульс и низкое кровяное давление. В тяжелом случае передозировки апноэ, кровообращение, остановка сердца и смерть может наступить.[19]
Фармакология
Фармакодинамика
Оксиморфон проявляет свои эффекты, связываясь и активируя μ-опиоидный рецептор (MOR) и, в гораздо меньшей степени, δ-опиоидный рецептор (DOR) и κ-опиоидный рецептор (KOR).[3] Его деятельность в DOR может усилить его деятельность в MOR.[3] Оксиморфон в 10 раз сильнее морфина.[20]
| Родство (Kя ) | Соотношение | ||
|---|---|---|---|
| MOR | DOR | KOR | MOR: DOR: KOR |
| 0,78 нМ | 50 нМ | 137 нМ | 1:64:176 |
| Сложный | Маршрут | Доза |
|---|---|---|
| Кодеин | PO | 200 мг |
| Гидрокодон | PO | 20–30 мг |
| Гидроморфон | PO | 7,5 мг |
| Гидроморфон | IV | 1,5 мг |
| Морфий | PO | 30 мг |
| Оксикодон | IV | 20 мг |
| Морфий | IV | 10 мг |
| Оксикодон | PO | 20 мг |
| Оксиморфон | PO | 7-10 мг |
| Оксиморфон | IV | 1 мг |
Фармакокинетика
Химия
Оксиморфон коммерчески производится из тебаин, который является второстепенным компонентом опийный мак (Папавер сомниферум), но тебаин содержится в большем количестве (3%) в корнях восточный мак (Papaver orientale).[3][25]Немецкие патенты середины 1930-х годов указывают, что оксиморфон, а также гидроморфон, гидрокодон, оксикодон, и ацетилморфон может быть приготовлен - без потребности в газообразном водороде - из растворов кодеин, морфий, и дионин кипячением кислого водного раствора или лекарственного препарата-предшественника, растворенного в этиловый спирт, в присутствии некоторых металлов, а именно палладий и платина в виде мелкодисперсного порошка или коллоидной формы или платиновой черноты.
Гидрохлорид оксиморфона представляет собой белые кристаллы без запаха или порошок от белого до почти белого цвета. Он темнеет по цвету при длительном воздействии света. Один грамм гидрохлорида оксиморфона растворим в 4 мл воды и плохо растворим в спирте и эфире. Он разлагается при контакте со светом.[19]
Оксиморфон можно ацетилировать, как морфин, гидроморфон и некоторые другие опиоиды. Моно-, ди-, три- и тетраэфиры оксиморфона были разработаны в 1930-х годах, но в настоящее время не используются в медицине. Предположительно, могут быть получены другие сложные эфиры, такие как никотинил, бензоил, формил, циннимоил и т. Д.[нужна цитата ]
США 2013 г. ДЭА годовые производственные квоты составляли 18 375 килограммов на переработку (из оксиморфона можно производить ряд препаратов, как обезболивающих, так и антагонисты опиоидов подобно налоксон ) и 6875 кг для непосредственного производства готовой продукции.[26] Оксиморфон также является второстепенным метаболитом оксикодон, который образован CYP2D6 -опосредованное O-деметилирование.[3]
История
Оксиморфон был впервые разработан в Германия в 1914 г.,[27] и запатентовано в США Endo Pharmaceuticals в 1955 г.[28] Он был введен в США в январе 1959 года и примерно в то же время в других странах.[3]
Общество и культура
Фирменные наименования
- Нуморфан (суппозиторий и раствор для инъекций)
- Opana ER (таблетка с расширенным выпуском): июнь 2017 г. запрос FDA на удаление из-за злоупотребления внутривенным введением.[29]
- Opana IR (таблетка немедленного высвобождения)
- O-Morphon в Бангладеш от Ziska Pharmaceutical ltd.
Торговое название Numorphan происходит по аналогии с названием Nucodan для оксикодон продукта (или наоборот), а также Параморфан / Параморфан для дигидроморфин и паракодин (дигидрокодеин ). Единственная коммерчески доступная соль оксиморфона в большей части мира в настоящее время - это гидрохлорид, который имеет коэффициент конверсии свободного основания 0,891, а моногидрат гидрохлорида оксиморфона имеет коэффициент 0,85.[19]
Общая маркировка таблеток - ATV10 / APO; HK10 (10 мг) продолговатый белый и ATV20 / APO; HK20 (20 мг) продолговатый белый.[нужна цитата ]
Злоупотреблять
В 1924 году Конгресс США запретил продажу, импорт или производство героин, еще одно опиоидное обезболивающее в Закон о борьбе с героином 1924 года.
За последние 30 лет[когда? ], злоупотребление опиоидами было превалирующей проблемой общественного здравоохранения. В последние годы[когда? ]эта проблема переросла в полноценную эпидемию и ведет к ряду других проблем общественного здравоохранения, включая распространение таких заболеваний, как гепатит С и вирус иммунодефицита человека (ВИЧ).[30][31]
В Соединенных Штатах по состоянию на 2013 год более 12 миллионов человек злоупотребляли опиоидными препаратами не реже одного раза в год.[32] В 2010 году 16 652 случая смерти были связаны с передозировкой опиатов, в 2015 году это число увеличилось до 33 091 человека.[33][34] В сентябре 2013 года новые руководящие принципы маркировки FDA для опиоидов длительного действия и пролонгированного высвобождения потребовали, чтобы производители устраняли умеренную боль в качестве показания к применению, оставляя препарат для «боли, достаточно сильной, чтобы требовать ежедневного круглосуточного длительного лечения опиоидами». "[35] однако это не ограничивало врачей назначать опиоиды для умеренного использования "по мере необходимости".[32]
В январе 2013 года Центры по контролю и профилактике заболеваний (CDC) сообщили о заболевании, связанном с внутривенным (IV) злоупотреблением пероральным Opana ER (оксиморфоном) в Теннесси. Синдром напоминал синдром тромботическая тромбоцитопеническая пурпура (ТТП).[36] Начальная терапия включала терапевтические плазмаферез, что касается ТТП. В отличие от ТТП, нет дефицита ADAMTS13 активности и антител против ADAMTS13 не обнаружено, что указывает на тромботическая микроангиопатия различной первопричины. Если будет признано, что злоупотребление внутривенной опаной будет признано, можно рассмотреть поддерживающую терапию вместо терапевтического плазмафереза.[37]
В январе 2015 года первая вспышка ВИЧ, связанная со злоупотреблением рецептурными опиоидными препаратами, была выявлена Департаментом здравоохранения штата Индиана (ISDH) в небольшой сельской местности округа Скотт на юго-востоке Индианы.[38] ISDH начала расследование этой вспышки ВИЧ, когда было подтверждено, что 11 человек оказались положительными на ВИЧ и связаны с одним и тем же сообществом. За три месяца этого расследования ISDH диагностировала в общей сложности 135 человек с ВИЧ, и это число продолжает расти. Причина этой вспышки связана с совместным использованием игл между лицами, злоупотребляющими опиоидами, что в некоторых случаях связано с совместным использованием игл до девяти разных партнеров.[31]
В конце марта 2015 г. в отчетах указывалось, что Остин, Индиана, был центром вспышки ВИЧ, вызванной употреблением оксиморфона в качестве инъекционного рекреационного наркотика. Вспышка болезни потребовала принятия срочных мер со стороны государственных чиновников.[39][40][41] «Встроенный» выпуск подкаста NPR от 31 марта 2016 года был подробным отчетом о посещении лиц, злоупотребляющих оксиморфоном в Остине, штат Индиана. В 2016 году розничная цена оксиморфона составила 140 долларов.[42]
Наиболее распространенным опиоидом, вызывающим злоупотребление в этой вспышке, был Opana ER, обезболивающий оксиморфон с длительным высвобождением, устойчивый к раздавливанию и производимый Endo Pharmaceuticals. Этот сложный для измельчения состав был запущен в производство в 2012 году, чтобы снизить риск злоупотребления при вдыхании измельченной таблетки. Однако лица, злоупотребляющие опиоидами, обошли эту проблему, найдя способ растворить и ввести наркотик.[38]
Масштабы этой вспышки привлекли внимание как CDC, так и FDA. CDC начал более масштабное расследование всех вспышек заболеваний, связанных с Opana ER, сосредоточив внимание на заболеваемости тромботической тромбоцитопенической пурпурой (ТТП) во время вспышки в Теннесси в 2012 году, а также вспышки ВИЧ в 2015 году в Индиане. FDA запустило постмаркетинговое исследование безопасности в отношении изменения рецептуры Opana ER в 2012 году.[43] а правительство штата Индиана помогло профинансировать еще одно исследование, изучающее связь между ВИЧ-инфекцией и инъекционным употреблением оксиморфона в Индиане с 2014 по 2015 год.[44]
Результаты этих исследований показали, что преобразование Opana в трудноразрушаемую таблетку непреднамеренно увеличивает риск передачи приобретенных инфекций, передающихся через кровь, потому что лица, злоупотребляющие опиоидами, переключились с использования препарата через нос на инъекции. Эта эпидемия привела к увеличению риска заражения инфекцией, передаваемой через кровь при употреблении инъекционных опиоидов, по сравнению с риском заражения инфекцией при употреблении инъекционного героина или кокаина.[30][43][44]
В июне 2017 года, столкнувшись с кризисом общественного здравоохранения, эпидемией опиоидов, FDA попросило Endo Pharmaceuticals «убрать с рынка свое опиоидное обезболивающее, переработанный Opana ER (гидрохлорид оксиморфона)». В своем пресс-релизе от 8 июня 2017 года они также отметили, что это был первый раз, когда FDA предприняло шаги по «изъятию из продажи опиоидных обезболивающих, продаваемых в настоящее время из-за последствий злоупотребления для общественного здравоохранения».[29] К 6 июля 2017 года Endo International добровольно выполнила требование FDA об удалении.[45]
Смотрите также
Рекомендации
- ^ "Drugs @ FDA: одобренные FDA лекарственные препараты". www.accessdata.fda.gov. Получено 7 ноября 2017.
- ^ Хуссейн М.А., Аунгст Б.Дж. (август 1997 г.). «Интраназальное всасывание оксиморфона». Журнал фармацевтических наук. 86 (8): 975–6. Дои:10.1021 / js960513x. PMID 9269879.
- ^ а б c d е ж грамм час я j Дэвис, член парламента; Блики, PA; Харди, Дж. (2009) [2005]. Опиоиды при раковой боли (2-е изд.). Оксфорд, Великобритания: Издательство Оксфордского университета. С. Глава 17. ISBN 978-0-19-157532-7.
- ^ Слоан, Пол (2008-08-01). «Обзор перорального оксиморфона в лечении боли». Терапия и управление клиническими рисками. 4 (4): 777–787. Дои:10.2147 / tcrm.s1784. ISSN 1176-6336. ЧВК 2621383. PMID 19209260.
- ^ Смит, Ховард С. (2009-04-01). «Клиническая фармакология оксиморфона». Медицина боли. 10 (Suppl_1): S3 – S10. Дои:10.1111 / j.1526-4637.2009.00594.x. ISSN 1526-2375.
- ^ Бабалонис, Шанна; Lofwall, Michelle R .; Нуццо, Пол А .; Уолш, Шэрон Л. (01.01.2016). «Фармакодинамические эффекты перорального оксиморфона: предрасположенность к злоупотреблениям, анальгетический профиль и прямые физиологические эффекты у людей». Биология зависимости. 21 (1): 146–158. Дои:10.1111 / adb.12173. ISSN 1355-6215. ЧВК 4383736. PMID 25130052.
- ^ Фишер, Джнос; Ганеллин, С. Робин (2006). Открытие лекарств на основе аналогов. Джон Вили и сыновья. п. 52X. ISBN 9783527607495.
- ^ Вольф, Лорен К. (19.06.2017). «FDA нацелено на опиоидную эпидемию». Новости химии и машиностроения. 95 (25): 8.
- ^ Комиссар, Офис (2019-09-10). «Сообщения для прессы - FDA требует удаления Opana ER из-за рисков, связанных со злоупотреблением». www.fda.gov.
- ^ Бернштейн, Ленни; Мерл, Рене (27.11.2019). «Шесть фармацевтических компаний вызваны в суд в рамках федерального расследования по опиоидам». Вашингтон Пост. Получено 2020-04-18.
- ^ Слоан, Пол (2008). «Обзор перорального оксиморфона в лечении боли». Терапия и управление клиническими рисками. 4 (4): 777–787. Дои:10.2147 / TCRM.S1784. ЧВК 2621383. PMID 19209260.
- ^ «Руководство по назначению опиоидов при хронической боли» (PDF). CDC. CDC. Получено 2 ноября 2018.
- ^ «Обезболивание при раке с помощью опиоидов: оптимизация обезболивания». Своевременно. Своевременно.
- ^ «Кодовый номер контролируемого вещества». Управление по борьбе с наркотиками США. ДЭА. Получено 2 ноября 2018.
- ^ Endo выведет Opana с рынка по запросу FDA. Аптека Таймс. Барретт, Дженнифер. В сети. Доступны на: https://www.pharmacytimes.com/product-news/endo-to-pull-opana-from-the-market-following-fda-request. По состоянию на 1 ноября 2018 г.
- ^ Оксиморфон ИК-вкладыш. Endo Pharmaceuticals. Веб-сайт FDA. Доступны на: https://www.accessdata.fda.gov/drugsatfda_docs/label/2012/021611s007lbl.pdf. По состоянию на 19 ноября 2018 г.
- ^ Оксиморфон-вкладыш ER. Endo Pharmaceuticals. Веб-сайт FDA. Доступны на: https://www.accessdata.fda.gov/drugsatfda_docs/label/2013/201655s004lbl.pdf. По состоянию на 19 ноября 2018 г.
- ^ "Авторизоваться". www.crlonline.com. Получено 2018-11-01.
- ^ а б c d Брейфилд, А, изд. (30 января 2013 г.). «Оксиморфон гидрохлорид». Мартиндейл: полный справочник лекарств. Фармацевтическая пресса. Получено 5 мая 2014.
- ^ Проммер, Э (февраль 2006 г.). «Оксиморфон: обзор». Поддерживающая терапия при раке. 14 (2): 109–15. Дои:10.1007 / s00520-005-0917-1. PMID 16317569. S2CID 26359576.
- ^ Корбетт А.Д., Патерсон SJ, Костерлиц HW (1993). «Селективность лигандов для опиоидных рецепторов». Опиоиды. Справочник по экспериментальной фармакологии. 104 / 1. С. 645–679. Дои:10.1007/978-3-642-77460-7_26. ISBN 978-3-642-77462-1. ISSN 0171-2004.
- ^ Кинг (25 октября 2010 г.). Фармакология женского здоровья. Издательство "Джонс и Бартлетт". С. 332–. ISBN 978-1-4496-1073-9.
- ^ Дэвид Х. Честнат; Синтия А Вонг; Лоуренс Ч. Цен; Уорвик Д Нган Ки, Яаков Бейлин, Джилл Мхайр (28 февраля 2014 г.). Акушерская анестезия Chestnut: принципы и практика, электронная книга. Elsevier Health Sciences. стр. 611–. ISBN 978-0-323-11374-8.CS1 maint: несколько имен: список авторов (связь)
- ^ Адриана П. Тициани (1 июня 2013 г.). Руководство по лекарствам для медсестер Хаварда. Elsevier Health Sciences. стр. 933–. ISBN 978-0-7295-8162-2.
- ^ Корриган, Д; Мартын, EM (май 1981 г.). «Содержание тебаина в декоративных маках, принадлежащих к секции papaver oxytona». Planta Medica. 42 (1): 45–9. Дои:10.1055 / с-2007-971544. PMID 17401879.
- ^ «2013 - Предлагаемые корректировки совокупных квот производства для контролируемых веществ Списка I и II и оценка годовой потребности в химических веществах, включенных в Список I: эфедрин, псевдоэфедрин и фенилпропаноламин на 2013 год». www.deadiversion.usdoj.gov.
- ^ Синатра, Раймонд (2010). Сущность обезболивающих и анальгетиков. MA, США: Cambridge University Press; 1 издание. п. 123. ISBN 978-0521144506.
- ^ Патент США 2806033, Mozes Juda Leweustein, "Производное морфина", опубликовано 1955-03-08, выпущено 1957-10-09.
- ^ а б «FDA требует удаления Opana ER из-за рисков, связанных со злоупотреблением» (Пресс-релиз). Сильвер-Спринг, Мэриленд. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. 8 июня 2017 г.. Получено 26 октября, 2017.
Сегодня Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США потребовало, чтобы Endo Pharmaceuticals удалила с рынка свое опиоидное обезболивающее, переработанное Opana ER (гидрохлорид оксиморфона) ... от продажи из-за последствий злоупотребления для общественного здравоохранения ... [Комиссар FDA Скотт Готтлиб, доктор медицины]: «Мы столкнулись с эпидемией опиоидов - кризисом общественного здравоохранения, и мы должны предпринять все необходимые шаги для сокращения масштабов злоупотребления опиоидами и злоупотреблять.
- ^ а б Раймонд, Дэниел (2015-03-02). «Инъекционная опана: вспышка ВИЧ-инфекции в Индиане и эпидемия опиоидов в Америке». Середина. Получено 2018-11-02.
- ^ а б «Опасности опиоидного болеутоляющего средства Opana перевешивают преимущества, - утверждает комиссия FDA». NPR.org. Получено 2018-11-02.
- ^ а б Гириуан, Лиза; Хэли, Мелисса (11 сентября 2013 г.). «FDA требует более строгой маркировки обезболивающих». Лос-Анджелес Таймс. Стр. A1 и A9.
- ^ «Передозировка наркотиков в США: информационный бюллетень». Центры по контролю за заболеваниями. Получено 12 сентября 2013.
- ^ Радд Р.А., Сет П., Дэвид Ф., Шолль Л. (декабрь 2016 г.). «Рост смертности от передозировки наркотиков и опиоидов - США, 2010–2015 годы». MMWR. Еженедельный отчет о заболеваемости и смертности. 65 (50–51): 1445–1452. Дои:10.15585 / ммwr.mm655051e1. PMID 28033313.
- ^ «Изменения в маркировке класса опиоидов в ER / LA и постмаркетинговые требования» (PDF). FDA. Получено 12 сентября 2013.
- ^ Центры по профилактике заболеваний (CDC) (январь 2013 г.). «Тромботическая тромбоцитопеническая пурпура (ТТП) -подобное заболевание, связанное с внутривенным злоупотреблением Opana ER - Теннесси, 2012». MMWR. Еженедельный отчет о заболеваемости и смертности. 62 (1): 1–4. ЧВК 4604918. PMID 23302815.
- ^ Миллер П.Дж., Фарланд А.М., Кнович М.А., Батт К.М., Оуэн Дж. (Июль 2014 г.). «Успешное лечение внутривенного злоупотребления пероральной Opana ER-индуцированной тромботической микроангиопатии без плазмафереза». Американский журнал гематологии. 89 (7): 695–7. Дои:10.1002 / ajh.23720. PMID 24668845. S2CID 27414213.
- ^ а б «Вспышка ВИЧ-инфекции в сообществе, связанная с употреблением оксиморфона путем инъекций - Индиана, 2015 г.». www.cdc.gov. Получено 2018-11-02.
- ^ Пакетт, Даниэль (30 марта 2015 г.). «Как вспышка ВИЧ поразила сельские районы Индианы - и почему нам следует обращать на это внимание». Вашингтон Пост. Получено 1 апреля 2015.
- ^ Конрад К., Брэдли Х.М., Броз Д., Будда С., Чепмен Е.Л., Галанг Р.Р., Хиллман Д., Хон Дж., Гувер К.В., Патель М.Р., Перес А., Питерс П.Дж., Понтонес П., Роузберри Дж. С., Сандовал М., Шилдс Дж., Уолтхолл Дж. , Waterhouse D, Weidle PJ, Wu H, Duwve JM (май 2015 г.). «Вспышка ВИЧ-инфекции в сообществе, связанная с инъекционным употреблением оксиморфона, - Индиана, 2015». MMWR. Еженедельный отчет о заболеваемости и смертности. 64 (16): 443–4. ЧВК 4584812. PMID 25928470.
- ^ Strathdee SA, Beyrer C (июль 2015 г.). «Продвигая иглу - как остановить вспышку ВИЧ в сельских районах Индианы». Медицинский журнал Новой Англии. 373 (5): 397–9. Дои:10.1056 / NEJMp1507252. PMID 26106947.
- ^ МакЭверс, Келли (31 марта 2016 г.). "Встроенный". NPR.org.
- ^ а б Стаффа Дж. (13 марта 2017 г.). Совместное заседание Консультативного комитета по безопасности лекарственных средств и управлению рисками (DSaRM) и Консультативного комитета по обезболивающим и анальгетическим препаратам (AADPAC): вопросы постмаркетинговой безопасности, связанные с переработанной Opana ER®(США, Управление по контролю за продуктами и лекарствами США, надзор и эпидемиология).
- ^ а б Питерс, Филип Дж .; Понтонес, Памела; Гувер, Карен В .; Patel, Monita R .; Галанг, Ромео Р .; Шилдс, Джессика; Blosser, Сара Дж .; Спиллер, Майкл У .; Комбс, Бретань (21.07.2016). «ВИЧ-инфекция, связанная с инъекционным употреблением оксиморфона в Индиане, 2014–2015 годы». Медицинский журнал Новой Англии. 375 (3): 229–239. Дои:10.1056 / nejmoa1515195. ISSN 0028-4793. PMID 27468059.
- ^ Палмер, Эрик (6 июля 2017 г.). «Пещеры Эндо под давлением FDA вытянут Opana ER с рынка». Fierce Pharma. Получено 26 октября, 2017.
