Атом - Atom
| Атом | |
|---|---|
 Иллюстрация гелий атом, изображающий ядро (розовый) и электронное облако раздача (черный). Ядро (вверху справа) в гелии-4 на самом деле сферически симметрично и очень похоже на электронное облако, хотя для более сложных ядер это не всегда так. Черная полоса - это одна ангстрем (10−10 м или же 100 вечера). | |
| Классификация | |
| Наименьшее признанное деление химического элемента | |
| Характеристики | |
| Диапазон масс | 1.67×10−27 к 4.52×10−25 кг |
| Электрический заряд | нулевой (нейтральный), или ион обвинять |
| Диаметр классифицировать | 62 вечера (Он ) до 520 вечера (CS ) (страница данных ) |
| Составные части | Электроны и компактный ядро из протоны и нейтроны |
An атом наименьшая единица обычного иметь значение что образует химический элемент. Каждый твердый, жидкость, газ, и плазма состоит из нейтральных или ионизированный атомы. Атомы очень маленькие, обычно около 100пикометры через. Они настолько малы, что точно предсказывают их поведение с помощью классическая физика - как если бы это были теннисные мячи, например - невозможно из-за квантовые эффекты.
Каждый атом состоит из ядро и один или несколько электроны связаны с ядром. Ядро состоит из одного или нескольких протоны и ряд нейтроны. Только самая распространенная разновидность водород не имеет нейтронов. Более 99,94% атомного масса находится в ядре. Протоны имеют положительный электрический заряд, электроны имеют отрицательный электрический заряд, а нейтроны не имеют электрического заряда. Если количество протонов и электронов равно, то атом электрически нейтрален. Если у атома больше или меньше электронов, чем протонов, то он имеет общий отрицательный или положительный заряд соответственно - такие атомы называются ионы.
Электроны атома притягиваются к протонам атомного ядра электромагнитная сила. Протоны и нейтроны в ядре притягиваются друг к другу ядерная сила. Эта сила обычно сильнее, чем электромагнитная сила, которая отталкивает положительно заряженные протоны друг от друга. При определенных обстоятельствах отталкивающая электромагнитная сила становится сильнее ядерной. В этом случае ядро раскол и оставляет за собой разные элементы. Это форма ядерный распад.
Число протонов в ядре - это атомный номер и он определяет, к какому химическому элементу принадлежит атом. Например, любой атом, содержащий 29 протонов, равен медь. Количество нейтронов определяет изотоп элемента. Атомы могут присоединяться к одному или нескольким другим атомам посредством химические связи формировать химические соединения Такие как молекулы или же кристаллы. Способность атомов объединяться и диссоциировать ответственна за большинство физических изменений, наблюдаемых в природе. Химия это дисциплина, изучающая эти изменения.
История атомной теории
В философии
Основная идея о том, что материя состоит из крошечных неделимых частиц, очень старая, она появилась во многих древних культурах, таких как Греция и Индия. Эта древняя идея была основана на философских рассуждениях, а не на научных рассуждениях, и современная атомная теория не основана на этих старых концепциях. Слово атом происходит от греческого слова атомос, что означает «неразрезанный».[1][2]
Закон множественных пропорций далтона

В начале 1800-х годов Джон Далтон собрал экспериментальные данные, собранные им самим и другими учеными, и обнаружил закономерность, известную теперь как "закон множественных пропорций Он заметил, что в химических соединениях, которые содержат конкретный химический элемент, содержание этого элемента в этих соединениях будет отличаться соотношением небольших целых чисел. Этот образец подсказал Дальтону, что каждый химический элемент соединяется с другими посредством некоторой основной и согласованной единицы. массы.
Например, есть два типа оксид олова: один представляет собой черный порошок, содержащий 88,1% олова и 11,9% кислорода, а другой - белый порошок, состоящий на 78,7% из олова и 21,3% кислорода. Корректируя эти цифры, в черном оксиде содержится около 13,5 г кислорода на каждые 100 г олова, а в белом оксиде - примерно 27 г кислорода на каждые 100 г олова. 13,5 и 27 образуют соотношение 1: 2. В этих оксидах на каждый атом олова приходится один или два атома кислорода соответственно (SnO и SnO2 ).[3][4]
В качестве второго примера Далтон рассмотрел два оксиды железа: черный порошок, состоящий на 78,1% из железа и 21,9% кислорода, и красный порошок из 70,4% железа и 29,6% кислорода. Корректируя эти цифры, в черном оксиде содержится около 28 г кислорода на каждые 100 г железа, а в красном оксиде - около 42 г кислорода на каждые 100 г железа. 28 и 42 образуют соотношение 2: 3. В этих соответствующих оксидах на каждые два атома железа приходится два или три атома кислорода (Fe2О2 и Fe2О3 ).[а][5][6]
В качестве последнего примера: оксид азота 63,3% азота и 36,7% кислорода, оксид азота состоит из 44,05% азота и 55,95% кислорода, и диоксид азота составляет 29,5% азота и 70,5% кислорода - поправляя цифры, на каждые 140 г азота в этих оксидах приходится около 80 г, 160 г и 320 г кислорода соответственно, что дает соотношение 1: 2: 4. Соответствующие формулы для этих оксидов: N2О, НЕТ, и НЕТ2.[7][8]
Кинетическая теория газов
В конце 18 века ряд ученых обнаружили, что они могут лучше объяснить поведение газов, описывая их как совокупность субмикроскопических частиц и моделируя их поведение, используя статистика и вероятность. В отличие от атомной теории Дальтона, кинетическая теория газов описывает не то, как газы химически реагируют друг с другом с образованием соединений, а их физическое поведение: диффузия, вязкость, проводимость, давление и т. Д.
Броуновское движение
В 1827 г. ботаник Роберт Браун использовал микроскоп, чтобы посмотреть на частицы пыли, плавающие в воде, и обнаружил, что они беспорядочно перемещаются, явление, которое стало известно как "Броуновское движение ". Считалось, что это вызвано ударами молекул воды по зернам. В 1905 году Альберт Эйнштейн доказал реальность этих молекул и их движений, создав первые статистическая физика анализ Броуновское движение.[9][10][11] Французский физик Жан Перрен использовали работу Эйнштейна для экспериментального определения массы и размеров молекул, тем самым предоставив физические доказательства корпускулярной природы материи.[12]
Открытие электрона
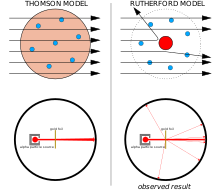
Оставили: Ожидаемые результаты: альфа-частицы проходят через модель атома с пренебрежимо малым отклонением.
Правильно: Наблюдаемые результаты: небольшая часть частиц отклонялась концентрированным положительным зарядом ядра.
В 1897 г. Дж. Дж. Томсон обнаружил, что катодные лучи не электромагнитные волны, а состоят из частиц, которые в 1800 раз легче, чем водород (легчайший атом). Томсон пришел к выводу, что эти частицы пришли из атомов внутри катода - они были субатомный частицы. Он назвал эти новые частицы тельца но позже они были переименованы электроны. Томсон также показал, что электроны идентичны частицам, испускаемым фотоэлектрический и радиоактивные материалы.[13] Было быстро признано, что электроны - это частицы, несущие электрические токи в металлических проводах. Томсон пришел к выводу, что эти электроны выходят из самих атомов катода в его приборах, а это означает, что атомы не неделимы, как следует из названия. атомос предлагает.
Открытие ядра
Дж. Дж. Томсон считал, что отрицательно заряженные электроны были распределены по всему атому в море положительного заряда, которое было распределено по всему объему атома.[14] Эту модель иногда называют сливовый пудинг модель.
Эрнест Резерфорд и его коллеги Ганс Гейгер и Эрнест Марсден у них возникли сомнения по поводу модели Томсона после того, как они столкнулись с трудностями при попытке построить прибор для измерения отношения заряда к массе альфа-частицы (это положительно заряженные частицы, испускаемые некоторыми радиоактивными веществами, такими как радий ). Альфа-частицы рассеивались воздухом в камере обнаружения, что делало измерения ненадежными. Томсон столкнулся с подобной проблемой в своей работе над катодными лучами, которую он решил, создав почти идеальный вакуум в своих инструментах. Резерфорд не думал, что столкнется с той же проблемой, потому что альфа-частицы намного тяжелее электронов. Согласно модели атома Томсона, положительный заряд в атоме недостаточно сконцентрирован для создания электрического поля, достаточно сильного, чтобы отклонить альфа-частицу, а электроны настолько легкие, что их должны легко отталкивать гораздо более тяжелые альфа-частицы. Тем не менее, рассеяние было, поэтому Резерфорд и его коллеги решили тщательно исследовать это рассеяние.[15]
Между 1908 и 1913 годами Рутфорд и его коллеги провели серию экспериментов, в которых они бомбардировали тонкие металлические фольги альфа-частицами. Они заметили альфа-частицы, отклоняющиеся на угол более 90 °. Чтобы объяснить это, Резерфорд предположил, что положительный заряд атома не распределяется по объему атома, как полагал Томсон, а сосредоточен в крошечном ядре в центре. Только такая интенсивная концентрация заряда может создать электрическое поле, достаточно сильное, чтобы отклонить альфа-частицы, как это наблюдается.[15]
Открытие изотопов
Экспериментируя с продуктами радиоактивный распад, в 1913 г. радиохимик Фредерик Содди обнаружил, что, по-видимому, существует более одного типа атомов в каждой позиции на периодическая таблица.[16] Период, термин изотоп был придуман Маргарет Тодд как подходящее название для разных атомов, принадлежащих одному элементу. Дж. Дж. Томсон создал технику для разделение изотопов через его работу над ионизированные газы, что впоследствии привело к открытию стабильные изотопы.[17]
Модель Бора

В 1913 г. физик Нильс Бор предложила модель, в которой предполагалось, что электроны атома вращаются вокруг ядра, но могли делать это только на конечном наборе орбит и могли прыгать между этими орбитами только при дискретных изменениях энергии, соответствующих поглощению или излучению фотона.[18] Это квантование использовалось, чтобы объяснить, почему орбиты электронов стабильны (учитывая, что обычно заряды при ускорении, включая круговое движение, теряют кинетическую энергию, которая излучается как электромагнитное излучение, см. синхротронное излучение ) и почему элементы поглощают и излучают электромагнитное излучение в дискретных спектрах.[19]
Позже в том же году Генри Мозли предоставили дополнительные экспериментальные доказательства в пользу Теория Нильса Бора. Эти результаты уточнены Эрнест Резерфорд 'песок Антониус ван ден Брук модель, которая предполагала, что атом содержит в своем ядро ряд положительных ядерные заряды что равно его (атомному) номеру в периодической таблице. До этих экспериментов атомный номер не была известна как физическая и экспериментальная величина. То, что он равен заряду атомного ядра, остается общепринятой атомной моделью сегодня.[20]
Химические связи между атомами были объяснены Гилберт Ньютон Льюис в 1916 году, как взаимодействия между составляющими их электронами.[21] Поскольку химические свойства элементов, как известно, в значительной степени повторяются в соответствии с периодический закон,[22] в 1919 году американский химик Ирвинг Ленгмюр предположил, что это можно объяснить, если электроны в атоме каким-то образом связаны или сгруппированы. Считалось, что группы электронов занимают набор электронные оболочки про ядро.[23]
Модель атома Бора была первой полной физической моделью атома. Он описал общую структуру атома, как атомы связаны друг с другом, и предсказал спектральные линии водорода. Модель Бора не была идеальной и вскоре была заменена более точной моделью Шредингера, но ее было достаточно, чтобы развеять все оставшиеся сомнения в том, что материя состоит из атомов. Для химиков идея атома была полезным эвристическим инструментом, но физики сомневались в том, действительно ли материя состоит из атомов, поскольку никто еще не разработал полную физическую модель атома.
Модель Шредингера
В Эксперимент Штерна-Герлаха 1922 г. предоставил дополнительные доказательства квантовой природы атомных свойств. Когда пучок атомов серебра пропускался через магнитное поле особой формы, пучок разделялся в соответствии с направлением углового момента атома, или вращение. Поскольку это направление вращения изначально является случайным, можно ожидать, что луч отклонится в случайном направлении. Вместо этого луч был разделен на две направленные компоненты, соответствующие атомной вращение быть ориентированным вверх или вниз по отношению к магнитному полю.[24]
В 1925 г. Вернер Гейзенберг опубликовал первую последовательную математическую формулировку квантовой механики (матричная механика ).[20] Годом ранее Луи де Бройль предложил гипотеза де Бройля: все частицы в некоторой степени ведут себя как волны,[25] и в 1926 г. Эрвин Шредингер использовал эту идею для разработки Уравнение Шредингера, математическая модель атома (волновая механика), описывающая электроны как трехмерные формы волны а не точечные частицы.[26]
Следствием использования форм волны для описания частиц является то, что математически невозможно получить точные значения как для позиция и импульс частицы в данный момент времени; это стало известно как принцип неопределенности, сформулированный Вернер Гейзенберг в 1927 г.[20] Согласно этой концепции, для данной точности измерения положения можно было получить только диапазон вероятных значений импульса, и наоборот.[27]Эта модель смогла объяснить наблюдения за поведением атомов, которые не могли объяснить предыдущие модели, например, определенные структурные и спектральный узоры атомов крупнее водорода. Таким образом, планетарная модель атома была отвергнута в пользу модели, описывающей атомная орбиталь зоны вокруг ядра, в которых наиболее вероятно наблюдение данного электрона.[28][29]
Открытие нейтрона
Развитие масс-спектрометр позволило с повышенной точностью измерять массу атомов. Устройство использует магнит, чтобы искривлять траекторию пучка ионов, а величина отклонения определяется отношением массы атома к его заряду. Химик Фрэнсис Уильям Астон использовали этот инструмент, чтобы показать, что изотопы имеют разные массы. В атомная масса этих изотопов варьируются в целых количествах, называемых правило целых чисел.[30] Объяснение этих различных изотопов ожидало открытия нейтрон, незаряженная частица с массой, подобной протон, физиком Джеймс Чедвик в 1932 году. Затем изотопы были объяснены как элементы с одинаковым числом протонов, но разным числом нейтронов в ядре.[31]
Деление, физика высоких энергий и конденсированные вещества
В 1938 году немецкий химик Отто Хан, ученик Резерфорда, направил нейтроны на атомы урана, надеясь получить трансурановые элементы. Вместо этого его химические эксперименты показали барий как продукт.[32][33] Год спустя, Лиз Мейтнер и ее племянник Отто Фриш подтвердил, что результаты Хана были первым экспериментальным ядерное деление.[34][35] В 1944 году Хан получил Нобелевская премия по химии. Несмотря на усилия Хана, вклад Мейтнер и Фриш не получил признания.[36]
В 1950-х годах разработка улучшенных ускорители частиц и детекторы частиц позволил ученым изучить влияние атомов, движущихся с высокими энергиями.[37] Нейтроны и протоны оказались адроны, или композиты из более мелких частиц, называемые кварки. В стандартная модель физики элементарных частиц был разработан, который до сих пор успешно объяснил свойства ядра с точки зрения этих субатомных частиц и сил, которые управляют их взаимодействиями.[38]
Структура
Субатомные частицы
Хотя слово атом первоначально обозначал частицу, которая не может быть разрезана на более мелкие частицы, в современном научном использовании атом состоит из различных субатомные частицы. Составляющие частицы атома электрон, то протон и нейтрон.
Электрон является наименее массивной из этих частиц на 9.11×10−31 кг, с отрицательным электрический заряд и размер, который слишком мал, чтобы его можно было измерить с помощью доступных методов.[39] Это была самая легкая частица с положительной измеренной массой покоя до открытия нейтрино масса. В обычных условиях электроны связаны с положительно заряженным ядром притяжением, создаваемым противоположными электрическими зарядами. Если у атома больше или меньше электронов, чем его атомный номер, тогда он становится соответственно отрицательно или положительно заряженным в целом; заряженный атом называется ион. Электроны известны с конца 19 века, в основном благодаря J.J. Томсон; видеть история субатомной физики для подробностей.
Протоны имеют положительный заряд и массу в 1836 раз больше, чем у электрона. 1.6726×10−27 кг. Число протонов в атоме называется его атомный номер. Эрнест Резерфорд (1919) наблюдали, что азот при бомбардировке альфа-частицами выбрасывает ядра водорода. К 1920 году он признал, что ядро водорода - это отдельная частица в атоме, и назвал его протон.
Нейтроны не имеют электрического заряда и имеют свободную массу в 1839 раз больше массы электрона, или 1.6749×10−27 кг.[40][41] Нейтроны - самые тяжелые из трех составляющих частиц, но их массу можно уменьшить за счет энергия связи ядра. Нейтроны и протоны (вместе известные как нуклоны ) имеют сопоставимые размеры - порядка 2.5×10−15 м- хотя «поверхность» этих частиц четко не определена.[42] Нейтрон был открыт в 1932 году английским физиком. Джеймс Чедвик.
в Стандартная модель По физике электроны - это действительно элементарные частицы без внутренней структуры, тогда как протоны и нейтроны - составные частицы, состоящие из элементарные частицы называется кварки. В атомах есть два типа кварков, каждый из которых имеет небольшой электрический заряд. Протоны состоят из двух до кварков (каждый с зарядом +2/3) и один вниз кварк (с зарядом -1/3). Нейтроны состоят из одного верхнего кварка и двух нижних кварков. Это различие объясняет разницу в массе и заряде двух частиц.[43][44]
Кварки удерживаются вместе сильное взаимодействие (или сильная сила), которая опосредуется глюоны. Протоны и нейтроны, в свою очередь, удерживаются друг с другом в ядре за счет ядерная сила, который является остатком сильного взаимодействия, имеющего несколько иные свойства дальности (подробнее см. статью о ядерном взаимодействии). Глюон является членом семейства калибровочные бозоны, которые являются элементарными частицами, передающими физические силы.[43][44]
Ядро

Все связанные протоны и нейтроны в атоме составляют крошечный атомное ядро, и все вместе называются нуклоны. Радиус ядра примерно равен фемтометры, куда - полное число нуклонов.[45] Это намного меньше радиуса атома, который составляет порядка 105 фм. Нуклоны связаны между собой короткодействующим потенциалом притяжения, называемым остаточная сильная сила. На расстояниях менее 2,5 фм эта сила намного сильнее, чем электростатическая сила это заставляет положительно заряженные протоны отталкиваться друг от друга.[46]
Атомы того же элемент имеют одинаковое количество протонов, называемых атомный номер. В пределах одного элемента количество нейтронов может варьироваться, определяя изотоп этого элемента. Общее количество протонов и нейтронов определяет нуклид. Число нейтронов относительно протонов определяет стабильность ядра, при этом некоторые изотопы претерпевают радиоактивный распад.[47]
Протон, электрон и нейтрон классифицируются как фермионы. Фермионы подчиняются Принцип исключения Паули что запрещает идентичный фермионы, такие как несколько протонов, из одного и того же квантового состояния в одно и то же время. Таким образом, каждый протон в ядре должен находиться в квантовом состоянии, отличном от всех других протонов, и то же самое относится ко всем нейтронам ядра и ко всем электронам электронного облака.[48]
Ядро, в котором количество протонов отличается от количества нейтронов, потенциально может перейти в более низкое энергетическое состояние в результате радиоактивного распада, в результате которого количество протонов и нейтронов будет более точно совпадать. В результате атомы с совпадающим количеством протонов и нейтронов более устойчивы к распаду, но с увеличением атомного номера взаимное отталкивание протонов требует увеличения доли нейтронов для поддержания стабильности ядра.[48]
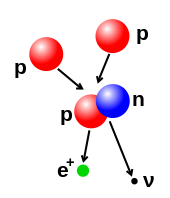
Число протонов и нейтронов в атомном ядре может быть изменено, хотя это может потребовать очень высоких энергий из-за сильного взаимодействия. Термоядерная реакция происходит, когда несколько атомных частиц соединяются с образованием более тяжелого ядра, например, в результате энергетического столкновения двух ядер. Например, в ядре Солнца протонам требуется энергия от 3 до 10 кэВ, чтобы преодолеть их взаимное отталкивание - кулоновский барьер - и сливаются в единое ядро.[49] Ядерное деление - противоположный процесс, в результате которого ядро расщепляется на два меньших ядра - обычно в результате радиоактивного распада. Ядро также можно модифицировать путем бомбардировки субатомными частицами высокой энергии или фотонами. Если это изменяет количество протонов в ядре, атом превращается в другой химический элемент.[50][51]
Если масса ядра после реакции слияния меньше суммы масс отдельных частиц, то разница между этими двумя значениями может быть выражена как тип используемой энергии (например, гамма-луч, или кинетическая энергия бета-частица ), как описано Альберт Эйнштейн с эквивалентность массы и энергии формула , куда потеря массы и это скорость света. Этот дефицит является частью энергия связи нового ядра, и именно невосполнимая потеря энергии заставляет слитые частицы оставаться вместе в состоянии, которое требует этой энергии для разделения.[52]
Слияние двух ядер, которые создают более крупные ядра с меньшими атомными номерами, чем утюг и никель - полное число нуклонов около 60 - обычно экзотермический процесс это высвобождает больше энергии, чем требуется для их объединения.[53] Именно этот процесс высвобождения энергии заставляет ядерный синтез в звезды Самоподдерживающаяся реакция. Для более тяжелых ядер энергия связи, приходящаяся на нуклон в ядре начинает уменьшаться. Это означает, что в процессах слияния образуются ядра с атомными номерами выше примерно 26, и атомные массы выше примерно 60, это эндотермический процесс. Эти более массивные ядра не могут подвергаться реакции синтеза, производящей энергию, которая может поддерживать гидростатическое равновесие звезды.[48]
Электронное облако

Электроны в атоме притягиваются к протонам ядра электромагнитная сила. Эта сила связывает электроны внутри электростатический потенциальная яма окружает меньшее ядро, что означает, что для выхода электрона необходим внешний источник энергии. Чем ближе электрон к ядру, тем больше сила притяжения. Следовательно, электронам, связанным около центра потенциальной ямы, требуется больше энергии для выхода, чем электронам, находящимся на большем расстоянии.
Электроны, как и другие частицы, обладают свойствами как частица и волна. Электронное облако - это область внутри потенциальной ямы, где каждый электрон образует своего рода трехмерную стоячая волна - форма волны, которая не движется относительно ядра. Это поведение определяется атомная орбиталь, математическая функция, которая характеризует вероятность того, что электрон окажется в определенном месте при измерении его положения.[54] Только дискретный (или квантованный ) набор этих орбиталей существует вокруг ядра, так как другие возможные волновые структуры быстро распадаются в более стабильную форму.[55] Орбитали могут иметь одну или несколько кольцевых или узловых структур и отличаются друг от друга размером, формой и ориентацией.[56]

Каждая атомная орбиталь соответствует определенному уровень энергии электрона. Электрон может изменить свое состояние на более высокий энергетический уровень, поглощая фотон с достаточной энергией, чтобы перевести его в новое квантовое состояние. Точно так же через спонтанное излучение, электрон в состоянии с более высокой энергией может перейти в состояние с более низкой энергией, при этом излучая избыточную энергию в виде фотона. Эти характерные значения энергии, определяемые разницей энергий квантовых состояний, ответственны за атомные спектральные линии.[55]
Количество энергии, необходимое для удаления или добавления электрона - энергия связи электрона - намного меньше, чем энергия связи нуклонов. Например, для снятия изоляции требуется всего 13,6 эВ. основное состояние электрон от атома водорода,[57] по сравнению с 2.23миллион эВ для расщепления дейтерий ядро.[58] Атомы электрически нейтральные, если в них равное количество протонов и электронов. Атомы, у которых есть либо дефицит, либо избыток электронов, называются ионы. Электроны, которые находятся дальше всего от ядра, могут быть переданы другим соседним атомам или разделены между атомами. По этому механизму атомы могут связь в молекулы и другие виды химические соединения подобно ионный и ковалентный сеть кристаллы.[59]
Характеристики
Ядерные свойства
По определению, любые два атома с одинаковым числом атомов протоны в своих ядрах принадлежат тем же химический элемент. Атомы с равным числом протонов, но разным числом нейтроны представляют собой разные изотопы одного и того же элемента. Например, все атомы водорода допускают ровно один протон, но существуют изотопы без нейтронов (водород-1, безусловно, самая распространенная форма,[60] также называется протием), один нейтрон (дейтерий ), два нейтрона (тритий ) и более двух нейтронов. Известные элементы образуют набор атомных номеров из однопротонного элемента водород до 118-протонного элемента Оганессон.[61] Все известные изотопы элементов с атомными номерами больше 82 являются радиоактивными, хотя радиоактивность элемента 83 (висмут ) настолько мала, что ею можно пренебречь.[62][63]
Около 339 нуклидов встречаются в природе земной шар,[64] из которых 252 (около 74%) распада не наблюдались и называются "стабильные изотопы ". Только 90 нуклидов стабильны. теоретически, в то время как еще 162 (в результате чего общее число составило 252) распада не наблюдалось, хотя теоретически это энергетически возможно. Они также формально классифицируются как «стабильные». Еще 34 радиоактивных нуклида имеют период полураспада более 100 миллионов лет и достаточно долгоживущие, чтобы присутствовать с момента рождения Солнечная система. Эта коллекция из 286 нуклидов известна как первичные нуклиды. Наконец, известно, что еще 53 короткоживущих нуклида встречаются в природе в качестве дочерних продуктов распада первичных нуклидов (таких как радий из уран ), или как продукты естественных энергетических процессов на Земле, таких как бомбардировка космическими лучами (например, углерод-14).[65][примечание 1]
Для 80 химических элементов не менее одного стабильный изотоп существуют. Как правило, для каждого из этих элементов существует всего несколько стабильных изотопов, в среднем 3,2 стабильных изотопа на элемент. Двадцать шесть элементов имеют только один стабильный изотоп, в то время как наибольшее количество стабильных изотопов, наблюдаемых для любого элемента, равно десяти, для элемента банка. Элементы 43, 61, и все элементы пронумерованы 83 или выше не имеют стабильных изотопов.[66]:1–12
На стабильность изотопов влияет соотношение протонов и нейтронов, а также наличие определенных «магических чисел» нейтронов или протонов, которые представляют собой замкнутые и заполненные квантовые оболочки. Эти квантовые оболочки соответствуют набору уровней энергии внутри модель оболочки ядра; заполненные оболочки, такие как заполненная оболочка из 50 протонов для олова, придает нуклиду необычную стабильность. Из 252 известных стабильных нуклидов только четыре имеют нечетное число протонов. и нечетное количество нейтронов: водород-2 (дейтерий ), литий-6, бор-10 и азот-14. Кроме того, только четыре встречающихся в природе радиоактивных нечетных нуклида имеют период полураспада более миллиарда лет: калий-40, ванадий-50, лантан-138 и тантал-180м. Большинство нечетно-нечетных ядер крайне нестабильны по отношению к бета-распад, потому что продукты распада четно-четные и, следовательно, более сильно связаны за счет эффекты спаривания ядер.[67]
Масса
Большая часть массы атома приходится на протоны и нейтроны, из которых он состоит. Общее количество этих частиц (называемых «нуклонами») в данном атоме называется массовое число. Это положительное целое число и безразмерно (вместо измерения массы), потому что оно выражает количество. Пример использования массового числа - «углерод-12», который имеет 12 нуклонов (шесть протонов и шесть нейтронов).
Настоящий масса покоящегося атома часто выражается в дальтон (Da), также называемая единой атомной единицей массы (u). Эта единица определяется как двенадцатая часть массы свободного нейтрального атома углерод-12, что примерно 1.66×10−27 кг.[68] Водород-1 (самый легкий изотоп водорода, который также является нуклидом с наименьшей массой) имеет атомный вес 1,007825 Да.[69] Значение этого числа называется атомная масса. У данного атома атомная масса приблизительно равна (в пределах 1%) его массовому числу, умноженному на атомную единицу массы (например, масса азота-14 составляет примерно 14 Да), но это число не будет точно целым, за исключением ( по определению) в случае углерода-12.[70] Наитяжелейший стабильный атом свинец-208,[62] с массой 207.9766521 Да.[71]
Поскольку даже самые массивные атомы слишком легки, чтобы работать с ними напрямую, химики вместо этого используют единицу родинки. Один моль атомов любого элемента всегда имеет одинаковое количество атомов (около 6.022×1023 ). Это число было выбрано таким образом, чтобы, если элемент имеет атомную массу 1 u, моль атомов этого элемента имеет массу, близкую к одному грамму. Из-за определения единая атомная единица массы, каждый атом углерода-12 имеет атомную массу ровно 12 Да, поэтому моль атомов углерода-12 весит точно 0,012 кг.[68]
Форма и размер
Атомы не имеют четко определенной внешней границы, поэтому их размеры обычно описываются в терминах радиус атома. Это мера расстояния, на которое электронное облако простирается от ядра.[72] Это предполагает, что атом имеет сферическую форму, которая характерна только для атомов в вакууме или свободном пространстве. Атомные радиусы могут быть получены из расстояний между двумя ядрами, когда два атома соединены в одну химическая связь. Радиус зависит от расположения атома на атомной диаграмме, типа химической связи, количества соседних атомов (координационный номер ) и квантово-механический собственность, известная как вращение.[73] На периодическая таблица Для элементов размер атома имеет тенденцию увеличиваться при перемещении вниз по столбцам, но уменьшается при перемещении по строкам (слева направо).[74] Следовательно, самым маленьким атомом является гелий радиусом 32вечера, а один из крупнейших - цезий в 225 часов вечера.[75]
Под воздействием внешних сил, например электрические поля, форма атома может отличаться от сферическая симметрия. Деформация зависит от величины поля и орбитального типа электронов внешней оболочки, как показано теоретико-групповой соображения. Асферические отклонения могут возникать, например, в кристаллы, где большие кристаллические электрические поля могут возникать при низкая симметрия узлы решетки.[76][77] Существенный эллипсоидальный было показано, что деформации происходят для ионов серы[78] и халькоген ионы[79] в пирит соединения типа.
Атомные размеры в тысячи раз меньше длины волны свет (400–700 нм ), поэтому их нельзя просмотреть с помощью оптический микроскоп, хотя отдельные атомы можно наблюдать с помощью сканирующий туннельный микроскоп. Чтобы представить себе миниатюрность атома, представьте, что типичный человеческий волос составляет около 1 миллиона атомов углерода в ширину.[80] В одной капле воды содержится около 2секстиллион (2×1021) атомов кислорода и вдвое больше атомов водорода.[81] Один карат алмаз с массой 2×10−4 кг содержит около 10 секстиллионов (1022) атомы углерод.[заметка 2] Если бы яблоко было увеличено до размеров Земли, то атомы в яблоке были бы примерно размером с исходное яблоко.[82]
Радиоактивный распад

Каждый элемент имеет один или несколько изотопов с нестабильными ядрами, которые подвержены радиоактивному распаду, в результате чего ядро испускает частицы или электромагнитное излучение. Радиоактивность может возникать, когда радиус ядра велик по сравнению с радиусом сильного взаимодействия, которое действует только на расстояниях порядка 1 фм.[83]
Наиболее распространенные формы радиоактивного распада:[84][85]
- Альфа-распад: этот процесс возникает, когда ядро испускает альфа-частицу, которая представляет собой ядро гелия, состоящее из двух протонов и двух нейтронов. Результатом выброса является новый элемент с более низким атомный номер.
- Бета-распад (и захват электронов ): эти процессы регулируются слабая сила, и возникают в результате превращения нейтрона в протон или протона в нейтрон. Переход нейтрона в протон сопровождается испусканием электрона и антинейтрино, в то время как переход протона в нейтрон (за исключением захвата электрона) вызывает испускание позитрон и нейтрино. Эмиссия электронов или позитронов называется бета-частицами. Бета-распад увеличивает или уменьшает атомный номер ядра на единицу. Захват электронов более распространен, чем эмиссия позитронов, потому что для этого требуется меньше энергии. В этом типе распада ядром поглощается электрон, а не позитрон, испускаемый ядром. При этом по-прежнему испускается нейтрино, а протон превращается в нейтрон.
- Гамма-распад: этот процесс является результатом изменения уровня энергии ядра в более низкое состояние, что приводит к испусканию электромагнитного излучения. Возбужденное состояние ядра, которое приводит к гамма-излучению, обычно возникает после испускания альфа- или бета-частицы. Таким образом, гамма-распад обычно следует за альфа- или бета-распадом.
Другие более редкие виды радиоактивный распад включают выброс нейтронов или протонов или кластеров нуклоны из ядра или более чем одного бета-частица. Аналогом гамма-излучения, которое позволяет возбужденным ядрам по-другому терять энергию, является внутренняя конверсия - процесс, который производит высокоскоростные электроны, которые не являются бета-лучами, с последующим образованием высокоэнергетических фотонов, которые не являются гамма-лучами. Несколько крупных ядер взрываются на два или более заряженных фрагмента различной массы плюс несколько нейтронов в результате распада, называемого спонтанным. ядерное деление.
Каждый радиоактивный изотоп имеет характерный период затухания - период полураспада - это определяется количеством времени, которое требуется для распада половины образца. Это экспоненциальный спад процесс, который неуклонно снижает долю оставшегося изотопа на 50% за каждый период полураспада. Следовательно, по прошествии двух периодов полураспада присутствует только 25% изотопа и так далее.[83]
Магнитный момент
Элементарные частицы обладают внутренним квантово-механическим свойством, известным как вращение. Это аналогично угловой момент объекта, который вращается вокруг своего центр массы, хотя, строго говоря, эти частицы считаются точечными, и нельзя сказать, что они вращаются. Отжим измеряется в единицах уменьшенного Постоянная Планка (ħ), причем электроны, протоны и нейтроны имеют спин ½ ħ, или «спин-½». В атоме электроны, движущиеся вокруг ядро обладать орбитальным угловой момент в дополнение к их спину, а само ядро обладает угловым моментом из-за своего ядерного спина.[86]
В магнитное поле произведенный атомом - его магнитный момент - определяется этими различными формами углового момента, точно так же, как вращающийся заряженный объект классически создает магнитное поле, но основной вклад вносит спин электрона. Из-за природы электронов подчиняться Принцип исключения Паули, в котором нельзя найти два электрона в одном квантовое состояние, связанные электроны образуют пары друг с другом, причем один член каждой пары находится в состоянии со спином вверх, а другой - в противоположном состоянии со спином вниз. Таким образом, эти спины компенсируют друг друга, уменьшая общий магнитный дипольный момент до нуля в некоторых атомах с четным числом электронов.[87]
В ферромагнитный таких элементов, как железо, кобальт и никель, нечетное количество электронов приводит к неспаренному электрону и чистому общему магнитному моменту. Орбитали соседних атомов перекрываются, и более низкое энергетическое состояние достигается, когда спины неспаренных электронов выровнены друг с другом, спонтанный процесс, известный как обменное взаимодействие. Когда магнитные моменты ферромагнитных атомов выровнены, материал может создавать измеримое макроскопическое поле. Парамагнитные материалы имеют атомы с магнитными моментами, которые выстраиваются в случайных направлениях, когда магнитное поле отсутствует, но магнитные моменты отдельных атомов выстраиваются в линию в присутствии поля.[87][88]
У ядра атома не будет спина, если в нем четное число нейтронов и протонов, но в других случаях нечетных чисел ядро может иметь спин. Обычно ядра со спином выстраиваются в случайных направлениях из-за тепловое равновесие, но для определенных элементов (например, ксенон-129 ) можно поляризовать значительная часть ядерных спиновых состояний, так что они выровнены в одном направлении - условие, называемое гиперполяризация. Это имеет важные приложения в магнитно-резонансная томография.[89][90]
Уровни энергии
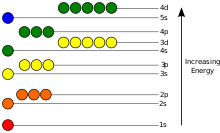
В потенциальная энергия электрона в атоме отрицательный относительно того, когда расстояние из ядра уходит в бесконечность; его зависимость от электронного позиция достигает минимум внутри ядра, примерно в обратная пропорция на расстояние. В квантово-механической модели связанный электрон может занимать только набор состояния с центром на ядре, и каждое состояние соответствует определенному уровень энергии; видеть не зависящее от времени уравнение Шредингера для теоретического объяснения. Уровень энергии можно измерить количество энергии, необходимое для развязывания электрон от атома, и обычно дается в единицах электронвольт (эВ). Наинизшее энергетическое состояние связанного электрона называется основным состоянием, т.е. стационарное состояние, а переход электрона на более высокий уровень приводит к возбужденному состоянию.[91] Энергия электрона увеличивается вместе с п потому что (среднее) расстояние до ядра увеличивается. Зависимость энергии от ℓ вызвано не электростатический потенциал ядра, но за счет взаимодействия между электронами.
Чтобы электрон переход между двумя разными состояниями, например основное состояние к первому возбужденное состояние, он должен поглощать или излучать фотон при энергии, соответствующей разнице в потенциальной энергии этих уровней, согласно Нильс Бор модель, что может быть точно рассчитано Уравнение Шредингера Электроны прыгают между орбиталями подобно частицам. Например, если один фотон ударяет по электрону, только один электрон меняет состояние в ответ на этот фотон; видеть Электронные свойства.
Энергия излучаемого фотона пропорциональна его энергии. частота, поэтому эти конкретные уровни энергии появляются в виде отдельных полос на электромагнитный спектр.[92] Каждый элемент имеет характерный спектр, который может зависеть от заряда ядра, подоболочек, заполненных электронами, электромагнитных взаимодействий между электронами и других факторов.[93]

Когда непрерывный спектр энергии проходит через газ или плазму, некоторые фотоны поглощаются атомами, заставляя электроны менять свой уровень энергии. Те возбужденные электроны, которые остаются связанными со своим атомом, спонтанно излучают эту энергию в виде фотона, перемещаясь в случайном направлении, и, таким образом, возвращаются на более низкие уровни энергии. Таким образом, атомы ведут себя как фильтр, образующий серию темных полосы поглощения в выходной энергии. (Наблюдатель, рассматривающий атомы с точки зрения, не включающей непрерывный спектр на заднем плане, вместо этого видит серию эмиссионные линии от фотонов, испускаемых атомами.) Спектроскопический измерения прочности и ширины атомные спектральные линии позволяют определить состав и физические свойства вещества.[94]
Внимательное изучение спектральных линий показывает, что некоторые из них тонкая структура расщепление. Это происходит из-за спин-орбитальная связь, которое представляет собой взаимодействие между спином и движением самого удаленного электрона.[95] Когда атом находится во внешнем магнитном поле, спектральные линии разделяются на три или более компонентов; явление, называемое Эффект Зеемана. Это вызвано взаимодействием магнитного поля с магнитным моментом атома и его электронов. Некоторые атомы могут иметь несколько электронные конфигурации с тем же уровнем энергии, которые, таким образом, выглядят как одна спектральная линия. Взаимодействие магнитного поля с атомом сдвигает эти электронные конфигурации на несколько разные уровни энергии, что приводит к появлению нескольких спектральных линий.[96] Наличие внешнего электрическое поле может вызвать сравнимое расщепление и сдвиг спектральных линий за счет изменения уровней энергии электронов, явление, называемое Эффект Старка.[97]
Если связанный электрон находится в возбужденном состоянии, взаимодействующий фотон с соответствующей энергией может вызвать стимулированное излучение фотона с соответствующим уровнем энергии. Чтобы это произошло, электрон должен перейти в состояние с более низкой энергией, разность энергий которого соответствует энергии взаимодействующего фотона. Излучаемый фотон и взаимодействующий фотон затем движутся параллельно и с совпадающими фазами. То есть волновые структуры двух фотонов синхронизированы. Это физическое свойство используется для создания лазеры, который может излучать когерентный луч световой энергии в узкой полосе частот.[98]
Валентность и связывающее поведение
Валентность - это объединяющая сила элемента. Он определяется количеством связей, которые он может образовывать с другими атомами или группами.[99] Самая внешняя электронная оболочка атома в несвязанном состоянии известна как валентной оболочки, а электроны в этой оболочке называются валентные электроны. Количество валентных электронов определяет связь поведение с другими атомами. Атомы склонны химически реагировать друг с другом таким образом, чтобы заполнить (или опустошить) их внешние валентные оболочки.[100] Например, перенос одного электрона между атомами является полезным приближением для связей, которые образуются между атомами, у которых на один электрон больше, чем у заполненной оболочки, и других, которые на один электрон меньше полной оболочки, например, в соединении хлорид натрия и другие химические ионные соли. Многие элементы обладают множественной валентностью или склонностью разделять разное количество электронов в разных соединениях. Таким образом, химическая связь Между этими элементами происходит много форм обмена электронами, которые представляют собой нечто большее, чем простой перенос электронов. Примеры включают элемент углерод и органические соединения.[101]
В химические элементы часто отображаются в периодическая таблица который предназначен для отображения повторяющихся химических свойств, а элементы с одинаковым числом валентных электронов образуют группу, которая выровнена в одном столбце таблицы. (Горизонтальные строки соответствуют заполнению квантовой оболочки электронами.) Внешняя оболочка элементов в дальнем правом углу таблицы полностью заполнена электронами, в результате чего образуются химически инертные элементы, известные как благородные газы.[102][103]
состояния

Количество атомов находится в различных состояниях материи, которые зависят от физических условий, таких как температура и давление. Варьируя условия, материалы могут переходить между твердые вещества, жидкости, газы и плазма.[104] Внутри государства материал также может существовать в разных аллотропы. Примером этого является твердый углерод, который может существовать как графит или же алмаз.[105] Также существуют газообразные аллотропы, такие как дикислород и озон.
При температурах, близких к абсолютный ноль, атомы могут образовывать Конденсат Бозе-Эйнштейна, в этот момент квантово-механические эффекты, которые обычно наблюдаются только в атомном масштабе, становятся очевидными в макроскопическом масштабе.[106][107] Этот переохлажденный набор атомов затем ведет себя как единый супер атом, что может позволить фундаментальные проверки квантово-механического поведения.[108]
Идентификация

Хотя атомы слишком малы, чтобы их можно было увидеть, такие устройства, как сканирующий туннельный микроскоп (STM) позволяют визуализировать их на поверхности твердых тел. В микроскопе используется квантовое туннелирование явление, которое позволяет частицам проходить через барьер, который с классической точки зрения был бы непреодолимым. Электроны туннелируют сквозь вакуум между двумя пристрастный электроды, обеспечивающие туннельный ток, который экспоненциально зависит от их расстояния. Один электрод представляет собой острый наконечник, в идеале заканчивающийся одним атомом. В каждой точке сканирования поверхности высота наконечника регулируется таким образом, чтобы туннельный ток оставался на заданном уровне. То, насколько наконечник перемещается к поверхности и от нее, интерпретируется как профиль высоты. При низком смещении микроскоп отображает усредненные электронные орбитали на плотно упакованных уровнях энергии - локальных плотность электронных состояний недалеко от Уровень Ферми.[109][110] Из-за большого расстояния оба электрода должны быть чрезвычайно стабильными; только тогда можно наблюдать периодичности, соответствующие отдельным атомам. Сам по себе метод не является химически специфичным и не может идентифицировать атомные частицы, присутствующие на поверхности.
Атомы легко определить по их массе. Если атом ионизированный удаляя один из своих электронов, его траектория, когда он проходит через магнитное поле будет гнуться. Радиус, на который магнитное поле поворачивает траекторию движущегося иона, определяется массой атома. В масс-спектрометр использует этот принцип для измерения отношение массы к заряду ионов. Если образец содержит несколько изотопов, масс-спектрометр может определить долю каждого изотопа в образце путем измерения интенсивности различных пучков ионов. Методы испарения атомов включают: атомно-эмиссионная спектроскопия с индуктивно связанной плазмой и масс-спектрометрия с индуктивно связанной плазмой, оба из которых используют плазму для испарения образцов для анализа.[111]
В атомно-зондовый томограф имеет субнанометровое разрешение в трехмерном пространстве и может химически идентифицировать отдельные атомы с помощью времяпролетной масс-спектрометрии.[112]
Методы электронной эмиссии, такие как Рентгеновская фотоэлектронная спектроскопия (XPS) и Оже-электронная спектроскопия (AES), которые измеряют энергии связи основные электроны, используются для неразрушающего определения атомных частиц, присутствующих в образце. При правильной фокусировке и то, и другое можно сделать для конкретной области. Другой такой метод - спектроскопия потерь энергии электронов (EELS), который измеряет потери энергии электронный луч в пределах просвечивающий электронный микроскоп когда он взаимодействует с частью образца.
Спектры возбужденные состояния может быть использован для анализа атомного состава далеких звезды. Специфический свет длины волн содержащийся в наблюдаемом свете звезд может быть отделен и связан с квантованными переходами в свободных атомах газа. Эти цвета можно воспроизвести с помощью газоразрядная лампа содержащий тот же элемент.[113] Гелий был обнаружен таким образом в спектре Солнца за 23 года до того, как был обнаружен на Земле.[114]
Происхождение и текущее состояние
Барионная материя составляет около 4% от общей плотности энергии наблюдаемая Вселенная, со средней плотностью около 0,25 частиц / м3 (по большей части протоны и электроны).[115] Внутри галактики, такой как Млечный Путь, частицы имеют гораздо более высокую концентрацию, с плотностью вещества в межзвездная среда (ISM) от 105 до 109 атомов / м3.[116] Считается, что Солнце находится внутри Местный пузырь, поэтому плотность в окрестности Солнца составляет всего около 103 атомов / м3.[117] Звезды образуются из плотных облаков в ISM, и эволюционные процессы звезд приводят к постоянному обогащению ISM элементами более массивными, чем водород и гелий.
До 95% барионной материи Млечного Пути сосредоточено внутри звезд, где условия неблагоприятны для атомной материи. Полная барионная масса составляет около 10% массы галактики;[118] остаток массы неизвестен темная материя.[119] Высоко температура внутри звезд делает большинство "атомов" полностью ионизированными, то есть разделяет все электроны из ядер. В звездные остатки - за исключением их поверхностных слоев - огромная давление сделать электронные оболочки невозможными.
Формирование
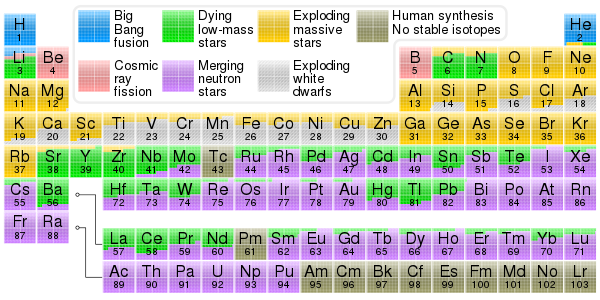
Считается, что электроны существуют во Вселенной с ранних стадий ее существования. Большой взрыв. Атомные ядра образуются в нуклеосинтез реакции. Примерно через три минуты Нуклеосинтез Большого взрыва произвел большую часть гелий, литий, и дейтерий во Вселенной, и, возможно, некоторые из бериллий и бор.[120][121][122]
Повсеместность и стабильность атомов зависит от их энергия связи, что означает, что атом имеет меньшую энергию, чем несвязанная система ядра и электронов. Где температура намного выше, чем потенциал ионизации, материя существует в виде плазма - газ положительно заряженных ионов (возможно, голых ядер) и электронов. Когда температура падает ниже потенциала ионизации, атомы становятся статистически благоприятный. Атомы (вместе со связанными электронами) стали преобладать над заряжен частицы 380 000 лет после Большого взрыва - эпохи, называемой рекомбинация, когда расширяющаяся Вселенная остыла достаточно, чтобы позволить электронам присоединиться к ядрам.[123]
После Большого взрыва, в результате которого не было углерод или же более тяжелые элементы, атомные ядра были объединены в звезды через процесс термоядерная реакция производить больше элемента гелий, и (через тройной альфа-процесс ) последовательность элементов от углерода до утюг;[124] видеть звездный нуклеосинтез для подробностей.
Изотопы, такие как литий-6, а также некоторые бериллий и бор, образуются в космосе через расщепление космических лучей.[125] Это происходит, когда протон высокой энергии ударяется о ядро атома, в результате чего выбрасывается большое количество нуклонов.
Элементы тяжелее железа производились в сверхновые и столкновение нейтронные звезды сквозь r-процесс, И в Звезды AGB сквозь s-процесс, оба из которых связаны с захватом нейтронов атомными ядрами.[126] Такие элементы, как вести образовались в основном в результате радиоактивного распада более тяжелых элементов.[127]
земной шар
Большинство атомов, составляющих земной шар и его жители в своем нынешнем виде присутствовали в туманность это рухнуло из молекулярное облако сформировать Солнечная система. Остальные являются результатом радиоактивного распада, и их относительное соотношение можно использовать для определения возраст Земли через радиометрическое датирование.[128][129] Большинство из гелий в коре Земли (около 99% гелия из газовых скважин, о чем свидетельствует его меньшее содержание гелий-3 ) является продуктом альфа-распад.[130]
На Земле есть несколько следов атомов, которых не было вначале (то есть не «изначальные»), и они не являются результатом радиоактивного распада. Углерод-14 постоянно генерируется космическими лучами в атмосфере.[131] Некоторые атомы на Земле были созданы искусственно либо намеренно, либо как побочные продукты ядерных реакторов или взрывов.[132][133] Из трансурановые элементы - только те, у которых атомные номера больше 92 плутоний и нептуний происходят естественным образом на Земле.[134][135] Радиоактивные периоды жизни трансурановых элементов короче нынешнего возраста Земли[136] и, таким образом, идентифицируемые количества этих элементов давно распались, за исключением следов плутоний-244 возможно, осажденный космической пылью.[128] Природные месторождения плутония и нептуния производятся захват нейтронов в урановой руде.[137]
Земля содержит примерно 1.33×1050 атомы.[138] Хотя небольшое количество независимых атомов благородные газы существуют, такие как аргон, неон, и гелий, 99% атмосфера связан в виде молекул, в том числе углекислый газ и двухатомный кислород и азот. На поверхности Земли подавляющее большинство атомов объединяются, образуя различные соединения, в том числе воды, соль, силикаты и оксиды. Атомы также могут объединяться для создания материалов, которые не состоят из дискретных молекул, в том числе кристаллы и жидкие или твердые металлы.[139][140] Эта атомная материя образует сетевые структуры, в которых отсутствует особый тип мелкомасштабного прерывистого порядка, связанный с молекулярной материей.[141]
Редкие и теоретические формы
Сверхтяжелые элементы
Все нуклиды с атомными номерами выше 82 (вести ) известны как радиоактивные. Нет нуклидов с атомным номером более 92 (уран ) существует на Земле как первичный нуклид, а более тяжелые элементы обычно имеют более короткий период полураспада. Тем не менее, "остров стабильности "охватывающие относительно долгоживущие изотопы сверхтяжелых элементов[142] с атомными номерами 110 к 114 может существовать.[143] Прогнозы периода полураспада самого стабильного нуклида на острове варьируются от нескольких минут до миллионов лет.[144] В любом случае сверхтяжелые элементы (с Z > 104) не существовало бы из-за увеличения Кулон отталкивание (что приводит к спонтанное деление со все более короткими периодами полураспада) в отсутствие каких-либо стабилизирующих эффектов.[145]
Экзотическая материя
Каждой частице материи соответствует антивещество частица с противоположным электрическим зарядом. Таким образом позитрон положительно заряженный антиэлектрон и антипротон отрицательно заряженный эквивалент протон. Когда материя и соответствующая частица антивещества встречаются, они аннигилируют друг друга. Из-за этого, наряду с дисбалансом между количеством частиц материи и антивещества, последние редки во Вселенной. Первые причины этого дисбаланса еще полностью не изучены, хотя теории бариогенез может предложить объяснение. В результате в природе не обнаружено никаких атомов антивещества.[146][147] В 1996 году аналог атома водорода из антивещества (антиводород ) был синтезирован на ЦЕРН лаборатория в Женева.[148][149]
Другой экзотические атомы были созданы путем замены одного из протонов, нейтронов или электронов другими частицами с таким же зарядом. Например, электрон можно заменить на более массивный мюон, образуя мюонный атом. Эти типы атомов можно использовать для проверки фундаментальных предсказаний физики.[150][151][152]
Смотрите также
Примечания
- ^ Для более свежих обновлений см. Брукхейвенская национальная лаборатория с Интерактивная карта нуклидов ] В архиве 25 июля 2020 в Wayback Machine.
- ^ Карат - это 200 миллиграммов. По определению, углерод-12 имеет 0,012 кг на моль. В Константа Авогадро определяет 6×1023 атомов на моль.
- ^ Формула оксида железа (II) записывается здесь как Fe2О2 а не более традиционный FeO, потому что это лучше иллюстрирует объяснение.
Рекомендации
- ^ Пуллман, Бернард (1998). Атом в истории человеческой мысли. Оксфорд, Англия: Издательство Оксфордского университета. С. 31–33. ISBN 978-0-19-515040-7.
- ^ Мельсен (1952). От атомоса к атому, стр. 18-19
- ^ Дальтон (1817 г.). Новая система химической философии т. 2, стр. 36
- ^ Мельсен (1952). От атомоса к атому, п. 137
- ^ Дальтон (1817 г.). Новая система химической философии т. 2. С. 28.
- ^ Миллингтон (1906). Джон Далтон, п. 113
- ^ Дальтон (1808 г.). Новая система химической философии т. 1. С. 316-319.
- ^ Холброу и др. (2010). Современная вводная физика, стр. 65-66
- ^ Эйнштейн, Альберт (1905). "Über die von der molkularkinetischen Theorie der Wärme geforderte Bewegung von in ruhenden Flüssigkeiten Suspendierten Teilchen" (PDF). Annalen der Physik (на немецком). 322 (8): 549–560. Bibcode:1905AnP ... 322..549E. Дои:10.1002 / andp.19053220806. В архиве (PDF) из оригинала 18 июля 2007 г.
- ^ Мазо, Роберт М. (2002). Броуновское движение: колебания, динамика и приложения. Издательство Оксфордского университета. стр.1 –7. ISBN 978-0-19-851567-8. OCLC 48753074.
- ^ Lee, Y.K .; Хун, К. (1995). "Броуновское движение". Имперский колледж. Архивировано из оригинал 18 декабря 2007 г.
- ^ Паттерсон, Г. (2007). «Жан Перрен и торжество атомной доктрины». Стараться. 31 (2): 50–53. Дои:10.1016 / j.endeavour.2007.05.003. PMID 17602746.
- ^ Томсон, Дж. Дж. (Август 1901 г.). «На телах меньше атомов». Ежемесячный журнал Popular Science: 323–335. Получено 21 июн 2009.
- ^ Наварро (2012). История электрона, п. 94
- ^ а б Хейльброн (2003). Эрнест Рутфорд и взрыв атома, стр. 64-68
- ^ "Фредерик Содди, Нобелевская премия по химии 1921 г.". Нобелевский фонд. В архиве из оригинала от 9 апреля 2008 г.. Получено 18 января 2008.
- ^ Томсон, Джозеф Джон (1913). «Лучи положительного электричества». Труды Королевского общества. А. 89 (607): 1–20. Bibcode:1913RSPSA..89 .... 1Т. Дои:10.1098 / rspa.1913.0057. В архиве из оригинала от 4 ноября 2016 г.
- ^ Стерн, Дэвид П. (16 мая 2005 г.). «Атомное ядро и ранняя модель атома Бора». НАСА /Центр космических полетов Годдарда. В архиве с оригинала от 20 августа 2007 г.
- ^ Бор, Нильс (11 декабря 1922 г.). "Нильс Бор, Нобелевская премия по физике 1922 г., Нобелевская лекция". Нобелевский фонд. В архиве из оригинала 15 апреля 2008 г.
- ^ а б c Паис, Авраам (1986). Внутренняя связь: материи и сил в физическом мире. Нью-Йорк: Издательство Оксфордского университета. стр.228–230. ISBN 978-0-19-851971-3.
- ^ Льюис, Гилберт Н. (1916). «Атом и молекула». Журнал Американского химического общества. 38 (4): 762–786. Дои:10.1021 / ja02261a002. В архиве (PDF) с оригинала 25 августа 2019 г.
- ^ Шерри, Эрик Р. (2007). Периодическая таблица Менделеева: ее история и ее значение. Oxford University Press, США. стр.205–226. ISBN 978-0-19-530573-9.
- ^ Ленгмюр, Ирвинг (1919). «Расположение электронов в атомах и молекулах». Журнал Американского химического общества. 41 (6): 868–934. Дои:10.1021 / ja02227a002. В архиве с оригинала 21 июня 2019 г.
- ^ Скалли, Марлан О .; Lamb, Willis E .; Барут, Асим (1987). «К теории аппарата Штерна-Герлаха». Основы физики. 17 (6): 575–583. Bibcode:1987ФоФ ... 17..575С. Дои:10.1007 / BF01882788. S2CID 122529426.
- ^ McEvoy, J. P .; Зарате, Оскар (2004). Введение в квантовую теорию. Тотемные книги. С. 110–114. ISBN 978-1-84046-577-8.
- ^ Козловский, Мирослав (2019). "Уравнение Шредингера История".
- ^ Чад Орзел (16 сентября 2014 г.). "Что такое принцип неопределенности Гейзенберга?". TED-Ed. В архиве из оригинала 13 сентября 2015 г. - через YouTube.
- ^ Браун, Кевин (2007). «Атом водорода». MathPages. В архиве из оригинала 13 мая 2008 г.
- ^ Харрисон, Дэвид М. (2000). «Развитие квантовой механики». Университет Торонто. В архиве из оригинала от 25 декабря 2007 г.
- ^ Астон, Фрэнсис В. (1920). «Строение атмосферного неона». Философский журнал. 39 (6): 449–455. Дои:10.1080/14786440408636058.
- ^ Чедвик, Джеймс (12 декабря 1935 г.). «Нобелевская лекция: нейтрон и его свойства». Нобелевский фонд. В архиве из оригинала 12 октября 2007 г.
- ^ Боуден, Мэри Эллен (1997). "Отто Хан, Лиз Мейтнер и Фриц Штрассманн". Успешные в химии: человеческое лицо химических наук. Филадельфия, Пенсильвания: Фонд химического наследия. стр.76–80, 125. ISBN 978-0-941901-12-3.
- ^ "Отто Хан, Лиз Мейтнер и Фриц Штрассманн". Институт истории науки. Июнь 2016 г. В архиве из оригинала 21 марта 2018 г.
- ^ Мейтнер, Лиза; Фриш, Отто Роберт (1939). «Распад урана нейтронами: новый тип ядерной реакции». Природа. 143 (3615): 239–240. Bibcode:1939Натура.143..239М. Дои:10.1038 / 143239a0. S2CID 4113262.
- ^ Шредер, М. "Lise Meitner - Zur 125. Wiederkehr Ihres Geburtstages" (на немецком). Архивировано из оригинал 19 июля 2011 г.. Получено 4 июн 2009.
- ^ Crawford, E .; Сайм, Рут Левин; Уокер, Марк (1997). «Нобелевский рассказ о послевоенной несправедливости». Физика сегодня. 50 (9): 26–32. Bibcode:1997ФТ .... 50i..26С. Дои:10.1063/1.881933.
- ^ Кулландер, Свен (28 августа 2001 г.). «Акселераторы и лауреаты Нобелевской премии». Нобелевский фонд. В архиве из оригинала от 13 апреля 2008 г.
- ^ «Нобелевская премия по физике 1990 г.». Нобелевский фонд. 17 октября 1990 г. В архиве из оригинала 14 мая 2008 г.
- ^ Демтредер, Вольфганг (2002). Атомы, молекулы и фотоны: введение в атомную, молекулярную и квантовую физику (1-е изд.). Springer. стр.39 –42. ISBN 978-3-540-20631-6. OCLC 181435713.
- ^ Воан, Грэм (2000). Кембриджский справочник по физике. Издательство Кембриджского университета. п.8. ISBN 978-0-521-57507-2. OCLC 224032426.
- ^ Mohr, P.J .; Тейлор, Б. и Ньюэлл, Д. (2014), «Рекомендуемые значения фундаментальных физических констант, рекомендованные CODATA за 2014 г.» В архиве 21 февраля 2012 в WebCite (Веб-версия 7.0). База данных была разработана Дж. Бейкером, М. Дума и С. Коточиговой. (2014). Национальный институт стандартов и технологий, Гейтерсбург, Мэриленд 20899.
- ^ МакГрегор, Малкольм Х. (1992). Загадочный электрон. Издательство Оксфордского университета. стр.33–37. ISBN 978-0-19-521833-6. OCLC 223372888.
- ^ а б Группа данных по частицам (2002). "Приключение частиц". Лаборатория Лоуренса Беркли. В архиве из оригинала от 4 января 2007 г.
- ^ а б Шомберт, Джеймс (18 апреля 2006 г.). «Элементарные частицы». Университет Орегона. В архиве из оригинала от 21 августа 2011 г.
- ^ Евремович, Татьяна (2005). Ядерные принципы в инженерии. Springer. п.63. ISBN 978-0-387-23284-3. OCLC 228384008.
- ^ Пфеффер, Джереми I .; Нир, Шломо (2000). Современная физика: вводный текст. Imperial College Press. С. 330–336. ISBN 978-1-86094-250-1. OCLC 45900880.
- ^ Веннер, Дженнифер М. (10 октября 2007 г.). "Как работает радиоактивный распад?". Карлтон-колледж. В архиве из оригинала от 11 мая 2008 г.
- ^ а б c Раймонд, Дэвид (7 апреля 2006 г.). «Ядерная энергия связи». Нью-Мексико. Архивировано из оригинал 1 декабря 2002 г.
- ^ Михос, Крис (23 июля 2002 г.). «Преодоление кулоновского барьера». Кейс Вестерн Резервный университет. В архиве из оригинала 12 сентября 2006 г.
- ^ Персонал (30 марта 2007 г.). "Азбука ядерной науки". Национальная лаборатория Лоуренса Беркли. В архиве из оригинала от 5 декабря 2006 г.
- ^ Махиджани, Арджун; Салеска, Скотт (2 марта 2001 г.). «Основы ядерной физики и деления». Институт энергетики и экологических исследований. В архиве из оригинала от 16 января 2007 г.
- ^ Шултис, Дж. Кеннет; Фау, Ричард Э. (2002). Основы ядерной науки и техники. CRC Press. С. 10–17. ISBN 978-0-8247-0834-4. OCLC 123346507.
- ^ Фьюэлл, М. (1995). «Атомный нуклид с самой высокой средней энергией связи». Американский журнал физики. 63 (7): 653–658. Bibcode:1995AmJPh..63..653F. Дои:10.1119/1.17828.
- ^ Малликен, Роберт С. (1967). «Спектроскопия, молекулярные орбитали и химическая связь». Наука. 157 (3784): 13–24. Bibcode:1967Научный ... 157 ... 13М. Дои:10.1126 / science.157.3784.13. PMID 5338306.
- ^ а б Brucat, Филип Дж. (2008). «Квантовый атом». Университет Флориды. Архивировано из оригинал 7 декабря 2006 г.
- ^ Манти, Дэвид (2001). «Атомные орбитали». Орбитальная центральная. В архиве из оригинала 10 января 2008 г.
- ^ Гертер, Терри (2006). «Лекция 8: Атом водорода». Корнелл Университет. Архивировано из оригинал 22 февраля 2012 г.
- ^ Bell, R.E .; Эллиотт, Л. (1950). «Гамма-лучи реакции H1(n, γ) D2 и связывающая энергия Дейтрона ». Физический обзор. 79 (2): 282–285. Bibcode:1950PhRv ... 79..282B. Дои:10.1103 / PhysRev.79.282.
- ^ Смирнов, Борис М. (2003). Физика атомов и ионов. Springer. стр.249 –272. ISBN 978-0-387-95550-6.
- ^ Матис, Ховард С. (9 августа 2000 г.). «Изотопы водорода». Путеводитель по ядерной настенной диаграмме. Национальная лаборатория Лоуренса Беркли. В архиве из оригинала 18 декабря 2007 г.
- ^ Вайс, Рик (17 октября 2006 г.). «Ученые объявляют о создании самого тяжелого атомного элемента». Вашингтон Пост. В архиве из оригинала от 21 августа 2011 г.
- ^ а б Подоконники, Алан Д. (2003). Науки о Земле - легкий путь. Образовательная серия Бэррона. стр.131–134. ISBN 978-0-7641-2146-3. OCLC 51543743.
- ^ Дюме, Бель (23 апреля 2003 г.). «Висмут побил рекорд периода полураспада для альфа-распада». Мир физики. В архиве из оригинала 14 декабря 2007 г.
- ^ Линдси, Дон (30 июля 2000 г.). «Радиоактивные вещества, пропавшие с Земли». Архив Дона Линдси. В архиве из оригинала от 28 апреля 2007 г.
- ^ Тули, Джагдиш К. (апрель 2005 г.). «Карты ядерного кошелька». Национальный центр ядерных данных, Брукхейвенская национальная лаборатория. В архиве из оригинала от 3 октября 2011 г.
- ^ Справочник CRC (2002).
- ^ Крейн, К. (1988). Введение в ядерную физику. Джон Уайли и сыновья. стр.68. ISBN 978-0-471-85914-7.
- ^ а б Миллс, Ян; Цвиташ, Томислав; Хоманн, Клаус; Каллай, Никола; Кучицу, Козо (1993). Величины, единицы и символы в физической химии (2-е изд.). Оксфорд: Международный союз теоретической и прикладной химии, Комиссия по терминологии и единицам физиохимических символов, Blackwell Scientific Publications. п.70. ISBN 978-0-632-03583-0. OCLC 27011505.
- ^ Чие, Чанг (22 января 2001 г.). «Нуклидная стабильность». Университет Ватерлоо. Архивировано из оригинал 30 августа 2007 г.
- ^ «Атомный вес и изотопный состав для всех элементов». Национальный институт стандартов и технологий. В архиве с оригинала 31 декабря 2006 г.. Получено 4 января 2007.
- ^ Audi, G .; Wapstra, A.H .; Тибо, К. (2003). "Оценка атомной массы Ame2003 (II)" (PDF). Ядерная физика A. 729 (1): 337–676. Bibcode:2003НуФА.729..337А. Дои:10.1016 / j.nuclphysa.2003.11.003. В архиве (PDF) из оригинала 16 октября 2005 г.
- ^ Гош, округ Колумбия; Бисвас, Р. (2002). «Теоретический расчет абсолютных радиусов атомов и ионов. Часть 1. Атомные радиусы». Int. J. Mol. Наука. 3 (11): 87–113. Дои:10.3390 / i3020087.
- ^ Шеннон, Р. Д. (1976). «Пересмотренные эффективные ионные радиусы и систематические исследования межатомных расстояний в галогенидах и халькогенидах» (PDF). Acta Crystallographica A. 32 (5): 751–767. Bibcode:1976AcCrA..32..751S. Дои:10.1107 / S0567739476001551.
- ^ Донг, Джуди (1998). «Диаметр атома». Сборник фактов по физике. В архиве из оригинала от 4 ноября 2007 г.
- ^ Зумдал, Стивен С. (2002). Вводная химия: основа (5-е изд.). Хоутон Миффлин. ISBN 978-0-618-34342-3. OCLC 173081482. В архиве из оригинала от 4 марта 2008 г.
- ^ Бете, Ганс (1929). "Termaufspaltung in Kristallen". Annalen der Physik. 3 (2): 133–208. Bibcode:1929АнП ... 395..133Б. Дои:10.1002 / andp.19293950202.
- ^ Биркхольц, Марио (1995). «Диполи, индуцированные кристаллическим полем в гетерополярных кристаллах - I. Концепция». Z. Phys. B. 96 (3): 325–332. Bibcode:1995ZPhyB..96..325B. CiteSeerX 10.1.1.424.5632. Дои:10.1007 / BF01313054. S2CID 122527743.
- ^ Birkholz, M .; Рудерт, Р. (2008). «Межатомные расстояния в дисульфидах со структурой пирита - случай эллипсоидального моделирования ионов серы». Физика Статус Solidi B. 245 (9): 1858–1864. Bibcode:2008ПССБР.245.1858Б. Дои:10.1002 / pssb.200879532.
- ^ Биркхольц, М. (2014). «Моделирование формы ионов в кристаллах типа пирита». Кристаллы. 4 (3): 390–403. Дои:10,3390 / крист 4030390.
- ^ Персонал (2007). "Маленькие чудеса: использование нанотехнологий". Государственный университет Орегона. В архиве из оригинала 21 мая 2011 г. - описывает ширину человеческого волоса как 105 нм и 10 атомов углерода при длине волны 1 нм.
- ^ Падилла, Майкл Дж .; Миаулис, Иоаннис; Сир, Марта (2002). Исследователь науки Прентис Холл: химические строительные блоки. Река Аппер Сэдл, Нью-Джерси: Prentice-Hall, Inc. стр. 32. ISBN 978-0-13-054091-1. OCLC 47925884.
В одной капле воды 2 000 000 000 000 000 000 000 (это 2 секстиллиона) атомов кислорода - и вдвое больше атомов водорода.
- ^ Фейнман, Ричард (1995). Шесть легких пьес. Группа пингвинов. п. 5. ISBN 978-0-14-027666-4. OCLC 40499574.
- ^ а б «Радиоактивность». Splung.com. В архиве из оригинала от 4 декабря 2007 г.. Получено 19 декабря 2007.
- ^ L'Annunziata, Майкл Ф. (2003). Справочник по радиоактивному анализу. Академическая пресса. стр.3 –56. ISBN 978-0-12-436603-9. OCLC 16212955.
- ^ Файерстоун, Ричард Б. (22 мая 2000 г.). «Режимы радиоактивного распада». Лаборатория Беркли. Архивировано из оригинал 29 сентября 2006 г.
- ^ Хорнак, Дж. П. (2006). «Глава 3: Физика спина». Основы ЯМР. Рочестерский технологический институт. В архиве из оригинала от 3 февраля 2007 г.
- ^ а б Шредер, Пол А. (25 февраля 2000 г.). «Магнитные свойства». Университет Джорджии. Архивировано из оригинал 29 апреля 2007 г.
- ^ Гебель, Грег (1 сентября 2007 г.). «[4.3] Магнитные свойства атома». Элементарная квантовая физика. На веб-сайте общественного достояния. Архивировано из оригинал 29 июня 2011 г.
- ^ Яррис, Линн (весна 1997 г.). "Говорящие картинки". Обзор исследований лаборатории Беркли. В архиве из оригинала от 13 января 2008 г.
- ^ Liang, Z.-P .; Хааке, Э.М. (1999). Вебстер, Дж. (ред.). Энциклопедия электротехники и электроники: магнитно-резонансная томография. т. 2. Джон Уайли и сыновья. С. 412–426. ISBN 978-0-471-13946-1.
- ^ Зегбрук, Барт Дж. Ван (1998). «Уровни энергии». Шиппенсбургский университет. Архивировано из оригинал 15 января 2005 г.
- ^ Фаулз, Грант Р. (1989). Введение в современную оптику. Courier Dover Publications. стр.227 –233. ISBN 978-0-486-65957-2. OCLC 18834711.
- ^ Martin, W.C .; Визе, W.L. (Май 2007 г.). «Атомная спектроскопия: сборник основных идей, обозначений, данных и формул». Национальный институт стандартов и технологий. В архиве из оригинала от 8 февраля 2007 г.
- ^ «Спектры излучения атомов - происхождение спектральных линий». Веб-сайт Авогадро. Архивировано из оригинал 28 февраля 2006 г.. Получено 10 августа 2006.
- ^ Фитцпатрик, Ричард (16 февраля 2007 г.). «Тонкая структура». Техасский университет в Остине. В архиве из оригинала от 21 августа 2011 г.
- ^ Вайс, Майкл (2001). "Эффект Зеемана". Калифорнийский университет в Риверсайде. В архиве из оригинала от 2 февраля 2008 г.
- ^ Beyer, H.F .; Шевелько, В. (2003). Введение в физику высокозарядных ионов. CRC Press. С. 232–236. ISBN 978-0-7503-0481-8. OCLC 47150433.
- ^ Уоткинс, Тайер. «Когерентность в вынужденной эмиссии». Государственный университет Сан-Хосе. В архиве из оригинала 12 января 2008 г.. Получено 23 декабря 2007.
- ^ ИЮПАК, Сборник химической терминологии, 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) "валентность ". Дои:10.1351 / goldbook.V06588
- ^ Ройш, Уильям (16 июля 2007 г.). «Виртуальный учебник органической химии». Университет штата Мичиган. Архивировано из оригинал 29 октября 2007 г.
- ^ «Ковалентная связь - Одинарные связи». химгид. 2000 г. В архиве из оригинала от 1 ноября 2008 г.
- ^ Хастед, Роберт; и другие. (11 декабря 2003 г.). «Периодическая таблица элементов». Лос-Аламосская национальная лаборатория. В архиве из оригинала 10 января 2008 г.
- ^ Баум, Руди (2003). "Элементаль: Периодическая таблица". Новости химии и машиностроения. В архиве из оригинала от 21 августа 2011 г.
- ^ Гудштейн, Дэвид Л. (2002). Состояния вещества. Courier Dover Publications. стр.436 –438. ISBN 978-0-13-843557-8.
- ^ Бражкин, Вадим В. (2006). «Метастабильные фазы, фазовые превращения и фазовые диаграммы в физике и химии». Успехи физики. 49 (7): 719–724. Bibcode:2006PhyU ... 49..719B. Дои:10.1070 / PU2006v049n07ABEH006013.
- ^ Майерс, Ричард (2003). Основы химии. Гринвуд Пресс. п.85. ISBN 978-0-313-31664-7. OCLC 50164580.
- ^ Персонал (9 октября 2001 г.). «Конденсат Бозе-Эйнштейна: новая форма вещества». Национальный институт стандартов и технологий. В архиве из оригинала от 3 января 2008 г.
- ^ Колтон, Имоджен; Файф, Жанетт (3 февраля 1999 г.). «Суператомы от конденсации Бозе-Эйнштейна». Мельбурнский университет. Архивировано из оригинал 29 августа 2007 г.
- ^ Джейкокс, Мэрилин; Гадзук, Дж. Уильям (ноябрь 1997 г.). «Сканирующий туннельный микроскоп». Национальный институт стандартов и технологий. В архиве из оригинала от 7 января 2008 г.
- ^ «Нобелевская премия по физике 1986 года». Нобелевский фонд. В архиве из оригинала 17 сентября 2008 г.. Получено 11 января 2008. В частности, см. Нобелевскую лекцию Дж. Биннига и Х. Рорера.
- ^ Якубовский, Н .; Моэнс, Люк; Vanhaecke, Франк (1998). «Секторные полевые масс-спектрометры в ИСП-МС». Spectrochimica Acta Часть B: Атомная спектроскопия. 53 (13): 1739–1763. Bibcode:1998AcSpe..53.1739J. Дои:10.1016 / S0584-8547 (98) 00222-5.
- ^ Мюллер, Эрвин В.; Паниц, Джон А.; Маклейн, С. Брукс (1968). «Атомно-зондовый полевой ионный микроскоп». Обзор научных инструментов. 39 (1): 83–86. Bibcode:1968RScI ... 39 ... 83М. Дои:10.1063/1.1683116.
- ^ Лохнер, Джим; Гибб, Мередит; Ньюман, Фил (30 апреля 2007 г.). "Что нам говорят Spectra?". НАСА / Центр космических полетов Годдарда. В архиве из оригинала 16 января 2008 г.
- ^ Зима, Марк (2007). «Гелий». WebElements. В архиве с оригинала от 30 декабря 2007 г.
- ^ Хиншоу, Гэри (10 февраля 2006 г.). "Из чего состоит Вселенная?". НАСА / WMAP. В архиве с оригинала 31 декабря 2007 г.
- ^ Чоппин, Грегори Р .; Лильензин, Ян-Олов; Ридберг, Янв (2001). Радиохимия и ядерная химия. Эльзевир. п. 441. ISBN 978-0-7506-7463-8. OCLC 162592180.
- ^ Дэвидсен, Артур Ф. (1993). "Астрономия в дальнем ультрафиолетовом диапазоне на космическом корабле" Астро-1 ". Наука. 259 (5093): 327–334. Bibcode:1993Наука ... 259..327Д. Дои:10.1126 / science.259.5093.327. PMID 17832344. S2CID 28201406.
- ^ Лекё, Джеймс (2005). Межзвездная среда. Springer. п.4. ISBN 978-3-540-21326-0. OCLC 133157789.
- ^ Смит, Найджел (6 января 2000 г.). «Поиски темной материи». Мир физики. В архиве из оригинала 16 февраля 2008 г.
- ^ Кросвелл, Кен (1991). «Бор, неровности и Большой взрыв: была ли материя распределена равномерно, когда Вселенная возникла? Возможно, нет; ключ к разгадке лежит в создании более легких элементов, таких как бор и бериллий». Новый ученый (1794): 42. Архивировано с оригинал 7 февраля 2008 г.
- ^ Копи, Крейг Дж .; Шрамм, Д. Н.; Тернер, MS (1995). «Нуклеосинтез Большого Взрыва и барионная плотность Вселенной». Наука (Представлена рукопись). 267 (5195): 192–199. arXiv:Astro-ph / 9407006. Bibcode:1995 Наука ... 267..192C. Дои:10.1126 / science.7809624. PMID 7809624. S2CID 15613185. В архиве с оригинала 14 августа 2019 г.
- ^ Хиншоу, Гэри (15 декабря 2005 г.). «Испытания Большого взрыва: элементы света». НАСА / WMAP. В архиве из оригинала 17 января 2008 г.
- ^ Эбботт, Брайан (30 мая 2007 г.). "Микроволновое (WMAP) исследование всего неба". Планетарий Хайдена. Архивировано из оригинал 13 февраля 2013 г.
- ^ Хойл, Ф. (1946). «Синтез элементов из водорода». Ежемесячные уведомления Королевского астрономического общества. 106 (5): 343–383. Bibcode:1946МНРАС.106..343Х. Дои:10.1093 / мнрас / 106.5.343.
- ^ Кнаут, округ Колумбия; Кнаут, округ Колумбия; Ламберт, Дэвид Л .; Крейн, П. (2000). «Недавно синтезированный литий в межзвездной среде». Природа. 405 (6787): 656–658. Bibcode:2000Натура.405..656K. Дои:10.1038/35015028. PMID 10864316. S2CID 4397202.
- ^ Машник, Степан Г. (2000). «О процессах нуклеосинтеза и отщепления солнечной системы и космических лучей». arXiv:astro-ph / 0008382.
- ^ Канзасская геологическая служба (4 мая 2005 г.). «Возраст Земли». Канзасский университет. Архивировано из оригинал 5 июля 2008 г.
- ^ а б Мануэль (2001). Происхождение элементов в солнечной системе, стр. 407-430, 511-519
- ^ Далримпл, Дж. Брент (2001). «Возраст Земли в двадцатом веке: проблема (в основном) решенная». Геологическое общество, Лондон, Специальные публикации. 190 (1): 205–221. Bibcode:2001ГСЛСП.190..205Д. Дои:10.1144 / GSL.SP.2001.190.01.14. S2CID 130092094. В архиве из оригинала от 11 ноября 2007 г.
- ^ Андерсон, Дон Л.; Foulger, G.R .; Мейбом, Андерс (2 сентября 2006 г.). «Гелий: фундаментальные модели». MantlePlumes.org. В архиве из оригинала от 8 февраля 2007 г.
- ^ Пенникотт, Кэти (10 мая 2001 г.). «Углеродные часы могут показывать неправильное время». PhysicsWeb. В архиве из оригинала от 15 декабря 2007 г.
- ^ Яррис, Линн (27 июля 2001 г.). «Новые сверхтяжелые элементы 118 и 116, обнаруженные в лаборатории Беркли». Лаборатория Беркли. Архивировано из оригинал 9 января 2008 г.
- ^ Алмаз, H; и другие. (1960). «Изобилие тяжелых изотопов в термоядерном устройстве Майка». Физический обзор. 119 (6): 2000–2004. Bibcode:1960ПхРв..119.2000Д. Дои:10.1103 / PhysRev.119.2000.
- ^ Постон-старший, Джон У. (23 марта 1998 г.). «Встречаются ли когда-либо в природе трансурановые элементы, такие как плутоний?». Scientific American. В архиве из оригинала 27 марта 2015 г.
- ^ Келлер, К. (1973). «Естественное появление лантаноидов, актинидов и сверхтяжелых элементов». Chemiker Zeitung. 97 (10): 522–530. OSTI 4353086.
- ^ Зайдер, Марко; Росси, Харальд Х. (2001). Радиационная наука для врачей и работников общественного здравоохранения. Springer. п.17. ISBN 978-0-306-46403-4. OCLC 44110319.
- ^ "Окло ископаемые реакторы". Кертинский технологический университет. Архивировано из оригинал 18 декабря 2007 г.. Получено 15 января 2008.
- ^ Вайзенбергер, Дрю. "Сколько атомов в мире?". Jefferson Lab. В архиве из оригинала 22 октября 2007 г.. Получено 16 января 2008.
- ^ Пидвирный, Майкл. «Основы физической географии». Университет Британской Колумбии Оканаган. В архиве из оригинала 21 января 2008 г.. Получено 16 января 2008.
- ^ Андерсон, Дон Л. (2002). «Внутреннее внутреннее ядро Земли». Труды Национальной академии наук. 99 (22): 13966–13968. Bibcode:2002PNAS ... 9913966A. Дои:10.1073 / pnas.232565899. ЧВК 137819. PMID 12391308.
- ^ Полинг, Линус (1960). Природа химической связи. Издательство Корнельского университета. С. 5–10. ISBN 978-0-8014-0333-0. OCLC 17518275.
- ^ Аноним (2 октября 2001 г.). «Вторая открытка с острова стабильности». ЦЕРН Курьер. В архиве из оригинала от 3 февраля 2008 г.
- ^ Карпов, А. В .; Загребаев, В. И .; Palenzuela, Y.M .; и другие. (2012). «Распад и устойчивость самых тяжелых элементов» (PDF). Международный журнал современной физики E. 21 (2): 1250013-1–1250013-20. Bibcode:2012IJMPE..2150013K. Дои:10.1142 / S0218301312500139.
- ^ "Подтверждение сверхтяжелого элемента 114: ступенька к острову стабильности". Лаборатория Беркли. 2009.
- ^ Мёллер, П. (2016). «Пределы ядерной карты, установленные делением и альфа-распадом» (PDF). Сеть конференций EPJ. 131: 03002-1–03002-8. Bibcode:2016EPJWC.13103002M. Дои:10.1051 / epjconf / 201613103002.
- ^ Коппес, Стив (1 марта 1999 г.). «Физики Фермилаборатории обнаружили новую асимметрию материи и антивещества». Чикагский университет. В архиве из оригинала от 19 июля 2008 г.
- ^ Кроми, Уильям Дж. (16 августа 2001 г.). «Время жизни в триллионные доли секунды: ученые исследуют антивещество». Вестник Гарвардского университета. В архиве из оригинала от 3 сентября 2006 г.
- ^ Хиджманс, Том В. (2002). «Физика элементарных частиц: холодный антиводород». Природа. 419 (6906): 439–440. Bibcode:2002Натура.419..439H. Дои:10.1038 / 419439a. PMID 12368837.
- ^ Персонал (30 октября 2002 г.). "Исследователи заглянули внутрь" антивещества ". Новости BBC. В архиве из оригинала от 22 февраля 2007 г.
- ^ Барретт, Роджер (1990). «Странный мир экзотического атома». Новый ученый (1728): 77–115. Архивировано из оригинал 21 декабря 2007 г.
- ^ Indelicato, Пол (2004). «Экзотические атомы». Physica Scripta. T112 (1): 20–26. arXiv:физика / 0409058. Bibcode:2004ФСТ..112 ... 20И. Дои:10.1238 / Physica.Topical.112a00020. S2CID 11134265. В архиве из оригинала от 4 ноября 2018 г.
- ^ Рипин, Барретт Х. (июль 1998 г.). «Недавние эксперименты с экзотическими атомами». Американское физическое общество. Архивировано из оригинал 23 июля 2012 г.
Библиография
- Оливер Мануэль (2001). Происхождение элементов в Солнечной системе: последствия наблюдений после 1957 года. Springer. ISBN 978-0-306-46562-8. OCLC 228374906.
- Эндрю Г. ван Мелсен (2004) [1952]. От атомоса к атому: история концепции атома. Перевод Генри Дж. Корена. Dover Publications. ISBN 0-486-49584-1.
- Дж. П. Миллингтон (1906). Джон Далтон. J. M. Dent & Co. (Лондон); Э. П. Даттон и Ко (Нью-Йорк).
- Чарльз Х. Холброу; Джеймс Н. Ллойд; Джозеф С. Амато; Энрике Гальвес; М. Элизабет Паркс (2010). Современная вводная физика. Springer Science & Business Media. ISBN 9780387790794.
- Джон Далтон (1808). Новая система химической философии об. 1.
- Джон Далтон (1817 г.). Новая система химической философии об. 2.
- Джон Л. Хейлброн (2003). Эрнест Резерфорд и взрыв атома. Oxford University Press. ISBN 0-19-512378-6.
- Жауме Наварро (2012). История электрона: Дж. Дж. И Дж. П. Томсон. Издательство Кембриджского университета. ISBN 9781107005228.
дальнейшее чтение
- Гангопадхьяя, Мриналканти (1981). Индийский атомизм: история и источники. Атлантическое нагорье, Нью-Джерси: Humanities Press. ISBN 978-0-391-02177-8. OCLC 10916778.
- Янноне, А. Пабло (2001). Словарь мировой философии. Рутледж. ISBN 978-0-415-17995-9. OCLC 44541769.
- Кинг, Ричард (1999). Индийская философия: введение в индуистскую и буддийскую мысль. Издательство Эдинбургского университета. ISBN 978-0-7486-0954-3.
- МакЭвилли, Томас (2002). Форма древней мысли: сравнительные исследования греческой и индийской философий. Allworth Press. ISBN 978-1-58115-203-6.
- Зигфрид, Роберт (2002). От элементов к атомам: история химического состава. ДИАНА. ISBN 978-0-87169-924-4. OCLC 186607849.
- Терези, Дик (2003). Утраченные открытия: древние корни современной науки. Саймон и Шустер. С. 213–214. ISBN 978-0-7432-4379-7.
- Вюрц, Чарльз Адольф (1881). Атомная теория. Нью-Йорк: Д. Эпплтон и компания. ISBN 978-0-559-43636-9.
внешняя ссылка
- Шарп, Тим (8 августа 2017 г.). "Что такое Атом?". Живая наука.
- "Автостопом по Вселенной, атомам и строению атома". h2g2. BBC. 3 января 2006 г.

![{displaystyle 1.07 {sqrt [{3}] {A}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a74a6ca6998768195969eef75ca046e8431c29d3)



