Аритмогенная кардиомиопатия - Arrhythmogenic cardiomyopathy
Эта статья нужны дополнительные цитаты для проверка. (Февраль 2009 г.) (Узнайте, как и когда удалить этот шаблон сообщения) |
| Аритмогенная кардиомиопатия | |
|---|---|
| Другие имена | аритмогенная кардиомиопатия правого желудочка (ARVC), аритмогенная дисплазия / кардиомиопатия правого желудочка (ARVD / C), дисплазия правого желудочка |
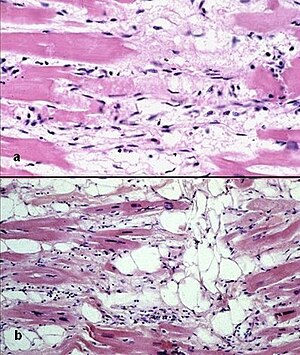 | |
| Микрофотография сердца ACM. | |
| Специальность | Кардиология |
Аритмогенная кардиомиопатия (ACM), аритмогенная дисплазия правого желудочка (АРВД), или же аритмогенная кардиомиопатия правого желудочка (ARVC), является унаследованным сердечное заболевание.[1]
ACM вызвано генетические дефекты частей сердечная мышца (также называемый миокард или же сердечная мышца) известный как десмосомы, области на поверхности клеток сердечной мышцы, которые связывают клетки вместе. Десмосомы состоят из нескольких белки, и многие из этих белков могут иметь вредные мутации.
Заболевание является разновидностью неишемический кардиомиопатия это в первую очередь касается Правый желудочек, хотя сообщалось о случаях заболевания исключительно левого желудочка. Он характеризуется гипокинетический области, затрагивающие свободную стенку желудочка, с замещением миокарда фибро-жиром, с ассоциированными аритмии часто берут начало в правом желудочке. Номенклатура АРВД в настоящее время считается неуместной и вводящей в заблуждение, поскольку АКМ не включает дисплазию стенки желудочка. Случаи ACM, происходящие из левого желудочка, привели к отказу от названия ARVC.
ACM можно найти вместе с диффузная ладонно-подошвенная кератодермия, и шерстяные волосы, при аутосомно-рецессивном состоянии, называемом Болезнь Наксоса, потому что эта генетическая аномалия также может повлиять на целостность поверхностных слоев кожи, наиболее подверженных давлению.[2]:513[3]
АКМ является важной причиной желудочковых аритмий у детей и молодых людей. Это наблюдается преимущественно у мужчин, и 30–50% случаев имеют семейное распространение.
Признаки и симптомы
Те, кто страдает аритмогенной кардиомиопатией, могут вообще не иметь никаких симптомов, несмотря на значительные отклонения в структуре сердца.[4] Если симптомы действительно возникают, первоначальное проявление часто связано с нарушением сердечного ритма (аритмией), которые при аритмогенной кардиомиопатии могут принимать форму сердцебиения или затемнения.[5] Внезапная смерть может быть первым проявлением АКМ без каких-либо предшествующих симптомов.[4] Эти симптомы часто возникают во время юность и в раннем взрослом возрасте, но признаки АКМ могут редко обнаруживаться у младенцев.
По мере прогрессирования ACM мышечная ткань в желудочках может расширяться и ослабевать. Обычно сначала ослабевает правый желудочек, что приводит к усталости и отеку лодыжек. На более поздних стадиях заболевания, при котором поражаются оба желудочка, может развиться одышка, особенно в положении лежа.[4]
Первые клинические признаки АКМ обычно возникают во время юность и ранняя взрослость. Однако у младенцев признаки АКМ проявляются редко.
Генетика
ACM обычно передается по наследству аутосомно-доминантный шаблон с переменным выражением. Только от 30% до 50% людей, затронутых ACM, будут иметь положительный результат теста на одну из известных генетических мутаций в хромосомный места связанные с заболеванием.[6][7] Новые исследования показали, что мутации (точечные мутации) в генах, кодирующих десмосомные белки (см. вставной диск ) являются основными возбудителями развития этого заболевания. Недавно было показано, что мутации в десмин Ген DES мог вызвать ACM.[8] Десмин представляет собой белок промежуточного филамента, который связан с десмосомы. Разные DES мутации вызывают аномальную агрегацию десмина и связанных белков.[9] В пенетрантность составляет 20–35% в целом, но значительно выше в Италии. В ACM вовлечены семь локусов генов. Неясно, изменяется ли патогенез в зависимости от различных вовлеченных локусов. Стандартные генетические скрининговые тесты в настоящее время тестируются и оцениваются в различных современных сердечно-сосудистых исследовательских центрах и больницах. Типы включают:
| Тип | OMIM | Ген | Locus | Ссылка |
|---|---|---|---|---|
| ARVD1lpl | 107970 | TGFB3 | 14q23-q24 | [10] |
| ARVD2 | 600996 | RYR2 | 1q42-q43 | [11] |
| ARVD3 | 602086 | ? | 14q12-q22 | |
| ARVD4 | 602087 | ? | 2q32.1-q32.3 | |
| ARVD5 | 604400 | TMEM43 | 3п23 | [12][13] |
| ARVD6 | 604401 | ? | 10п14-п12 | |
| ARVD7 | 609160 | DES | 10q22.3 | [14][15] |
| ARVD8 | 607450 | DSP | 6п24 | [16] |
| ARVD9 | 609040 | ПКП2 | 12п11 | [17] |
| ARVD10 | 610193 | DSG2 | 18q12.1-q12 | [18][19] |
| ARVD11 | 610476 | DSC2 | 18q12.1 | [20][21] |
| ARVD12 | 611528 | ЮП | 17q21 | [22][23] |
| ILK | 11п15.4 | [24] | ||
| LMNA | [25] |
Патогенез
В патогенез ACM в значительной степени неизвестно. Апоптоз (запрограммированная гибель клеток), по-видимому, играет большую роль. Ранее считалось, что вовлечен только правый желудочек, но недавние когорты показали много случаев заболевания левого желудочка и болезни двух желудочков. Болезненный процесс начинается в субэпикардиальной области и продвигается к поверхности эндокарда, приводя к трансмуральному поражению (возможно, за счет аневризматической дилатации желудочков). Остаточный миокард ограничен субэндокардиальной областью и трабекулами желудочков. Эти трабекулы могут стать гипертрофированными.
Расширение аневризмы при вскрытии выявляется в 50% случаев. Обычно это происходит в диафрагмальной, апикальной и инфундибулярной областях (известном как треугольник дисплазии). Левый желудочек поражен у 50–67% людей. Если поражен левый желудочек, это обычно является поздним течением болезни и имеет плохой прогноз.
При ACM наблюдаются две патологические модели: жировая инфильтрация и фибро-жировая инфильтрация.
Жировая инфильтрация
Первая, жировая инфильтрация, ограничивается правым желудочком. Это включает частичное или почти полное замещение миокарда жировой тканью. без истончение стен. Он затрагивает преимущественно апикальную и инфундибулярную области правого желудочка. Левый желудочек и межжелудочковая перегородка обычно не затрагиваются. При жировой инфильтрации воспалительных инфильтратов не наблюдается. Есть свидетельства миоцит (клетки миокарда) дегенерация и смерть наблюдаются в 50% случаев жировой инфильтрации.
Фибро-жировая инфильтрация
Вторая, фиброзно-жировая инфильтрация, включает замену миоцитов фибро-жировой тканью. Пятнистый миокардит поражает до 2/3 случаев с воспалительными инфильтратами (в основном Т-клетки ) видно на микроскопии. Атрофия миокарда возникает из-за травмы и апоптоз. Это приводит к истончению свободной стенки ПЖ (до толщины <3 мм). Миоциты замещаются фибро-жировой тканью. Предпочтительно вовлеченные области включают в себя впускной тракт ПЖ, выводной тракт ПЖ и верхушку ПЖ. Однако в некоторых случаях может быть задействована свободная стенка ЛЖ. Поражение межжелудочковой перегородки встречается редко. Пораженные участки склонны к образованию аневризмы.
Роль упражнений
Недавно некоторые исследования определили, что интенсивные упражнения представляют собой новый риск ускоренного прогрессирования заболевания. Одно ретроспективное исследование с участием 301 пациента убедительно продемонстрировало, что субпопуляции, участвующие в интенсивной физической активности (например, профессиональные спортсмены), имели более раннее начало симптомов и более раннюю смертность по сравнению с другими популяциями.[26]
Желудочковые аритмии

Желудочковые аритмии из-за ACM обычно возникают из-за пораженного правого желудочка. Тип аритмии колеблется от частой преждевременные желудочковые комплексы (PVC) в вентрикулярная тахикардия (VT) в мерцание желудочков (VF).
Хотя инициирующий фактор желудочковых аритмий неясен, это может быть связано с триггерной активностью или повторным входом.
Желудочковые аритмии обычно связаны с физической нагрузкой, что позволяет предположить, что они чувствительны к катехоламинам. Желудочковые сокращения обычно имеют отклонение оси вправо. Множественная морфология желудочковой тахикардии может присутствовать у одного и того же человека, что предполагает множественные аритмогенный очаги или проводящие пути.
Тахикардия оттока правого желудочка (RVOT) является наиболее частой ЖТ, наблюдаемой у людей с ACM. В этом случае ЭКГ показывает блокада левой ножки пучка Гиса (LBBB) морфология с нижней осью.
Диагностика
В дифференциальная диагностика К желудочковой тахикардии из-за АКМ относятся:
- Врожденный порок сердца
- Отремонтирован тетралогия Фалло
- Аномалия Эбштейна
- Аномалия Уля
- Дефект межпредсердной перегородки
- Частичный аномальный венозный возврат
- Приобретенный порок сердца
- Заболевание трехстворчатого клапана
- Легочная гипертония
- Инфаркт правого желудочка
- Возвратная тахикардия связки-ответвления
- Разное
- Предварительно возбужденная атриовентрикулярная тахикардия
- Идиопатическая тахикардия при ПВО
- Саркоидоз
Для постановки диагноза АКМ используется ряд клинических тестов, в том числе ЭКГ (ЭКГ), эхокардиография, ангиография правого желудочка, МРТ сердца и генетическое тестирование.
ЭКГ
У 90% людей с АРВД есть отклонения ЭКГ. Наиболее частая аномалия ЭКГ, наблюдаемая при АКМ, - это инверсия зубца Т в отведениях V.1 к V3. Однако это неспецифический вывод, и его можно рассматривать как нормальный вариант в блокада правой ножки пучка Гиса (БПНПГ), женщины и дети до 12 лет.
Сама БПНПГ часто наблюдается у людей с АКМ. Это может быть связано с задержкой активации правого желудочка, а не с какой-либо внутренней аномалией в правой ножке пучка Гиса.

Эпсилон-волна встречается примерно у 50% пациентов с ACM. Это описывается как терминальная выемка в комплексе QRS. Это связано с замедлением внутрижелудочковой проводимости. Эпсилон-волна можно увидеть на поверхностной ЭКГ; однако чаще это наблюдается на ЭКГ с усредненным сигналом.
Желудочковый эктопия на поверхности ЭКГ при установке АКМ обычно блокада левой ножки пучка Гиса (LBBB) морфология с осью QRS от -90 до +110 градусов. Источником эктопических сокращений обычно является одна из трех областей жировой дегенерации («треугольник дисплазии»): тракт оттока правого желудочка, тракт притока правого желудочка и верхушка правого желудочка.
Сигнал усредненной ЭКГ (SAECG ) используется для обнаружения поздних потенциалов и эпсилон-волн у людей с АКМ.
Эхокардиография
Эхокардиография может выявить увеличенный гипокинетический правый желудочек со стенкой ПЖ толщиной как бумага. Расширение правого желудочка вызовет дилатацию фиброзного кольца трикуспидального клапана с последующим расширением. трикуспидальная регургитация. Также может присутствовать парадоксальное движение перегородки.
МРТ

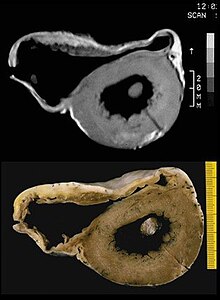
Жировая инфильтрация свободной стенки ПЖ может быть видна на МРТ сердца. Жир имеет повышенную интенсивность на изображениях, взвешенных по T1. Однако может быть трудно дифференцировать внутримиокардиальный жир и эпикардиальный жир, который обычно наблюдается рядом с нормальным сердцем. Кроме того, субтрикуспидальный отдел может быть трудно отличить от атриовентрикулярной борозды, которая богата жиром.
МРТ сердца может визуализировать крайнее истончение и акинез свободной стенки ПЖ. Однако нормальная стенка без ПЖ может иметь толщину около 3 мм, что делает тест менее чувствительным.
Ангиография
Ангиография правого желудочка считается Золотой стандарт для диагностики АКМ. Результаты, согласующиеся с ACM, представляют собой акинетическую или дискинетическую выпуклость, локализованную в инфундибулярной, апикальной и субтрикуспидальной областях правого желудочка. Специфичность 90%; тем не менее, тест зависит от наблюдателя.
Биопсия
Трансвенозная биопсия правого желудочка может быть высокоспецифичной для ACM, но имеет низкую чувствительность. К ложноположительным результатам относятся другие состояния с жировой инфильтрацией желудочка, такие как хроническое злоупотребление алкоголем и мышечная дистрофия Дюшенна / Беккера.
Однако ложноотрицательные результаты являются обычным явлением, поскольку болезнь обычно прогрессирует от эпикарда к эндокарду (при этом образец биопсии поступает из эндокарда), а также из-за сегментарного характера заболевания. Кроме того, из-за тонкой, как бумага, свободной стенки правого желудочка, которая является обычным явлением при этом заболевании, большинство образцов биопсии берутся из межжелудочковой перегородки, которая обычно нет вовлечены в процесс болезни.
Образец биопсии, соответствующий ACM, должен иметь> 3% жира,> 40% фиброзной ткани и <45% миоцитов.
Посмертная гистологическая демонстрация полной замены миокарда правого желудочка жировой или фибро-жировой тканью согласуется с ACM.
Генетическое тестирование
ACM - это аутосомно-доминантный черта с уменьшенным пенетрантность. Приблизительно у 40–50% пациентов с АКМ обнаружена мутация в одном из нескольких генов, кодирующих компоненты десмосома, который может помочь подтвердить диагноз ACM.[27] Поскольку ACM является аутосомно-доминантным признаком, дети пациентов с ACM имеют 50% шанс унаследовать мутацию, вызывающую заболевание. Каждый раз, когда мутация выявляется с помощью генетического тестирования, можно использовать семейное генетическое тестирование, чтобы отличить родственников, которые подвержены риску заболевания, и тех, кто не подвержен риску. Генетическое тестирование ACM клинически доступно.[28]
Диагностические критерии
Патогномоничной особенности АКМ нет. Диагноз ACM основан на сочетании основных и второстепенных критериев. Для постановки диагноза ACM необходимы два основных критерия или же 1 основной и 2 второстепенных критерия или же 4 второстепенных критерия.[29]
Основные критерии
- Дисфункция правого желудочка
- Сильная дилатация и уменьшение ПЖ фракция выброса с незначительным нарушением ЛЖ или без него
- Локализованные аневризмы ПЖ
- Тяжелая сегментарная дилатация ПЖ
- Характеристика тканей
- Фибро-жировое замещение миокарда при эндомиокардиальной биопсии
- Электрокардиографические аномалии
- Волны Эпсилона в V1 - V3
- Локализованное удлинение (> 110 мс) QRS в V1 - V3
- Инвертированные зубцы T в V1 -V3 у лица старше 12 лет, при отсутствии блокада правой ножки пучка Гиса (БПНПГ)
- Желудочковая тахикардия с блокада левой ножки пучка Гиса (LBBB) морфология с верхней осью
- История семьи
- Семейное заболевание подтверждено клинически, вскрытием или хирургическим вмешательством.
Второстепенные критерии
- Дисфункция правого желудочка
- Легкая глобальная дилатация ПЖ и / или пониженная фракция выброса при нормальном ЛЖ.
- Легкая сегментарная дилатация ПЖ
- Регионарный гипокинез ПЖ
- Характеристика тканей
- Электрокардиографические аномалии
- Поздние потенциалы по сигналу усредненной ЭКГ.
- Желудочковая тахикардия с блокада левой ножки пучка Гиса (LBBB) морфология с нижней или неизвестной осью
- Частые ЖЭ (> 500 ЖЭ / 24 часа)
Управление
Целью лечения АКМ является снижение частоты внезапной сердечной смерти. Это вызывает клиническую дилемму: как профилактически лечить бессимптомного пациента, которому был поставлен диагноз во время семейного скрининга.
Определенная подгруппа людей с АКМ считается подверженной высокому риску внезапной сердечной смерти. Связанные характеристики включают:
- Юный возраст
- Соревновательная спортивная деятельность
- Злокачественный семейный анамнез
- Обширное заболевание ПЖ со сниженной фракцией выброса правого желудочка.
- Поражение левого желудочка
- Обморок
- Эпизод желудочковой аритмии
Варианты лечения включают фармакологическое, хирургическое, катетерную абляцию и установку имплантируемый кардиовертер-дефибриллятор.
До принятия решения о варианте лечения, запрограммированная электростимуляция в электрофизиология лаборатория может быть проведена для получения дополнительной прогностической информации. Цели программной стимуляции включают:
- Оценка аритмогенного потенциала болезни
- Оцените гемодинамические последствия устойчивой ЖТ.
- Определите, можно ли прервать ЖТ с помощью антитахикардической стимуляции.
Независимо от выбранного варианта ведения пациента, как правило, рекомендуется изменить образ жизни, в том числе отказаться от физических упражнений, стимуляторов сердечной деятельности (например, кофеина, никотина, псевдоэфедрина) и алкоголя.
Что касается физической активности и упражнений, пациенты с ARVC, а также носители генов патогенных ARVC-ассоциированных десмосомных мутаций не должны участвовать в спортивных соревнованиях. Этим пациентам следует рекомендовать ограничить свои программы физических упражнений занятиями в свободное время и оставаться под клиническим наблюдением.[30]
Лекарства
Фармакологическое лечение АКМ включает подавление аритмии и предотвращение образования тромбов.
Соталол, а бета-блокатор и класс III антиаритмическое средство, является наиболее эффективным антиаритмическим средством при АКМ. Другие используемые антиаритмические средства включают: амиодарон и обычные бета-адреноблокаторы (например, метопролол). Если используются антиаритмические агенты, их эффективность следует контролировать с помощью серийного амбулаторного холтеровского мониторирования, чтобы продемонстрировать уменьшение аритмических событий.
Пока ингибиторы ангиотензинпревращающего фермента (Ингибиторы АПФ) хорошо известны тем, что замедляют прогрессирование при других кардиомиопатиях, их полезность при АКМ не доказана.
Лица со сниженной фракцией выброса правого желудочка с дискинетическими участками правого желудочка могут получить пользу от длительной антикоагуляции с варфарин для предотвращения тромбообразования и последующего легочная эмболия.
Катетерная абляция
Катетерная абляция может использоваться для лечения трудноизлечимой желудочковой тахикардии. Успешность этого метода составляет 60–90%.[31] К сожалению, из-за прогрессирующего характера заболевания часто возникают рецидивы (частота рецидивов 60%) с образованием новых аритмогенных очагов. Показания к катетерной абляции включают резистентную к лекарствам желудочковую тахикардию и частые рецидивы желудочковой тахикардии после МКБ размещение, вызывающее частые разряды ИКД.
Имплантируемый кардиовертер-дефибриллятор
An МКБ является наиболее эффективной профилактикой внезапной сердечной смерти. Из-за непомерно высокой стоимости ИКД их обычно не устанавливают всем пациентам с АКМ.
Показания к установке ИКД в условиях АКМ включают:
- Остановка сердца из-за ЖТ или ФЖ
- Симптоматическая ЖТ, которая не индуцируется во время запрограммированная стимуляция
- Неудачная запрограммированная лекарственная терапия под контролем стимуляции
- Тяжелое поражение ПЖ с плохой переносимостью ЖТ
- Внезапная смерть ближайшего члена семьи
Поскольку ИКД обычно вводятся через трансвенозный доступ в правый желудочек, возникают осложнения, связанные с установкой ИКД и последующим наблюдением.
Из-за чрезмерного истончения свободной стенки ПЖ во время имплантации можно перфорировать ПЖ, что потенциально может вызвать тампонада перикарда. По этой причине предпринимаются все попытки разместить электрод дефибриллятора на межжелудочковой перегородке.
После успешной имплантации прогрессирующий характер заболевания может привести к фиброзно-жировому замещению миокарда в месте установки электрода. Это может привести к недооценке электрической активности человека (потенциально вызывая неспособность определять ЖТ или ФЖ) и к неспособности стимулировать желудочек.
Пересадка сердца
Пересадка сердца может выполняться в ACM. Это может быть показано, если аритмии, связанные с заболеванием, неконтролируемы, или если имеется тяжелая двухжелудочковая сердечная недостаточность, которая не поддается лечению с помощью фармакологической терапии.
Семейный скрининг
Все члены семьи первой степени родства пострадавшего должны пройти скрининг на ACM. Это используется для установления образца наследования. Если не указано иное, обследование следует начинать в подростковом возрасте. Скрининговые тесты включают:
- Эхокардиограмма
- ЭКГ
- Сигнал усредненной ЭКГ
- Холтеровское мониторирование
- МРТ сердца
- Нагрузочный тест с физической нагрузкой
Прогноз
У пациентов с АКМ длительное время бессимптомно. Хотя это генетически передающееся заболевание, люди в подростковом возрасте могут не иметь каких-либо характеристик ACM на скрининговых тестах.
Многие люди имеют симптомы, связанные с желудочковой тахикардией, например учащенное сердцебиение, головокружение или обморок. Другие могут иметь симптомы и признаки, связанные с правожелудочковой недостаточностью, такие как отек нижних конечностей или застой в печени с повышенным содержанием печеночных ферментов.
АКМ - заболевание прогрессирующее. Со временем правый желудочек становится более вовлеченным, что приводит к правожелудочковой недостаточности. Правый желудочек выйдет из строя до того, как возникнет дисфункция левого желудочка. Однако к тому времени, когда у человека появятся признаки явной правожелудочковой недостаточности, будет обнаружено гистологическое поражение левого желудочка. В конце концов, левый желудочек также будет вовлечен, что приведет к двухжелудочковой недостаточности. Признаки и симптомы левожелудочковой недостаточности могут стать очевидными, включая застойную сердечную недостаточность, фибрилляцию предсердий и повышенную частоту тромбоэмболических событий.
Эпидемиология
Распространенность АКМ составляет около 1/10 000 от общей популяции в Соединенные Штаты, хотя некоторые исследования показали, что это может быть так же часто, как 1/1000. Недавно было обнаружено, что 1/200 являются носителями мутаций, предрасполагающих к ACM.[32] Основываясь на этих выводах и других данных, считается, что у большинства пациентов могут потребоваться дополнительные факторы, такие как другие гены, спортивный образ жизни, воздействие определенных вирусов и т. Д., Чтобы в конечном итоге у пациента развились признаки и симптомы ACM.[33] На его долю приходится до 17% всех внезапных сердечных смертей среди молодых. В Италия распространенность составляет 40 на 10 000, что делает его наиболее частой причиной внезапной сердечной смерти среди молодого населения.[34]
Известные случаи
- Коламбус Крю полузащитник Кирк Урсо 5 августа 2012 года потерял сознание вместе с друзьями, а через час был объявлен мертвым. Позднее вскрытие показало, что причиной является болезнь.[35][36]
- Севилья и испанский международный левый защитник Антонио Пуэрта умер от этого состояния в возрасте 22 лет, 28 августа 2007 г., через три дня после нескольких остановок сердца при оспаривании Ла Лига игра против Хетафе.[37][38]
- англичанин Мэтт Гэдсби также умер от этого состояния после того, как потерял сознание на поле 9 сентября 2006 г., когда играл за Хинкли Юнайтед в Конференция Север игра против Harrogate Town.[39][40]
- Сюзанна Кро, американская детская актриса, наиболее известная по роли в Семья Куропаток, внезапно умерла от этого заболевания в 2015 году в возрасте 52 лет.[41]
- Джеймс Тейлор Английский международный игрок в крикет, вышел на пенсию с апреля 2016 года.[42]
- Крисси Тейлор Американская модель умерла 2 июля 1995 года в семейном доме во Флориде. Официальной причиной ее смерти была сердечная аритмия и тяжелая астма, последняя из которых у нее никогда не диагностировалась. Ее семья поручила независимым экспертам изучить образцы тканей ее сердечной мышцы, и они пришли к выводу, что наиболее вероятной причиной смерти был пропущенный диагноз АКМ.
- Джордан Бойд (1997-2013), канадский юный хоккеист. Заболевание ему поставили посмертно после того, как он скончался после обрушения в тренировочном лагере в 2013 году.[43]
Смотрите также
Рекомендации
- ^ Пиличу, Каллиопи; Тиене, Гаэтано; Баус, Барбара; Ригато, Илария; Лаццарини, Элизабетта; Мильоре, Федерико; Пераццоло Марра, Мартина; Риццо, Стефания; Зорзи, Алессандро; Далиенто, Лучано; Коррадо, Доменико; Бассо, Кристина (2 апреля 2016 г.). «Аритмогенная кардиомиопатия». Журнал редких заболеваний Orphanet. 11 (1): 33. Дои:10.1186 / s13023-016-0407-1. ЧВК 4818879. PMID 27038780.
- ^ Фридберг И.М., Фитцпатрик ТБ (2003). Дерматология Фитцпатрика в общей медицине (6-е изд.). Макгроу-Хилл. ISBN 978-0-07-138076-8.
- ^ Джеймс В.Д., Бергер Т.Г., Элстон Д.М., Одом РБ (2006). Болезни кожи Эндрюса: клиническая дерматология (10-е изд.). Сондерс. ISBN 978-0-7216-2921-6.
- ^ а б c Коррадо, Доменико; Бассо, Кристина; Судья, Дэниел П. (2017-09-15). «Аритмогенная кардиомиопатия». Циркуляционные исследования. 121 (7): 784–802. Дои:10.1161 / CIRCRESAHA.117.309345. ISSN 1524-4571. ЧВК 4818879. PMID 28912183.
- ^ Коррадо, Доменико; Link, Mark S .; Калкинс, Хью (2017-01-05). «Аритмогенная кардиомиопатия правого желудочка». Медицинский журнал Новой Англии. 376 (1): 61–72. Дои:10.1056 / NEJMra1509267. ISSN 1533-4406. PMID 28052233.
- ^ Cox MG, van der Zwaag PA, van der Werf C, van der Smagt JJ, Noorman M, Bhuiyan ZA, Wiesfeld AC, Volders PG, van Langen IM, Atsma DE, Dooijes D, van den Wijngaard A, Houweling AC, Jongbloed JD , Йорданс Л., Крамер М.Дж., Довенданс П.А., де Баккер Дж.М., Уайлд А.А., ван Тинтелен Дж. П., Хауэр Р. Н. (июнь 2011 г.). «Аритмогенная дисплазия правого желудочка / кардиомиопатия: патогенные мутации десмосом у основных пациентов предсказывают исход семейного скрининга: голландское последующее исследование генотипа-фенотипа аритмогенной дисплазии правого желудочка / кардиомиопатии». Тираж. 123 (23): 2690–700. Дои:10.1161 / cycleaha.110.988287. PMID 21606396.
- ^ Fressart V, Duthoit G, Donal E, Probst V, Deharo JC, Chevalier P, Klug D, Dubourg O, Delacretaz E, Cosnay P, Scanu P, Extramiana F, Keller D, Hidden-Lucet F, Simon F, Bessirard V, Roux-Buisson N, Hebert JL, Azarine A, Casset-Senon D, Rouzet F, Lecarpentier Y, Fontaine G, Coirault C, Frank R, Hainque B, Charron P (июнь 2010 г.). «Анализ десмосомных генов при аритмогенной дисплазии / кардиомиопатии правого желудочка: спектр мутаций и клиническое влияние на практике». Europace. 12 (6): 861–8. Дои:10.1093 / europace / euq104. PMID 20400443.
- ^ Klauke B, Kossmann S, Gaertner A, Brand K, Stork I, Brodehl A, Dieding M, Walhorn V, Anselmetti D, Gerdes D, Bohms B, Schulz U, Zu Knyphausen E, Vorgerd M, Gummert J, Milting H (декабрь 2010). «De novo desmin-мутация N116S связана с аритмогенной кардиомиопатией правого желудочка». Молекулярная генетика человека. 19 (23): 4595–607. Дои:10,1093 / hmg / ddq387. PMID 20829228.
- ^ Brodehl A, Hedde PN, Dieding M, Fatima A, Walhorn V, Gayda S, Šarić T., Klauke B, Gummert J, Anselmetti D, Heilemann M, Nienhaus GU, Milting H (май 2012 г.). «Двухцветная фотоактивационная локализационная микроскопия мутантов десмина, связанных с кардиомиопатией». Журнал биологической химии. 287 (19): 16047–57. Дои:10.1074 / jbc.M111.313841. ЧВК 3346104. PMID 22403400.
- ^ Beffagna G, Occhi G, Nava A, Vitiello L, Ditadi A, Basso C, Bauce B, Carraro G, Thiene G, Towbin JA, Danieli GA, Rampazzo A (февраль 2005 г.). «Регуляторные мутации в гене трансформирующего фактора роста-бета3 вызывают аритмогенную кардиомиопатию правого желудочка типа 1». Сердечно-сосудистые исследования. 65 (2): 366–73. Дои:10.1016 / j.cardiores.2004.10.005. PMID 15639475.
- ^ Милтинг Х., Лукас Н., Клауке Б., Кёрфер Р., Перро А., Остерзиль К.Дж., Фогт Дж., Петерс С., Тилечек Р., Варшань М. (август 2006 г.). «Составные полиморфизмы в гене рецептора рианодина 2, связанные с аритмогенной кардиомиопатией правого желудочка». Сердечно-сосудистые исследования. 71 (3): 496–505. Дои:10.1016 / j.cardiores.2006.04.004. PMID 16769042.
- ^ Мернер Н.Д., Ходжкинсон К.А., Хейвуд А.Ф., Коннорс С., Френч В.М., Дренкхан Дж. Д., Купприон С., Рамаданова К., Тирфельдер Л., Маккенна В., Галлахер Б., Моррис-Ларкин Л., Бассет А. С., Парфри П. С., Янг Т.Л. (апрель 2008 г.) . «Аритмогенная кардиомиопатия правого желудочка типа 5 представляет собой полностью проникающее, летальное аритмическое нарушение, вызванное миссенс-мутацией в гене TMEM43». Американский журнал генетики человека. 82 (4): 809–21. Дои:10.1016 / j.ajhg.2008.01.010. ЧВК 2427209. PMID 18313022.
- ^ Кристенсен А.Х., Андерсен С.Б., Тибьярг-Хансен А., Хаунсо С., Свендсен Дж. Х. (сентябрь 2011 г.). «Мутационный анализ и оценка кардиальной локализации TMEM43 при аритмогенной кардиомиопатии правого желудочка». Клиническая генетика. 80 (3): 256–64. Дои:10.1111 / j.1399-0004.2011.01623.x. PMID 21214875.
- ^ Klauke B, Kossmann S, Gaertner A, Brand K, Stork I, Brodehl A, Dieding M, Walhorn V, Anselmetti D, Gerdes D, Bohms B, Schulz U, Zu Knyphausen E, Vorgerd M, Gummert J, Milting H (декабрь 2010). «De novo desmin-мутация N116S связана с аритмогенной кардиомиопатией правого желудочка». Молекулярная генетика человека. 19 (23): 4595–607. Дои:10,1093 / hmg / ddq387. PMID 20829228.
- ^ Бермудес-Хименес Ф.Дж., Карриель V, Бродель А., Аламинос М., Кампос А, Ширмер I, Милтинг Х., Абрил Б. Б., Альварес М., Лопес-Фернандес С., Гарсиа-Джустиниани Д., Монсеррат Л., Терседор Л., Хименес-Хименес ( Апрель 2018 г.). «Новая мутация десмина p.Glu401Asp нарушает образование волокон, нарушает целостность клеточной мембраны и вызывает тяжелую аритмогенную кардиомиопатию / дисплазию левого желудочка». Тираж. 137 (15): 1595–1610. Дои:10.1161 / CIRCULATIONAHA.117.028719. PMID 29212896.
- ^ Bauce B, Basso C, Rampazzo A, Beffagna G, Daliento L, Frigo G, Malacrida S, Settimo L, Danieli G, Thiene G, Nava A (август 2005 г.). «Клинический профиль четырех семей с аритмогенной кардиомиопатией правого желудочка, вызванной доминантными мутациями десмоплакина». Европейский журнал сердца. 26 (16): 1666–75. Дои:10.1093 / eurheartj / ehi341. PMID 15941723.
- ^ Герулл Б., Хойзер А., Вихтер Т., Пол М., Бассон К. Т., Макдермотт Д. А., Лерман Б. Б., Марковиц С. М., Эллинор П. Т., Макрей К. А., Петерс С., Гроссманн К. С., Дренкхан Д., Мишели Б., Засс-Клаассен С., Бирчмайер В. Дитц Р., Брайтхардт Г., Шульце-Бар Э., Тирфельдер Л. (ноябрь 2004 г.). «Мутации в десмосомном белке плакофилине-2 часто встречаются при аритмогенной кардиомиопатии правого желудочка». Природа Генетика. 36 (11): 1162–4. Дои:10,1038 / ng1461. PMID 15489853.
- ^ Pilichou K, Nava A, Basso C, Beffagna G, Bauce B, Lorenzon A, Frigo G, Vettori A, Valente M, Towbin J, Thiene G, Danieli GA, Rampazzo A (март 2006). «Мутации в гене десмоглеина-2 связаны с аритмогенной кардиомиопатией правого желудочка». Тираж. 113 (9): 1171–9. Дои:10.1161 / CIRCULATIONAHA.105.583674. PMID 16505173.
- ^ Авад М.М., Далал Д., Чо Э, Амат-Аларкон Н., Джеймс К., Тичнелл К., Такер А., Рассел С.Д., Блумке Д.А., Дитц Х.С., Калкинс Х., судья Д.П. (июль 2006 г.). «Мутации DSG2 способствуют аритмогенной дисплазии / кардиомиопатии правого желудочка». Американский журнал генетики человека. 79 (1): 136–42. Дои:10.1086/504393. ЧВК 1474134. PMID 16773573.
- ^ Heuser A, Plovie ER, Ellinor PT, Grossmann KS, Shin JT, Wichter T., Basson CT, Lerman BB, Sasse-Klaassen S, Thierfelder L, MacRae CA, Gerull B (декабрь 2006 г.). «Мутант десмоколлин-2 вызывает аритмогенную кардиомиопатию правого желудочка». Американский журнал генетики человека. 79 (6): 1081–8. Дои:10.1086/509044. ЧВК 1698714. PMID 17186466.
- ^ Syrris P, Ward D, Evans A, Asimaki A, Gandjbakhch E, Sen-Chowdhry S, McKenna WJ (ноябрь 2006 г.). «Аритмогенная дисплазия / кардиомиопатия правого желудочка, связанная с мутациями в десмосомном гене десмоколлин-2». Американский журнал генетики человека. 79 (5): 978–84. Дои:10.1086/509122. ЧВК 1698574. PMID 17033975.
- ^ Антониадис Л., Цацопулу А., Анастасакис А., Сиррис П., Асимаки А., Панайотакос Д., Замбартас С., Стефанадис С., МакКенна В. Дж., Протонотариос Н. (сентябрь 2006 г.). «Аритмогенная кардиомиопатия правого желудочка, вызванная делециями в плакофилине-2 и плакоглобине (болезнь Наксоса) в семьях из Греции и Кипра: взаимосвязь генотип-фенотип, диагностические особенности и прогноз». Европейский журнал сердца. 27 (18): 2208–16. Дои:10.1093 / eurheartj / ehl184. PMID 16893920.
- ^ Асимаки А., Сиррис П., Вихтер Т., Маттиас П., Саффитц Дж. Э., МакКенна В. Дж. (Ноябрь 2007 г.). «Новая доминантная мутация в плакоглобине вызывает аритмогенную кардиомиопатию правого желудочка». Американский журнал генетики человека. 81 (5): 964–73. Дои:10.1086/521633. ЧВК 2265660. PMID 17924338.
- ^ Brodehl A, Rezazadeh S, Williams T., Munsie NM, Liedtke D, Oh T, Ferrier R, Shen Y, Jones SJ, Stiegler AL, Boggon TJ, Duff HJ, Friedman JM, Gibson WT, Childs SJ, Gerull B (февраль 2019 г. ). «Мутации в ILK, кодирующей интегрин-связанную киназу, связаны с аритмогенной кардиомиопатией». Трансляционные исследования. 208: 15–29. Дои:10.1016 / j.trsl.2019.02.004. ЧВК 7412573. PMID 30802431.
- ^ Форлео С, Кармозино М, Реста Н, Рампаццо А, Валечче Р., Соррентино С, Яковьелло М, Пизани Ф, Прочино Дж, Гербино А, Скардапане А, Симоне С, Калор М, Торретта С, Свелто М, Фавале С (2015) . «Клиническая и функциональная характеристика новой мутации в гене ламина а / с в семье из нескольких поколений с аритмогенной сердечной ламинопатией». PLOS ONE. 10 (4): e0121723. Bibcode:2015PLoSO..1021723F. Дои:10.1371 / journal.pone.0121723. ЧВК 4383583. PMID 25837155.
- ^ Маццанти, Андреа; Нг, Кевин; Фарагли, Алессандро; Мараджна, Риккардо; Чиодароли, Елена; Орфану, Николетта; Монтефорте, Никола; Мемми, Мирелла; Гамбелли, Патрик (декабрь 2016 г.). «Аритмогенная кардиомиопатия правого желудочка». Журнал Американского колледжа кардиологии. 68 (23): 2540–2550. Дои:10.1016 / j.jacc.2016.09.951. PMID 27931611.
- ^ Сен-Чоудри С., Сиррис П., МакКенна В. Дж. (Ноябрь 2007 г.). «Роль генетического анализа в ведении пациентов с аритмогенной дисплазией / кардиомиопатией правого желудочка». Журнал Американского колледжа кардиологии. 50 (19): 1813–21. Дои:10.1016 / j.jacc.2007.08.008. PMID 17980246.
- ^ Обзор генетического тестирования ARVD / C
- ^ Маркус, Фрэнк И. (2010). «Диагностика аритмогенной кардиомиопатии / дисплазии правого желудочка. Предлагаемая модификация критериев рабочей группы». Тираж.
- ^ Пелличча, А (2019). «Рекомендации для спортсменов с кардиомиопатиями, миокардитом и перикардитом по занятиям спортом и спортом в свободное время: заявление секции спортивной кардиологии Европейской ассоциации профилактической кардиологии (EAPC)». Европейский журнал сердца. 40: 19–33.
- ^ Фонтен Дж., Тонет Дж., Галле Й, Ласко Дж., Хидден-Люсет Ф., Ауат П., Халими Ф., Пулен Ф., Джонсон Н., Чарфеддин Х., Фрэнк Р. (ноябрь 2000 г.). «Катетерная абляция желудочковой тахикардии при аритмогенной дисплазии правого желудочка: 16-летний опыт». Текущие кардиологические отчеты. 2 (6): 498–506. Дои:10.1007 / s11886-000-0034-1. PMID 11203287.
- ^ Lahtinen AM, Lehtonen E, Marjamaa A, Kaartinen M, Heliö T, Porthan K, Oikarinen L, Toivonen L, Swan H, Jula A, Peltonen L, Palotie A, Salomaa V, Kontula K (август 2011 г.). «Преобладающие в популяции десмосомные мутации, предрасполагающие к аритмогенной кардиомиопатии правого желудочка». Ритм сердца. 8 (8): 1214–21. Дои:10.1016 / j.hrthm.2011.03.015. PMID 21397041.
- ^ Джайн Р. Атлетический статус и аритмогенная дисплазия / кардиомиопатия правого желудочка: от физиологических наблюдений к патологическому объяснению. Гипотеза 2010, 8 (1): e2. - Смотрите больше на: http://www.hypothesisjournal.com/?p=844#sthash.aB859Jm2.dpuf
- ^ Коррадо Д., Фонтейн Г., Аритмогенная дисплазия правого желудочка / кардиомиопатия. Необходимость в международном регистре. Тираж 2000 г .; 101: e101-e106
- ^ Джарди А. «22-летний полузащитник экипажа Кирк Урсо скончался после того, как его доставили в больницу из бара». Коламбус Диспетч. Диспетчерская полиграфическая компания. Получено 21 сентября 2012.
- ^ Джарди А. «Коронер: Урсо из команды умер от ранее существовавшего сердечного приступа». Коламбус Диспетч. Диспетчерская полиграфическая компания. Получено 21 сентября 2012.
- ^ «Звезда Севильи перенесла сердечный приступ». BBC Sport. 2007-08-25. Получено 2007-08-25.
- ^ Звезда Севильи умерла после обвала
- ^ "Причина смерти". Группа сердечных наследственных заболеваний. Архивировано из оригинал 18 августа 2006 г.. Получено 2006-10-31.
- ^ «Шок при смерти звездного игрока». icBirmingham.co.uk. 11 сентября 2006 г.. Получено 2007-11-26.
- ^ Сюзанна Кро умерла от редкого сердечного приступа, сообщил коронер, msn.com; по состоянию на 27 октября 2015 г.
- ^ "Джеймс Тейлор: игрок с битой Англии и Ноттингемшира вынужден уйти в отставку". BBC Sport. 2016-04-12. Получено 2016-05-15.
- ^ Жизнь и карьера Джордана Бойда | Герои домашней команды НХЛ, получено 2019-10-14
внешняя ссылка
| Классификация | |
|---|---|
| Внешние ресурсы |
