Рак яичников - Ovarian cancer
| Рак яичников | |
|---|---|
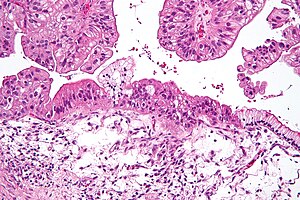 | |
| Микрофотография муцинозной карциномы яичников окрашенный H&E. | |
| Специальность | Онкология, гинекология |
| Симптомы | Рано: нечеткий[1] Потом: вздутие живота, боль в области таза, вздутие живота, потеря аппетита[1] |
| Обычное начало | Обычный возраст постановки диагноза 63 года.[2] |
| Типы | Карцинома яичников, опухоль зародышевых клеток, стромальная опухоль полового канатика[3] |
| Факторы риска | Никогда не иметь детей, гормональная терапия после менопауза, лекарства от бесплодия, ожирение, генетика[4][3][5] |
| Диагностический метод | Биопсия ткани[1] |
| Уход | Хирургия, радиационная терапия, химиотерапия[1] |
| Прогноз | Пятилетняя выживаемость c. 49% (США)[6] |
| Частота | 1,2 миллиона (2015)[7] |
| Летальные исходы | 161,100 (2015)[8] |
Рак яичников это рак который формируется в или на яичник.[4][9] Это приводит к ненормальному клетки которые имеют возможность вторгаться или распространять к другим частям тела.[10] Когда этот процесс начинается, симптомы могут отсутствовать или проявляться только неопределенно.[1] Симптомы становятся более заметными по мере прогрессирования рака.[1][11] Эти симптомы могут включать вздутие живота, боль в области таза, вздутие живота, и потеря аппетита, среди прочего.[1] Общие области, в которые может распространяться рак, включают подкладка живота, лимфатический узел, легкие, и печень.[12]
Риск рака яичников увеличивается у женщин с овулированный больше за свою жизнь. Сюда входят те, у кого никогда не было детей, те, у кого овуляция начинается в более молодом возрасте, и те, кто достигает менопаузы в более старшем возрасте.[3] Другие факторы риска включают: гормональная терапия после менопауза, лекарства от бесплодия, и ожирение.[4][5] Факторы, снижающие риск, включают: гормональные противозачаточные, перевязка маточных труб, и кормление грудью.[5] Около 10% случаев связаны с наследственным генетическим риском; женщины с мутациями в генах BRCA1 или же BRCA2 вероятность развития заболевания составляет около 50%.[3] Карцинома яичников - наиболее распространенный тип рака яичников, составляющий более 95% случаев.[3] Существует пять основных подтипов карциномы яичников, из которых серозная карцинома высокой степени злокачественности (HGSC) является наиболее распространенным.[3] Эти опухоли яичников как полагают, начинаются в клетках, покрывающих яичники,[3] хотя некоторые могут образоваться в Фаллопиевы трубы.[13] Менее распространенные типы рака яичников включают: опухоли половых клеток[14]и стромальные опухоли полового канатика.[3] Диагноз рака яичников подтверждается биопсия ткани, обычно удаляемой во время операции.[1]
Скрининг не рекомендуется женщинам, относящимся к группе среднего риска, поскольку данные не подтверждают снижение смертности и высокий уровень ложноположительные тесты может привести к ненужной операции, которая сопровождается собственными рисками.[15] Людям из группы очень высокого риска в профилактических целях могут удалить яичники.[4] При выявлении и лечении на ранней стадии рак яичников часто излечим.[1] Лечение обычно включает комбинацию хирургических вмешательств, радиационная терапия, и химиотерапия.[1] Результаты зависят от степени заболевания, подтипа имеющегося рака и других заболеваний.[16][3] Общая пятилетняя выживаемость в США - 49%.[6] В развивающихся странах результаты хуже.[3]
В 2012 году новые случаи заболевания зарегистрированы примерно у 239 000 женщин.[3] В 2015 году он присутствовал у 1,2 миллиона женщин и привел к смерти 161 100 человек во всем мире.[8][7] Среди женщин он занимает седьмое место по распространенности рака и восьмое место среди причин смерти от рака.[3] Типичный возраст постановки диагноза - 63 года.[2] Смерть от рака яичников чаще встречается в Северной Америке и Европе, чем в Африке и Азии.[3]
Признаки и симптомы
Ранние симптомы
Рано приметы и симптомы рака яичников может отсутствовать или быть незаметным. В большинстве случаев симптомы существуют в течение нескольких месяцев, прежде чем их можно будет распознать и поставлен диагноз.[17][18] Симптомы могут быть ошибочно диагностированы как синдром раздраженного кишечника.[19] Ранние стадии рака яичников обычно безболезненны. Симптомы могут различаться в зависимости от подтипа.[17] Яичников пограничные опухоли, также известные как опухоли яичников с низким злокачественным потенциалом (LMP), не вызывают увеличения CA125 уровни и не идентифицируются с помощью ультразвука. Типичные симптомы опухоли LMP могут включать: вздутие живота или тазовая боль. Особенно большие образования имеют тенденцию быть доброкачественными или пограничными.[20][17]
Наиболее типичные симптомы рака яичников включают: вздутие живота, боль или дискомфорт в животе или тазу, боль в спине, нерегулярные менструации или постменопаузальное вагинальное кровотечение, боль или кровотечение после или во время половой акт, потеря аппетита, усталость, понос, несварение желудка, изжога, запор, тошнота, чувство сытости, и, возможно, симптомы мочеиспускания (в том числе частое мочеиспускание и срочное мочеиспускание ).[18]
Поздние симптомы
Растущая масса может вызвать боль, если перекрут яичника развивается. Симптомы могут быть вызваны массовым надавливанием на другие органы брюшной полости или тазовыми метастазами.[17][21][22] Если эти симптомы начинают проявляться чаще или серьезнее, чем обычно, особенно после отсутствия значительных симптомов в анамнезе, считается, что это рак яичников.[17][20] Метастазы могут вызвать Узелок сестры Марии Джозеф.[22] Редко, тератомы может вызвать синдром растущей тератомы или же перитонеальный глиоматоз.[22] Некоторый опыт менометроррагия и аномальное вагинальное кровотечение после менопаузы в большинстве случаев. Другие общие симптомы включают: гирсутизм, боль в животе, вирилизация, и придаточная масса.[23]
Дети
У подростков или детей с опухолями яичников симптомы могут включать сильную боль в животе, раздражение брюшина, или же кровотечение.[24] Симптомы опухоли стромы полового канатика гормоны что может повлиять на развитие вторичные половые признаки. Опухоли стромы полового канатика у детей препубертатного возраста могут проявляться: раннее половое созревание; Также распространены боли в животе и вздутие живота. Подростки с опухолями стромы полового тяжа могут испытывать аменорея. По мере того, как рак прогрессирует, он может вызвать скопление жидкости в животе. Если злокачественное новообразование не было диагностировано к моменту возникновения асцита, оно обычно диагностируется вскоре после этого.[17] На поздних стадиях рака также могут возникать образования в брюшной полости, лимфатических узлах или плевральный выпот.[22]
Факторы риска
Рак яичников связан с продолжительностью овуляции. Таким образом не иметь детей является фактором риска рака яичников, вероятно, потому, что овуляция подавляется во время беременности. Во время овуляции клетки постоянно стимулируются к делению, пока продолжаются овуляторные циклы. Следовательно, люди, не родившие детей рискуют заболеть раком яичников в два раза больше, чем те, у кого есть. Более длительный период овуляции из-за раннего первая менструация и поздно менопауза также является фактором риска.[20][25][26] И ожирение, и заместительная гормональная терапия также повышают риск.[17]
Риск развития рака яичников меньше у женщин, у которых меньше менструальных циклов, нет менструальных циклов, кормление грудью, принимаете оральные контрацептивы, имеете многоплодную беременность и беременность в раннем возрасте. Риск развития рака яичников снижается у женщин, перенесших перевязка маточных труб (в просторечии известное как «привязка трубок»), удаление обоих яичников или гистерэктомия (операция, при которой удаляется матка, а иногда и шейка матки).[18] Возраст также является фактором риска.[17][16]
Гормоны
Использование лекарств от бесплодия может способствовать развитию яичников пограничная опухоль формация, но связь между ними спорна и трудна для изучения.[19] Препараты для лечения бесплодия могут быть связаны с более высоким риском пограничных опухолей.[22] Те, кто лечился от бесплодия, но остались нерожавшими, имеют более высокий риск развития эпителиального рака яичников; однако те, кто успешно лечится от бесплодия и впоследствии рожает, не подвергаются более высокому риску. Это может быть связано с выделением предраковых клеток во время беременности, но причина остается неясной.[20] Фактором риска может быть само бесплодие, а не лечение.[25]
Гормональные состояния, такие как синдром поликистоза яичников и эндометриоз связаны с раком яичников, но эта связь полностью не подтверждена.[19] Заместительная гормональная терапия в постменопаузе (ЗГТ) эстрогеном, вероятно, увеличивает риск рака яичников. Связь не была подтверждена в крупномасштабном исследовании,[20][27] но известные исследования, включая Исследование миллиона женщин поддержали эту ссылку. ЗГТ в постменопаузе с комбинацией эстрогена и прогестерона может увеличивать одновременный риск, если используется более 5 лет, но этот риск возвращается к норме после прекращения терапии.[25] Эстрогеновая ЗГТ с прогестинами или без них увеличивает риск эндометриоидных и серозных опухолей, но снижает риск муцинозных опухолей. Более высокие дозы эстрогена увеличивают этот риск.[22] Эндометриоз - еще один фактор риска рака яичников,[25] как и боль при менструации. Эндометриоз связан со светлоклеточными и эндометриоидными подтипами, серозными опухолями низкой степени злокачественности, опухолями I и II стадии, опухолями 1 степени и более низкой смертностью.[22]
До менопаузы ожирение может увеличить риск рака яичников, но после менопаузы этот риск отсутствует. Этот риск также актуален для тех, кто страдает ожирением и никогда не принимал ЗГТ. Подобная ассоциация с раком яичников проявляется у более высоких людей.[25]
Генетика

Семейный анамнез рака яичников является фактором риска рака яичников. Люди с наследственный неполипозный рак толстой кишки (Синдром Линча), а пациенты с генетическими аномалиями BRCA-1 и BRCA-2 подвергаются повышенному риску.
Основным генетическим фактором риска рака яичников является мутация BRCA1 или же BRCA2 гены, или в Ремонт несоответствия ДНК гены, присутствующие в 10% случаев рака яичников. Только один аллель нужно мутировать, чтобы подвергнуть человека высокому риску. Ген может быть унаследован по материнской или отцовской линии, но имеет переменную пенетрантность.[17][20] Хотя мутации в этих генах обычно связаны с повышенным риском рака груди, они также несут значительный пожизненный риск рака яичников, пик которого достигает человека в возрасте 40-50 лет. Самый низкий указанный риск составляет 30%, а самый высокий - 60%.[19][17][20] Мутации в BRCA1 имеют пожизненный риск развития рака яичников 15–45%.[22] Мутации в BRCA2 менее рискованны, чем те, у кого BRCA1с пожизненным риском от 10% (самый низкий риск) до 40% (самый высокий риск).[17][22] В среднем, BRCA-ассоциированные раки развиваются на 15 лет раньше, чем их спорадические аналоги, потому что людям, унаследовавшим мутации одной копии своего гена, нужна только одна мутация, чтобы запустить процесс канцерогенеза, тогда как людям с двумя нормальными генами нужно было бы приобрести две мутации.[20]
В США пять из 100 женщин с родственник первой степени с раком яичников в конечном итоге сами заболеют раком яичников, что подвергает тех, у кого есть больные члены семьи, в три раза больше риска, чем женщины с здоровыми членами семьи. Семь из 100 женщин с двумя или более родственниками с раком яичников в конечном итоге заболеют раком яичников.[20][28] В целом 5–10% случаев рака яичников имеют генетическую причину.[20] Мутации BRCA связаны с тяжелым серозным немуцинозным эпителиальным раком яичников.[22]
Сильная семейная история рак эндометрия, рак толстой кишки, или другой рак желудочно-кишечного тракта может указывать на наличие синдрома, известного как наследственный неполипозный колоректальный рак (также известный как синдром Линча), который повышает риск развития ряда видов рака, включая рак яичников. Синдром Линча вызван мутациями в генах восстановления несоответствия, включая MSH2, MLH1, MLH6, PMS1, и PMS2.[17] Риск рака яичников для человека с синдромом Линча составляет от 10 до 12 процентов.[17][20] Люди Исландское происхождение, Европейское еврейское происхождение /Еврейское происхождение ашкенази, и Венгерское происхождение имеют более высокий риск эпителиального рака яичников.[20] Ген бета-рецептора эстрогена (ESR2 ) кажется ключом к патогенезу и ответу на терапию.[29] Другие гены, связанные с раком яичников: BRIP1, MSH6, RAD51C и RAD51D.[30] CDH1, ЧЕК2, PALB2 и RAD50 также были связаны с раком яичников.[31]
Некоторые редкие генетические нарушения связаны с определенными подтипами рака яичников. Синдром Пейтца-Егерса, редкое генетическое заболевание, также предрасполагает людей к опухоль полового канатика с кольцевыми канальцами.[19][17] Болезнь Олье и Синдром Маффуччи связаны с опухоли гранулезных клеток у детей, а также может быть связан с опухолями Сертоли-Лейдига. Доброкачественные фибромы связаны с синдром невоидной базальноклеточной карциномы.[17]
Факторы окружающей среды
В промышленно развитых странах, за исключением Японии, высокий уровень развития эпителиального рака яичников, что может быть связано с диетой в этих странах. Кавказский на 30–40% выше риск рака яичников по сравнению с Чернить и Латиноамериканцы, вероятно, из-за социально-экономических факторов; белые женщины, как правило, имеют меньше детей и разную частоту гинекологических операций, которые влияют на риск рака яичников.[20]
Когортные исследования обнаружили корреляцию между потреблением молочных продуктов и раком яичников, но исследования случай-контроль не показывают эту корреляцию. Существуют неоднозначные доказательства относительно эффекта красное мясо и обработанное мясо при раке яичников.[22]
Предварительные данные свидетельствуют о том, что тальк, пестициды, и гербициды повышают риск рака яичников.[32] Американское онкологическое общество отмечает, что на данный момент ни одно исследование не смогло точно связать какое-либо химическое вещество в окружающей среде или в рационе человека напрямую с мутациями, вызывающими рак яичников.[33]
Другой
Употребление алкоголя не связано с раком яичников.[22][34] Другие факторы, которые были исследованы, например: курение, низкий уровень Витамин Д в крови,[35] наличие включения кисты яичников, и заражение вирус папилломы человека (причина некоторых случаев рак шейки матки ), были опровергнуты как факторы риска рака яичников.[19][22] Канцерогенность промежность тальк является спорным, потому что он может действовать как раздражитель, если попадает через репродуктивный тракт к яичникам.[22][20][25] Исследования методом случай-контроль показали, что использование перинеального талька действительно увеличивает риск рака яичников, но более частое использование талька не создает большего риска.[22] Использование тальк в других частях тела не имеет отношения к раку яичников.[25] Сидя регулярное лечение в течение продолжительных периодов времени связано с более высокой смертностью от эпителиального рака яичников. Риск не отменяется регулярными упражнениями, хотя и снижается.[36]
Возраст (до 70 лет) является фактором риска развития эпителиального рака яичников, поскольку в клетках может накапливаться больше мутаций, что в конечном итоге вызывает рак. Те, кому за 80, подвергаются несколько меньшему риску.[20]
Курение табак связан с более высоким риском муцинозный рак яичников; после Отказ от курения, риск со временем возвращается к норме. Диета с высоким содержанием животных жиров может быть связана с раком яичников, но связь неясна. Кажется, что диета играет очень небольшую роль в риске рака яичников.[25] Более высокие уровни С-реактивный белок связаны с более высоким риском развития рака яичников.[22]
Защитные факторы
Подавление овуляции, которое в противном случае могло бы повредить эпителий яичников и следовательно, воспаление, как правило, защитный. Этого эффекта можно добиться иметь детей, принимая комбинированные оральные контрацептивы, и кормление грудью, все из которых являются защитными факторами.[17] Более длительный период грудного вскармливания коррелирует с большим снижением риска рака яичников.[25] С каждым рождением риск рака яичников снижается еще больше, и этот эффект наблюдается до пяти родов. Комбинированные оральные контрацептивы снижают риск рака яичников до 50%, а защитный эффект комбинированных оральных контрацептивов может сохраняться 25–30 лет после их прекращения.[20][25] Регулярное использование аспирин или же ацетаминофен (парацетамол) может быть связан с более низким риском рака яичников; Другой НПВП похоже, не имеют подобного защитного эффекта.[22]
Перевязка маточных труб защищает, потому что канцерогены не могут добраться до яичника и фимбрии через влагалище, матку и фаллопиевы трубы.[17] Перевязка маточных труб также защищает женщин с мутацией BRCA1, но не мутацией BRCA2.[22] Гистерэктомия снижает риск и удаление как фаллопиевых труб, так и яичников (двустороннее сальпингоофорэктомия ) резко снижает риск не только рака яичников, но и рака груди.[19] Это по-прежнему является предметом исследования, так как связь между гистерэктомии и нижней риск развития рака яичников является спорным. Причины, по которым гистерэктомия может иметь защитное действие, по состоянию на 2015 г. не выяснены.[25]
Диета, включающая большое количество каротин, волокно, и витамины с низким содержанием жира - в частности, диета с некрахмалистыми овощами (например, брокколи и лук ) - может быть защитным,[20] хотя исследования в этой области все еще продолжаются.[25] Повышенное потребление кофеина и потребление более двух чашек чая в день были связаны с более низким риском рака яичников.[22] Курение табака защищает от опухолей стромы полового шнура.[23]
Патофизиология
| Ген мутировал | Тип мутации | Подтип | Распространенность |
|---|---|---|---|
| AKT1 | усиление | 3% | |
| AKT2 | усиление / мутация | 6%,[19] 20%[37] | |
| ARID1A | точечная мутация | эндометриоид и светлая клетка | |
| BECN1 | удаление | ||
| BRAF | точечная мутация | низкокачественный серозный | 0.5% |
| BRCA1 | бессмысленная мутация | полноценный серозный | 5% |
| BRCA2 | мутация сдвига рамки | полноценный серозный | 3% |
| CCND1 | усиление | 4% | |
| CCND2 | усиление регулирования | 15% | |
| CCNE1 | усиление | 20% | |
| CDK12 | полноценный серозный | ||
| CDKN2A | подавление (30%) и удаление (2%) | 32% | |
| CTNNB1 | чистая ячейка | ||
| DICER1 | миссенс-мутация (соматическая) | неэпителиальный | 29% |
| DYNLRB1 (км23) | мутация | 42% | |
| EGFR | усиление / сверхэкспрессия | 20% | |
| ERBB2 (Her2 / neu) | усиление / сверхэкспрессия | муцинозный и низкосерозный | 30% |
| ФМС | совместное выражение с CSF-1 | 50% | |
| FOXL2 | точечная мутация (от 402 C до G) | взрослая гранулезная клетка | ~100% |
| JAG1 | усиление | 2% | |
| JAG2 | усиление | 3% | |
| KRAS | усиление | муцинозный и низкосерозный | 11% |
| MAML1 | амплификация и точечная мутация | 2% | |
| MAML2 | амплификация и точечная мутация | 4% | |
| MAML3 | усиление | 2% | |
| MLH1 | 1% | ||
| NF1 | делеция (8%) и точечная мутация (4%) | полноценный серозный | 12% |
| NOTCH3 | амплификация и точечная мутация | 11% | |
| NRAS | низкокачественный серозный | ||
| PIK3C3 (PI3K3) | амплификация / мутация | 12–20% | |
| PIK3CA | усиление | эндометриоид и светлая клетка | 18% |
| PPP2R1A | эндометриоид и светлая клетка | ||
| PTEN | удаление | эндометриоид и светлая клетка | 7% |
| RB1 | делеция (8%) и точечная мутация (2%) | 10% | |
| TGF-β | мутация / сверхэкспрессия | 12% | |
| TP53 | мутация / сверхэкспрессия | полноценный серозный | 20–50% |
| TβRI | мутация | 33% | |
| TβRII | мутация | 25% | |
| USP36 | чрезмерное выражение |
Рак яичников образуется при ошибках в нормальном яичнике. рост клеток происходить. Обычно, когда клетки стареют или повреждаются, они умереть, и их место занимают новые клетки. Рак начинается, когда новые клетки образуются ненужными, а старые или поврежденные клетки не умирают должным образом. Накопление дополнительных клеток часто образует массу ткани, называемую опухоль яичника или рост. Эти аномальные раковые клетки имеют много генетические аномалии которые заставляют их чрезмерно расти.[38] Когда яичник выпускает яйцо, то яичный фолликул разрывается и становится желтое тело. Эту структуру необходимо восстановить путем деления клеток яичника.[25] Непрерывная овуляция в течение длительного времени означает усиление восстановления яичника путем деления клеток, которые могут приобретать мутации при каждом делении.[20]
В целом, наиболее частые генные мутации при раке яичников происходят в NF1, BRCA1, BRCA2, и CDK12. Рак яичников I типа, который обычно протекает менее агрессивно, обычно микроспутниковая нестабильность в нескольких генах, включая оба онкогена (в первую очередь BRAF и KRAS ) и опухолевые супрессоры (особенно PTEN ).[19] Наиболее частыми мутациями при раке I типа являются: КРАС, BRAF, ERBB2, PTEN, PIK3CA, и ARID1A.[22] Рак типа II, более агрессивный тип, имеет различные мутировавшие гены, в том числе p53, BRCA1, и BRCA2.[19] Раки низкой степени злокачественности обычно имеют мутации в KRAS, тогда как рак любой степени, развивающийся из опухолей с низким потенциалом злокачественности, обычно имеет мутации в p53.[20] Раковые опухоли типа I, как правило, развиваются из предшественников поражений, тогда как рак типа II может развиваться из серозная трубная интраэпителиальная карцинома.[22] Серозный рак которые имеют мутации BRCA, также неизбежно имеют мутации p53, что указывает на то, что удаление обоих функциональных генов важно для развития рака.[20]
В 50% случаев тяжелого серозного рака восстановление гомологичной рекомбинационной ДНК является дисфункциональным, как и выемка и FOXM1 сигнальные пути. У них также почти всегда есть мутации p53. Помимо этого, мутации в серозной карциноме высокой степени трудно охарактеризовать, кроме их высокой степени геномная нестабильность. BRCA1 и BRCA2 необходимы для восстановления гомологичной рекомбинации ДНК, и мутации зародышевой линии в этих генах обнаруживаются примерно у 15% людей с раком яичников.[19] Наиболее частыми мутациями BRCA1 и BRCA2 являются мутации сдвига рамки считывания который возник в небольшом население-основатель евреев ашкенази.[20]
Почти 100% редких муцинозных карцином имеют мутации в KRAS и усиление ERBB2 (также известен как Her2 / neu).[19] В целом, 20% случаев рака яичников имеют мутации в Her2 / neu.[17]
Серозные карциномы могут развиться из серозная трубная интраэпителиальная карцинома, а не развиваются спонтанно из ткани яичника. Другие карциномы развиваются из корковые кисты включения, которые представляют собой группы эпителиальных клеток яичников внутри строма.[20]
Диагностика
Экзамен
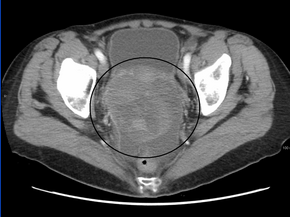
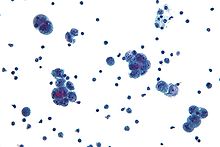
Диагностика рака яичников начинается с физического осмотра (включая тазовое обследование ), анализ крови (для CA-125 а иногда и другие маркеры), и трансвагинальное УЗИ.[17][39] Иногда ректовагинальное обследование используется, чтобы помочь спланировать операцию.[20] Диагноз должен быть подтвержден хирургическим вмешательством для осмотра брюшная полость, брать биопсия (образцы тканей для микроскопический анализ ) и ищите раковые клетки в абдоминальной жидкости. Это помогает определить, есть ли образование яичников. доброкачественный или злокачественный.[17]
Ранние стадии рака яичников (I / II) трудно диагностировать, потому что большинство симптомов неспецифичны и поэтому мало пригодны для диагностики; в результате он редко диагностируется, пока не распространился на более поздние стадии (III / IV).[40] Кроме того, симптомы рака яичников могут быть похожи на синдром раздраженного кишечника. У пациентов, у которых возможна беременность, BHCG уровень можно измерить в процессе диагностики. Сыворотка альфа-фетопротеин, нейрон-специфическая энолаза, и лактатдегидрогеназа можно измерить у молодых девушек и подростков с подозрением на опухоли яичников поскольку у более молодых пациентов больше шансов получить злокачественные опухоли половых клеток.[17][22]
Физикальное обследование, включая тазовое обследование, и УЗИ органов малого таза (трансвагинальное или иное) имеют важное значение для постановки диагноза: физический осмотр может выявить увеличенный обхват живота и / или асцит (жидкость в брюшной полости), а гинекологический осмотр может выявить образование яичников или брюшной полости.[19] Придаточное образование является важным признаком, который часто указывает на рак яичников, особенно если он фиксированный, узелковый, нерегулярный, твердый и / или двусторонний. 13–21% образований придатков вызваны злокачественными новообразованиями; однако есть и другие доброкачественные причины образования придатков, в том числе фолликулярная киста яичника, лейомиома, эндометриоз, внематочная беременность, гидросальпинкс, тубовариальный абсцесс, перекрут яичника, дермоидная киста, цистаденома (серозный или муцинозный), дивертикулярный или же аппендикулярный абсцесс, опухоль нервной оболочки, тазовая почка, мочеточниковый или же дивертикул мочевого пузыря, доброкачественная кистозная мезотелиома брюшины, туберкулез брюшины, или же параовариальная киста. Яичники, которые можно прощупать, также являются признаком рака яичников у женщин в постменопаузе. Другие части медицинского осмотра при подозрении на рак яичников могут включать: обследование груди и пальцевое ректальное исследование. Пальпация надключичный, подмышечный, и паховый лимфатический узел может раскрыть лимфаденопатия, что может указывать на метастазирование. Еще одним индикатором может быть наличие плевральный выпот, что можно отметить на аускультация.[22]
Когда злокачественное новообразование яичников включено в список диагностических возможностей, показано ограниченное количество лабораторных тестов. Обычно проводят общий анализ крови и анализ электролитов сыворотки;[41] когда присутствует рак яичников, эти тесты часто показывают высокое количество тромбоцитов (20–25% людей) и низкий уровень натрия в крови из-за химических сигналов, выделяемых опухолью.[20] Положительный тест на ингибин А и ингибин B может указывать на опухоль гранулезных клеток.[22]
Анализ крови на маркерную молекулу CA-125 полезен для дифференциальной диагностики и последующего наблюдения за заболеванием, но сам по себе он не является эффективным методом скрининга рака яичников на ранней стадии из-за его неприемлемо низкого уровня. чувствительность и специфичность.[41] Уровни СА-125 у людей в пременопаузе более 200 Ед / мл могут указывать на рак яичников, как и любое повышение СА-125 выше 35 Ед / мл у людей в постменопаузе. Уровни CA-125 неточны при раке яичников на ранней стадии, так как полностью половина пациентов с раком яичников I стадии имеют нормальный уровень CA-125.[22][20] CA-125 также может быть повышен при доброкачественных (незлокачественных) состояниях, включая: эндометриоз, беременность, миома матки, менструация, кисты яичников, системная красная волчанка, болезнь печени, воспалительное заболевание кишечника, воспалительные заболевания органов малого таза, и лейомиома.[22][42] HE4 - еще один кандидат на тестирование на рак яичников, хотя он не был тщательно протестирован. Другие опухолевые маркеры рака яичников включают: CA19-9, CA72-4, CA15-3, иммуносупрессивный кислый белок, гаптоглобин-альфа, OVX1, мезотелин, лизофосфатидная кислота, остеопонтин, и фактор роста фибробластов 23.[22]
Использование панелей для анализа крови может помочь в диагностике.[22][41] Панель OVA1 включает CA-125, бета-2 микроглобулин, трансферрин, аполипопротеин A1, и транстиретин. OVA1 выше 5,0 у людей в пременопаузе и 4,4 у людей в постменопаузе указывает на высокий риск рака.[20] Для выявления опухолей стромы полового тяжа используется другой набор лабораторных тестов. Высокий уровень тестостерон или же дегидроэпиандростерона сульфат в сочетании с другими симптомами и высоким уровнем ингибин А и ингибин B может указывать на SCST любого типа.[23]
Текущие исследования ищут способы учитывать опухолевые маркеры. протеомика в сочетании с другими индикаторами заболевания (например, радиологическими данными и / или симптомами) для повышения точности диагностики. Проблема такого подхода состоит в том, что разная распространенность рака яичников означает, что даже тесты с очень высокой чувствительностью и специфичностью по-прежнему будут приводить к ряду ложноположительных результатов, что, в свою очередь, может привести к таким проблемам, как выполнение хирургических процедур, при которых рак не обнаруживается во время операции.[нужна цитата ] Геномика подходы к лечению рака яичников еще не разработаны.[22]
КТ сканирование предпочтительно для оценки степени опухоли в брюшно-тазовой полости, хотя магнитно-резонансная томография также можно использовать.[19] КТ-сканирование также может быть полезно для поиска сальник или дифференциация жидкости от солидной опухоли в брюшной полости, особенно в опухолях с низким потенциалом злокачественности. Однако он может не обнаружить опухоли меньшего размера. Иногда рентгенограмма грудной клетки используется для обнаружения метастазов в груди или плевральный выпот. Другой тест на метастатическое заболевание, хотя он используется нечасто, - это клизма бария, который может показать, вовлечена ли в заболевание ректосигмовидная кишка. Позитронно-эмиссионная томография, сканирование костей, и парацентез имеют ограниченное использование; Фактически, парацентез может вызвать образование метастазов в месте введения иглы и может не дать полезных результатов.[20] Однако парацентез можно использовать в тех случаях, когда нет массы таза и асцит все еще присутствует.[20] Врач, подозревающий рак яичников, также может выполнить маммография или биопсия эндометрия (в случае аномального кровотечения) для оценки возможности злокачественных новообразований груди и эндометрия соответственно. Вагинальное ультразвуковое исследование часто является визуализирующим исследованием первой линии, выполняемым при обнаружении придатков. Некоторые характеристики придаточного образования указывают на злокачественность яичников; они обычно бывают твердыми, неправильными, многоячеистыми и / или большими; и они обычно имеют сосочковые особенности, центральные сосуды и / или нерегулярные внутренние перегородки.[22] Однако SCST не имеет определенных характеристик при рентгенографическом исследовании.[23]
Чтобы окончательно диагностировать рак яичников, требуется хирургическая процедура для осмотра брюшной полости. Это может быть открытая процедура (лапаротомия, разрез через брюшная стенка ) или же хирургия замочной скважины (лапароскопия ). Во время этой процедуры подозрительные ткани удаляются и отправляются на микроскопический анализ. Обычно это одностороннее сальпингоофорэктомия удаление одного пораженного яичника и фаллопиевой трубы. Жидкость из брюшной полости также может быть проанализирована на наличие раковых заболеваний. клетки. При обнаружении рака эту процедуру также можно использовать для определения степени его распространения (что является одной из форм стадия опухоли ).[17]
Оценка риска
Широко признанный метод оценки риска злокачественного рака яичников - это индекс риска злокачественности (RMI), рассчитываемый на основе начального тренировка.[19][43] Обычно считается, что оценка RMI более 200 или 250 указывает на высокий риск рака яичников.[19][22]
RMI рассчитывается как:
- RMI = оценка УЗИ × оценка менопаузы x уровень CA-125 в Ед / мл.[19]
Два метода могут использоваться для определения оценки УЗИ и оценки менопаузы, при этом полученные оценки обозначаются как RMI 1 и RMI 2, соответственно, в зависимости от того, какой метод используется.
| Особенность | RMI 1[19] | RMI 2[22][44] |
|---|---|---|
Ультразвуковые отклонения:
|
|
|
| Оценка менопаузы |
|
|
| CA-125 | Количество в Ед / мл | Количество в Ед / мл |
Еще один метод количественной оценки риска рака яичников - это алгоритм риска рака яичников (ROCA), который отслеживает уровни с течением времени и определяет, достаточно ли они растут, чтобы оправдать трансвагинальное ультразвуковое исследование.[20] Алгоритм риска злокачественных новообразований яичников использует уровни CA-125 и HE4 уровни для расчета риска рака яичников; он может быть более эффективным, чем RMI. Модели IOTA можно использовать для оценки вероятности злокачественной опухоли придатков.[45] Они включают модель риска LR2, расчет риска Простых правил (SRrisk) и модель оценки различных новообразований в придатках (ADNEX), которые можно использовать для оценки риска злокачественного новообразования в придаточном новообразовании на основе его характеристик и факторов риска. Алгоритм QCancer (Ovary) используется для прогнозирования вероятности рака яичников от факторов риска.[22]
Патология
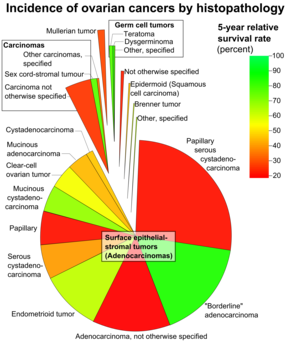
Рак яичников классифицируется в соответствии с микроскопическим видом их структур (гистология или же гистопатология ). Гистология определяет многие аспекты клинического лечения, ведения и прогноз. Макропатология рака яичников очень похожа независимо от гистологического типа: опухоли яичников имеют твердые и кистозные образования.[20] В соответствии с ВИДЯЩИЙ, типы рака яичников у женщин в возрасте 20 лет и старше:[46]
| Процент рак яичников в женщинах возраст 20+ | Процент рак яичников в женщинах возраст 20+ по подразделение | Гистология | Пятилетний RSR |
|---|---|---|---|
| 89.7 | Поверхностная эпителиально-стромальная опухоль (аденокарцинома ) | 54.4 | |
| 26.4 | Папиллярная серозная цистаденокарцинома | 21.0 | |
| 15.9 | Пограничная аденокарцинома (занижено - короткий интервал сбора данных) | 98.2 | |
| 12.6 | Аденокарцинома, если не указано иное | 18.3 | |
| 9.8 | Эндометриоидная опухоль | 70.9 | |
| 5.8 | Серозная цистаденокарцинома | 44.2 | |
| 5.5 | Папиллярный | 21.0 | |
| 4.2 | Муцинозная цистаденокарцинома | 77.7 | |
| 4.0 | Светлоклеточная опухоль яичников | 61.5 | |
| 3.4 | Муцинозная аденокарцинома | 49.1 | |
| 1.3 | Цистаденокарцинома | 50.7 | |
| 5.5 | Карцинома | ||
| 4.1 | Карцинома, не указанная иначе | 26.8 | |
| 1.1 | Половой канатик-стромальная опухоль | 87.8 | |
| 0.3 | Другие уточненные карциномы | 37.3 | |
| 1.7 | Мюллерова опухоль | 29.8 | |
| 1.5 | Опухоль зародышевых клеток | 91.0 | |
| 0.8 | Тератома | 89.1 | |
| 0.5 | Дисгерминома | 96.8 | |
| 0.3 | Другое, указано | 85.1 | |
| 0.6 | Не указано иное | 23.0 | |
| 0.5 | Эпидермоид (плоскоклеточная карцинома ) | 51.3 | |
| 0.2 | Опухоль Бреннера | 67.9 | |
| 0.2 | Другое, указано | 71.7 |
Рак яичников гистологически и генетически делится на тип I или тип II. Раковые опухоли типа I имеют низкую гистологическую степень и включают эндометриоидные, муцинозные и светлоклеточные карциномы. Раковые опухоли типа II имеют более высокий гистологический класс и включают серозную карциному и карциносаркому.[19]
Эпителиальная карцинома
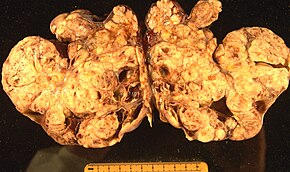
Поверхностная эпителиально-стромальная опухоль, также известный как эпителиальная карцинома яичников, является наиболее распространенным типом рака яичников, составляющим примерно 90% случаев рака яичников. Это включает в себя серозная опухоль, эндометриоидная опухоль, и муцинозный цистаденокарцинома. Реже встречаются злокачественные опухоли Эндометриоид рак яичников, Очистить ячейку рак яичников и опухоль Бреннера (переходно-клеточная карцинома яичника ). Эпителиальный рак яичников развивается из эпителий, слой клеток, покрывающий яичник.[47]
Серозная карцинома
Большинство людей с эпителиальной карциномой яичников, около двух третей, имеют серозная карцинома,[19] хотя эта доля оценивается как 80%.[22][48] Серозная карцинома низкой степени злокачественности менее агрессивна, чем серозная карцинома высокой степени злокачественности, хотя обычно плохо поддается химиотерапии или гормональному лечению.[19] Считается, что серозная карцинома начинается в Фаллопиевых труб.[47] Гистологически серозные аденокарциномы имеют псаммома тела. Серозные аденокарциномы низкой степени злокачественности напоминают эпителий фаллопиевых труб, тогда как серозные аденокарциномы высокой степени злокачественности проявляются анаплазия и ядерная атипия.[20]
В 50% случаев серозные карциномы являются двусторонними, а в 85% случаев на момент постановки диагноза они распространились за пределы яичника. Большинство из них имеют диаметр более 15 см.[48]
Серозная трубная интраэпителиальная карцинома (STIC) в настоящее время признана предшественником большинства так называемых серозных карцином яичников высокой степени злокачественности.[49]STIC характеризуется
- Аномальное окрашивание p53
- Индекс распространения Ki67 более 10%
- Положительный WT1 (для исключения метастазов)[50]
Мелкоклеточная карцинома
Мелкая ячейка Карцинома яичников встречается редко и имеет два основных подтипа: гиперкальциемический и легочный. Обычно это приводит к летальному исходу в течение 2 лет после постановки диагноза. Гиперкальциемическая мелкоклеточная карцинома яичников в подавляющем большинстве случаев поражает людей в возрасте от 20 до 20 лет. высокий уровень кальция в крови, и поражает один яичник. Легочный мелкоклеточный рак яичников обычно поражает оба яичника у пожилых женщин и выглядит так: овсяноклеточный рак легкого.[20]
Первичная карцинома брюшины
Первичные карциномы брюшины развиваются из брюшина, мембрана, покрывающая брюшная полость который имеет то же эмбриональное происхождение, что и яичник. Их часто обсуждают и классифицируют как рак яичников, когда они поражают яичник.[47][51] Они могут развиваться даже после удаления яичников и могут выглядеть как мезотелиома.[20]
Светлоклеточная карцинома
Светлоклеточные карциномы яичников обычно плохо реагируют на химиотерапию и могут быть связаны с эндометриозом.[19] Они составляют примерно 5% всех случаев рака эндометрия. У японских женщин светлоклеточный рак яичников развивается чаще, чем у других групп женщин.[22]
Светлоклеточная аденокарцинома

Светлоклеточные аденокарциномы гистопатологически схожи с другими светлоклеточные карциномы, с чистые клетки и клетки шиповника. Они составляют примерно 5–10% эпителиальных раковых заболеваний яичников и связаны с эндометриозом в полости малого таза. Как правило, они находятся на ранней стадии и поэтому излечиваются хирургическим путем, но передовые светлоклеточные аденокарциномы (примерно 20%) имеют плохой прогноз и часто устойчивы к химиотерапии платиной.[20]
Эндометриоид
Эндометриоидные аденокарциномы составляют примерно 15–20% эпителиального рака яичников. Поскольку эндометриоидные аденокарциномы обычно имеют низкую степень злокачественности, они имеют хороший прогноз. Эти опухоли часто возникают одновременно с эндометриоз или рак эндометрия.[20]
Злокачественная смешанная мюллерова опухоль (карциносаркома)
Смешанные мюллеровы опухоли составляют менее 1% рака яичников. У них есть видимые эпителиальные и мезенхимальные клетки, что имеет тенденцию к плохому прогнозу.[20]
Муцинозный
Муцинозные опухоли включают муцинозную аденокарциному и муцинозную цистаденокарциному.[20]
Муцинозная аденокарцинома
Муцинозные аденокарциномы составляют 5–10% эпителиального рака яичников. Гистологически они похожи на аденокарциномы кишечника или шейки матки и часто являются метастазами аппендикулярный или же рак толстой кишки. Муцинозные аденокарциномы на поздней стадии имеют плохой прогноз, обычно хуже, чем серозные опухоли, и часто устойчивы к химиотерапии платиной, хотя встречаются редко.[20]
Псевдомиксома брюшины
Псевдомиксома брюшины относится к скоплению инкапсулированного слизистого или гелеобразного материала в брюшно-тазовой полости, которое очень редко вызывается первичной муцинозной опухолью яичников. Чаще всего это связано с метастазами рака кишечника в яичники.[20]
Недифференцированный эпителиальный
Недифференцированные раковые образования - те, по которым невозможно определить тип клеток - составляют около 10% эпителиального рака яичников и имеют сравнительно плохой прогноз.[20][47] При исследовании под микроскопом в этих опухолях обнаруживаются очень аномальные клетки, которые располагаются в виде скоплений или пластин. Обычно внутри опухоли видны скопления серозных клеток.[20]
Злокачественная опухоль Бреннера
Злокачественные опухоли Бреннера встречаются редко. Гистологически они имеют плотную фиброзную строму с участками переходного эпителия и некоторую плоскоклеточную дифференцировку. Чтобы быть классифицированным как злокачественная опухоль Бреннера, она должна иметь очаги опухоли Бреннера и переходно-клеточную карциному. Компонент переходно-клеточной карциномы обычно плохо дифференцирован и напоминает рак мочевыводящих путей.[20]
Переходно-клеточная карцинома
Переходно-клеточные карциномы составляют менее 5% случаев рака яичников. Гистологически они похожи на карцинома мочевого пузыря. Прогноз промежуточный - лучше, чем у большинства эпителиальных опухолей, но хуже, чем у злокачественных опухолей Бреннера.[20]
Половой канатик-стромальная опухоль
Половой канатик-стромальная опухоль, включая эстроген -производство гранулезно-клеточная опухоль, доброкачественный текома и вирилизирующий Опухоль из клеток Сертоли-Лейдига или же арренобластома, составляет 7% случаев рака яичников. Чаще всего они возникают у женщин в возрасте от 50 до 69 лет, но могут встречаться у женщин любого возраста, включая молодых девушек. Они обычно не агрессивны и обычно односторонние;[17] поэтому их обычно лечат только хирургическим путем. Опухоли стромы полового канатика являются основными опухолями яичников, продуцирующими гормоны.[23]
Несколько разных ячеек из мезенхима может вызвать опухоли полового канатика или стромы. К ним относятся фибробласты и эндокринные клетки. Симптомы опухоли полового канатика или стромы яичников могут отличаться от других типов рака яичников. Общие признаки и симптомы включают: перекрут яичника, кровоизлияние от или разрыва опухоли, образования в брюшной полости и гормонального сбоя. У детей изосексуальное преждевременное развитие псевдопубертата может возникать при опухолях гранулезных клеток, поскольку они продуцируют эстроген. Эти опухоли вызывают нарушения менструального цикла (чрезмерное кровотечение, нечастые менструации, или же нет менструации ) или постменопаузальное кровотечение. Поскольку эти опухоли производят эстроген, они могут вызывать или возникать одновременно с рак эндометрия или же рак молочной железы. Другие опухоли полового канатика / стромы имеют отчетливые симптомы. Опухоли из клеток Сертоли-Лейдига вызывают вирилизация и чрезмерный рост волос из-за производства тестостерон и андростендион, что также может вызвать синдром Кушинга в редких случаях. Также возникают опухоли стромы полового канатика, которые не вызывают гормонального дисбаланса, в том числе доброкачественные фибромы, которые вызывают асцит и гидроторакс.[17] При опухолях половых клеток опухоли полового канатика и стромы являются наиболее распространенным раком яичников, диагностируемым у женщин до 20 лет.[23]
Гранулезно-клеточная опухоль
Опухоли из гранулезных клеток являются наиболее распространенными опухолями стромы полового канатика, составляющими 70% случаев, и делятся на два гистологических подтипа: опухоли из гранулезных клеток взрослых, которые развиваются у женщин старше 50 лет, и ювенильные гранулезные опухоли, которые развиваются до полового созревания или до 30 лет. Оба развиваются в фолликул яичника из популяции клеток, которые окружают половые клетки.[23]
Взрослая гранулезно-клеточная опухоль
Опухоли из гранулезных клеток у взрослых характеризуются более поздним началом (30+ лет, в среднем 50). Эти опухоли вырабатывают высокий уровень эстрогена, что вызывает его характерные симптомы: менометроррагия; гиперплазия эндометрия; нежный, увеличенная грудь; постменопаузальное кровотечение; и вторичная аменорея. Масса опухоли может вызывать другие симптомы, включая боль в животе и вздутие живота, или симптомы, похожие на внематочная беременность если опухоль кровоточит и разрывается.[23]
Ювенильная гранулезно-клеточная опухоль
Опухоль из клеток Сертоли-Лейдига
Опухоли Сертоли-Лейдига чаще всего встречаются у женщин в возрасте до 30 лет и особенно распространены до полового созревания.[23]
Склерозирующие стромальные опухоли
Склерозирующие стромальные опухоли обычно возникают у девочек до полового созревания или у женщин в возрасте до 30 лет.[23]
Опухоль зародышевых клеток
Опухоли половых клеток яичника развиваются из яичника. стволовые клетки.[47] Опухоль зародышевых клеток составляет около 30% опухолей яичников, но только 5% случаев рака яичников, потому что большинство опухолей половых клеток являются тератомы и большинство тератом доброкачественные. Злокачественные тератомы, как правило, возникают у пожилых женщин, когда один из зародышевых листков опухоли превращается в плоскоклеточная карцинома.[17] Опухоли зародышевых клеток, как правило, возникают у молодых женщин (20–30 лет) и девочек, составляя 70% случаев рака яичников в этой возрастной группе.[24] Опухоли половых клеток могут включать дисгерминомы, тератомы, опухоли желточного мешка / опухоли энтодермального синуса и хориокарциномы, если они возникают в яичнике. Некоторые опухоли половых клеток имеют изохромосома 12, где одно плечо хромосомы 12 удалено и заменено дубликатом другого.[17] Большинство злокачественных опухолей зародышевых клеток имеют лучший прогноз, чем другие подтипы, и более чувствительны к химиотерапии. На момент постановки диагноза они, скорее всего, будут стадией I.[23] В целом они метастазируют чаще, чем эпителиальный рак яичников. Кроме того, используемые маркеры рака зависят от типа опухоли: хориокарциномы контролируются бета-ХГЧ и опухоли энтодермального синуса с альфа-фетопротеин.[17]
Опухоли зародышевых клеток обычно обнаруживаются, когда они становятся большими пальпируемыми массами. Однако, как и опухоли полового канатика, они могут вызывать перекрут яичников или кровоизлияние, а у детей - преждевременное половое созревание изосексуалов. Они часто метастазируют в близлежащие лимфатические узлы, особенно в парааортальные и тазовые лимфатические узлы.[17] Наиболее частый симптом опухолей половых клеток: подострая боль в животе вызвано кровотечением из опухоли, некротизирующий, или растягивая капсула яичника. Если опухоль разрывается, вызывает сильное кровотечение или перекручивает яичник, это может вызвать острая боль в животе, который встречается менее чем у 10% людей с опухолями половых клеток. Они также могут выделять гормоны, которые изменяют менструальный цикл. В 25% опухолей половых клеток рак обнаруживается во время плановое обследование и не вызывает симптомов.[23]
Диагностика опухолей половых клеток может быть затруднена из-за нормального менструального цикла и половое созревание может вызывать боль и симптомы со стороны малого таза, и молодая женщина может даже полагать, что эти симптомы связаны с беременностью, и не обращаться за лечением из-за стигмы подростковая беременность. Анализы крови на альфа-фетопротеин, кариотип, хорионический гонадотропин человека и функция печени используются для диагностики опухоли половых клеток и потенциально сопутствующей дисгенезии гонад. Первоначально зародышевую опухоль можно принять за доброкачественную. киста яичника.[23]
Дисгерминома
Дисгерминома составляет 35% случаев рака яичников у молодых женщин и является наиболее вероятной опухолью из половых клеток, способной метастазировать в лимфатические узлы; узловые метастазы встречаются в 25–30% случаев.[24][23] Эти опухоли могут иметь мутации в то КОМПЛЕКТ ген, мутация, известная своей ролью в опухоль стромы желудочно-кишечного тракта. Люди с XY-кариотипом и яичниками (гонадная дисгенезия ) или кариотип X, 0 и яичники (Синдром Тернера ), у которых развивается односторонняя дисгерминома, подвержены риску гонадобластома в другом яичнике, и в этом случае оба яичника обычно удаляются при обнаружении односторонней дисгерминомы, чтобы избежать риска возникновения другой злокачественной опухоли. Гонадобластомы у людей с синдромом Свайера или Тернера становятся злокачественными примерно в 40% случаев. Однако в целом дисгерминомы бывают двусторонними в 10–20% случаев.[17][23]
Они состоят из клеток, которые не могут различать далее и развиваются непосредственно из половых клеток или из гонадобластом. Дисгерминомы содержат синцитиотрофобласты примерно в 5% случаев и, следовательно, может вызвать повышение уровня ХГЧ. На первый взгляд дисгерминомы обычно имеют цвет от розового до коричневого, имеют несколько долей и твердые. Микроскопически они идентичны семиномы и очень близко к эмбриональные первичные половые клетки, имеющий большие, многогранные, округлые чистые клетки. Ядра однородные, круглые или квадратные с выступающими ядрышки и цитоплазма имеет высокий уровень гликоген. Воспаление - еще один видный гистологический признак дисгерминомы.[23]
Хориокарцинома
Хориокарцинома может возникать как первичная опухоль яичников, развивающаяся из половых клеток, хотя обычно это гестационное заболевание, которое метастазирует в яичник. Первичная хориокарцинома яичников имеет неблагоприятный прогноз и может протекать без беременности. Они производят высокий уровень ХГЧ и могут вызывать раннее половое созревание у детей или менометроррагия (нерегулярные, обильные менструации) после менархе.[23]
Незрелая (солидная) тератома
Незрелые или солидные тератомы являются наиболее частым типом опухолей половых клеток яичников, составляя 40–50% случаев. Тератомы характеризуются наличием дезорганизованных тканей, возникающих из всех трех эмбриональных клеток. ростковые отростки: эктодерма, мезодерма, и энтодерма; незрелые тератомы также имеют недифференцированные стволовые клетки которые делают их более злокачественными, чем зрелые тератомы (дермоидные кисты). Различные ткани видны при крупной патологии и часто включают кости, хрящи, волосы, слизь, или же кожный жир, но эти ткани не видны снаружи, они представляют собой твердую массу с долями и кистами. Гистологически они имеют большое количество нейроэктодерма организованы в листы и трубочки вместе с глия; количество нервной ткани определяет гистологический класс. Незрелые тератомы обычно поражают только один яичник (в 10% случаев встречаются дермоидные кисты) и обычно метастазируют по брюшине. Они также могут вызывать разрастание имплантатов зрелой тератомы по всей брюшной полости при заболевании, называемом синдром растущей тератомы; они обычно доброкачественные, но будут продолжать расти во время химиотерапии и часто требуют дальнейшего хирургического вмешательства. В отличие от зрелых тератом незрелые тератомы образуют множество спайки, что снижает вероятность перекрута яичника. Специфического маркера незрелых тератом нет, но карциноэмбриональный антиген (CEA), CA-125, CA19-9 или AFP иногда могут указывать на незрелую тератому.[23]
Тератомы стадии I составляют большинство (75%) случаев и имеют лучший прогноз: 98% пациентов выживают 5 лет; если опухоль стадии I также относится к степени 1, ее можно лечить только односторонним хирургическим вмешательством. Опухоли стадии II - IV составляют оставшуюся четверть случаев и имеют худший прогноз: 73–88% пациентов выживают 5 лет.[23]
Зрелая тератома (дермоидная киста)
Зрелые тератомы или дермоидные кисты - это редкие опухоли, состоящие в основном из доброкачественной ткани, которые развиваются после менопаузы. Опухоли состоят из дезорганизованной ткани с узелками злокачественной ткани, которые могут быть разных типов. Наиболее частым злокачественным новообразованием является плоскоклеточная карцинома, но аденокарцинома, базально-клеточная карцинома, карциноидная опухоль, нейроэктодермальная опухоль, злокачественная меланома, саркома, сальная опухоль, и зоб яичников также может быть частью дермоидной кисты. Их лечат хирургическим вмешательством и адъювантной химиотерапией платиной или облучением.[23]
Опухоль желточного мешка / опухоль энтодермального синуса
Желточный мешок опухоли, ранее называемые опухолями энтодермального синуса, составляют примерно 10-20% злокачественных новообразований половых клеток яичников и имеют худший прогноз из всех опухоли зародышевых клеток яичников. Они возникают как до менархе (в одной трети случаев), так и после менархе (в остальных двух третях случаев). У половины людей опухоли желточного мешка диагностируются на стадии I. Как правило, они односторонние, вплоть до метастазирования, которое происходит в брюшной полости и через кровоток в легкие. Опухоли желточного мешка быстро растут и легко рецидивируют, и после рецидива их нелегко лечить. Опухоли желточного мешка стадии I хорошо поддаются лечению, при этом 5-летняя выживаемость без признаков заболевания составляет 93%, но опухоли стадии II-IV менее поддаются лечению, с показателем выживаемости 64–91%.[23]
Они выглядят твердыми, рыхлыми и желтыми с некротическими и геморрагическими участками. Они также часто содержат кисты, которые могут переродиться или разорваться. Гистологически опухоли желточного мешка характеризуются наличием Тела Шиллера-Дюваля (которые патогномоничны для опухолей желточного мешка) и сетчатый узор. Опухоли желточного мешка обычно выделяют альфа-фетопротеин и может быть иммуногистохимически окрашены на предмет его наличия; уровень альфа-фетопротеина в крови является полезным маркером рецидива.[23]
Эмбриональная карцинома
Эмбриональные карциномы - редкий тип опухолей, обычно обнаруживаемый в смешанных опухолях, - развиваются непосредственно из половых клеток, но не дифференцируются окончательно; в редких случаях они могут развиваться в дисгенетических гонадах. В дальнейшем они могут развиться во множество других новообразований, включая хориокарциному, опухоль желточного мешка и тератому. Они возникают у более молодых людей, средний возраст на момент постановки диагноза составляет 14 лет, и секретируют как альфа-фетопротеин (в 75% случаев), так и ХГЧ.[23]
Гистологически эмбриональная карцинома похожа на эмбриональный диск, состоящий из эпителия, анапластический клетки в неорганизованных листах с железистыми пространствами и сосочковыми структурами.[23]
Полиэмбриома
Полиэмбриомы, самая незрелая форма тератомы и очень редкие опухоли яичников, гистологически характеризуются наличием нескольких эмбрион -подобные тела со структурой, напоминающей зародышевый диск, желточный мешок, и амниотической мешок. Гигантские клетки синцитиотрофобласта также встречаются при полиэмбриомах.[23]
Плоскоклеточная карцинома
Первичная плоскоклеточная карцинома яичников встречается редко и имеет плохой прогноз на поздней стадии. Чаще плоскоклеточный рак яичников представляет собой цервикальные метастазы, области дифференцировки в эндометриоидной опухоли или происходит из зрелой тератомы.[20]
Смешанные опухоли
Смешанные опухоли содержат элементы более чем одного из вышеуказанных классов гистологии опухолей. Чтобы относиться к смешанной опухоли, второстепенный тип должен составлять более 10% опухоли.[22] Хотя смешанные карциномы могут иметь любую комбинацию типов клеток, смешанные злокачественные опухоли яичников обычно являются серозными / эндометриоидными или светлоклеточными / эндометриоидными.[20] Смешанные зародышевые опухоли составляют примерно 25–30% всех половых клеток рака яичников с комбинациями дисгерминомы, опухоли желточного мешка и / или незрелой тератомы. Прогноз и лечение зависят от типов клеток.[23]
Вторичный рак яичников
Рак яичников также может быть вторичным раком, результатом метастаз от первичного рака в другом месте тела.[17] Около 7% случаев рака яичников возникают из-за метастазов, а остальные - первичного рака.[нужна цитата ] Общие первичные раковые образования: рак молочной железы, рак толстой кишки, рак аппендикса, и рак желудка (первичный рак желудка, метастазирующий в яичник, называется Опухоли Крукенберга ).[17] Опухоли Крукенберга содержат клетки перстневого кольца и муцинозные клетки.[20] Рак эндометрия и лимфомы также могут метастазировать в яичник.[48]
Пограничные опухоли
Яичников пограничные опухоли, иногда называемые опухолями яичников с низким злокачественным потенциалом (LMP), имеют как доброкачественные, так и злокачественные признаки.[20] Опухоли LMP составляют примерно 10-15% всех опухолей яичников.[22][47] Они развиваются раньше, чем эпителиальный рак яичников, примерно в возрасте 40–49 лет. Обычно у них нет обширного вторжения; 10% опухолей LMP имеют области микроинвазии стромы (<3 мм, <5% опухоли). Опухоли LMP имеют другие аномальные особенности, в том числе повышенный митоз, изменения в размере клетки или размере ядра, аномальные ядра, стратификация клеток и небольшие выступы на ячейках (сосочковые выступы). Серозные и / или муцинозные характеристики можно увидеть при гистологическом исследовании, а серозная гистология составляет подавляющее большинство распространенных опухолей LMP. Более 80% опухолей LMP относятся к стадии I; 15% относятся к стадии II и III и менее 5% - к стадии IV.[20] Имплантаты опухолей LMP часто бывают неинвазивными.[47]
Постановка
Рак яичников ставят с помощью FIGO система стадирования и использует информацию, полученную после операции, которая может включать в себя абдоминальная гистерэктомия через срединная лапаротомия, удаление (обычно) обоих яичников и фаллопиевых труб, (обычно) сальник, тазовые (перитонеальные) промывания, оценка забрюшинные лимфатические узлы (в том числе тазовый и парааортальные лимфатические узлы ), аппендэктомия при подозрении на муцинозные опухоли и биопсии таза / брюшины для цитопатология.[19][17][22][52] Около 30% случаев рака яичников, которые, по-видимому, ограничиваются яичником, имеют микроскопические метастазы, поэтому даже рак I стадии должен быть полностью поставлен на стадию.[17] В 22% случаев рака, предположительно относящихся к I стадии, наблюдаются лимфатические метастазы.[22] Этап AJCC такой же, как этап FIGO. Система стадирования AJCC описывает степень первичной опухоли (T), отсутствие или наличие метастаз поблизости лимфатический узел (N) и отсутствие или наличие отдаленных метастазов (M).[53] Наиболее частая стадия диагностики - стадия IIIc, на которую ставится более 70% диагнозов.[17]
FIGO
| Этап | Описание | |||
|---|---|---|---|---|
| я | Рак полностью ограничивается яичником | |||
| Я | вовлекается один яичник, капсула не повреждена, опухоли на поверхности яичника нет, смывы отрицательные | |||
| IB | вовлекает оба яичника; капсула цела; на поверхности яичников опухоли нет; отрицательные стирки | |||
| IC | опухоль затрагивает один или оба яичника | |||
| IC1 | хирургический разлив | |||
| IC2 | разрыв капсулы или опухоль на поверхности яичника | |||
| IC3 | положительный асцит или промывания | |||
| II | тазовое расширение опухоли (должно быть ограничено тазом) или первичная перитонеальная опухоль, вовлекающая один или оба яичника | |||
| IIA | опухоль, обнаруженная на матке или фаллопиевых трубах | |||
| МИБ | опухоль в другом месте таза | |||
| III | рак, обнаруженный вне таза или в забрюшинных лимфатических узлах, поражает один или оба яичника | |||
| IIIA | метастазы в забрюшинных лимфатических узлах или микроскопические метастазы в экстратазную область | |||
| IIIA1 | метастазы в забрюшинные лимфатические узлы | |||
| IIIA1 (i) | метастаз диаметром менее 10 мм | |||
| IIIA1 (ii) | метастаз более 10 мм в диаметре | |||
| IIIA2 | микроскопические метастазы в брюшину независимо от статуса забрюшинных лимфатических узлов | |||
| IIIB | метастазы в брюшину диаметром не более 2 см, независимо от статуса забрюшинных лимфатических узлов; или метастаз в капсулу печени или селезенки | |||
| IIIC | метастазы в брюшину диаметром более 2 см, независимо от статуса забрюшинных лимфатических узлов; или метастаз в капсулу печени или селезенки | |||
| IV | отдаленные метастазы (то есть за пределами брюшины) | |||
| IVA | плевральный выпот, содержащий раковые клетки | |||
| IVB | метастазы в отдаленные органы (включая паренхиму селезенки или печени) или метастазы в паховые и экстраабдоминальные лимфатические узлы |

Рак яичников 1 стадии
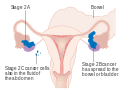
Рак яичников 2 стадия
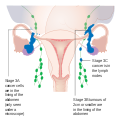
Рак яичников 3 стадии

Рак яичников 4 стадии
AJCC / TNM
Система стадирования AJCC / TNM указывает, где опухоль развивалась, распространилась на лимфатические узлы и метастазы.[22]
| Этап | Описание | ||
|---|---|---|---|
| Т | Первичная опухоль | ||
| Tx | Не подлежит оценке | ||
| T0 | Нет доказательств | ||
| Т1 | Опухоль ограничена яичником / яичниками | ||
| T1a | Один яичник с интактной капсулой, без поверхностной опухоли и отрицательным асцитом / смывом брюшины | ||
| T1b | Оба яичника с интактными капсулами, без поверхностной опухоли и отрицательным асцитом / смывом брюшины | ||
| T1c | Один или оба яичника с разрывом капсулы или капсулы, поверхностная опухоль, положительный асцит / перитонеальные смывы | ||
| Т2 | Опухоль яичников и таза (расширение или имплантация) | ||
| T2a | Распространение в матку или фаллопиевы трубы, отрицательный асцит / перитонеальные смывы | ||
| T2b | Распространение в других тканях малого таза, отрицательный асцит / смывы брюшины | ||
| T2c | Распространение на любые ткани малого таза, положительный асцит / перитонеальные смывы | ||
| Т3 | Опухоль находится в яичниках и метастазирует за пределы таза в брюшину (включая капсулу печени). | ||
| T3a | Микроскопический метастаз | ||
| T3b | Макроскопические метастазы диаметром менее 2 см | ||
| T3c | Макроскопические метастазы диаметром более 2 см | ||
| N | Метастазы в регионарные лимфатические узлы | ||
| Nx | Не подлежит оценке | ||
| N0 | Нет метастазов | ||
| N1 | Наличие метастазов | ||
| M | Отдаленные метастазы | ||
| M0 | Нет метастазов | ||
| M1 | Наличие метастазов (за исключением капсулы печени, включая паренхиму печени и цитологически подтвержденный плевральный выпот) |
Этапы AJCC / TNM можно соотнести с этапами FIGO:[22]
| FIGO | Т | N | M |
|---|---|---|---|
| я | Т1 | N0 | M0 |
| Я | T1a | N0 | M0 |
| IB | T1b | N0 | M0 |
| IC | T1c | N0 | M0 |
| II | Т2 | N0 | M0 |
| IIA | T2a | N0 | M0 |
| МИБ | T2b | N0 | M0 |
| IIC | T2c | N0 | M0 |
| III | Т3 | N0 | M0 |
| IIIA | T3a | N0 | M0 |
| IIIB | T3b | N0 | M0 |
| IIIC | T3c | N0 / N1 | M0 |
| IV | Любой | Любой | M1 |
Оценка
Опухоли 1-й степени имеют хорошо дифференцированные клетки (очень похожи на нормальные ткани) и имеют наилучший прогноз. Опухоли 2 степени также называют умеренно хорошо дифференцированными, и они состоят из клеток, напоминающих нормальную ткань. Опухоли 3-й степени имеют наихудший прогноз, а их клетки аномальные, называемые плохо дифференцированными.[54]
Метастазы при раке яичников очень распространены в брюшной полости и возникают в результате отшелушивания, когда раковые клетки прорываются через капсулу яичника и могут свободно перемещаться по брюшной полости. Метастазы рака яичников обычно растут на поверхности органов, а не внутри; они также часто встречаются на сальнике и слизистой оболочке брюшины. Раковые клетки также могут перемещаться через лимфатическая система и метастазируют в лимфатические узлы, связанные с яичниками через кровеносные сосуды; то есть лимфатические узлы вдоль инфундибуло-тазовая связка, то широкой связки, а круглая связка. Наиболее часто затрагиваемые группы включают парааортальный, гипогастральный, наружная подвздошная кость, обтуратор, и паховые лимфатические узлы. Обычно рак яичников не метастазирует в печень, легкие, мозг или почки, если только это не рецидивирующее заболевание; это отличает рак яичников от многих других форм рака.[20]
Скрининг
Не существует простого и надежного способа проверить наличие рака яичников у женщин, у которых нет никаких признаков или симптомов. Скрининг не рекомендуется женщинам, относящимся к группе среднего риска, поскольку фактические данные не подтверждают снижение смертности, а высокий уровень ложноположительных результатов тестов может привести к ненужному хирургическому вмешательству, которое сопровождается собственными рисками.[15] В мазок из шейки матки не проверяет на рак яичников.[18]
Рак яичников обычно пальпируется только на поздних стадиях.[20] Скрининг не рекомендуется использовать CA-125 измерения, HE4 уровни, УЗИ или пальпация придатков у женщин из группы среднего риска. Риск развития рака яичников у людей с генетическими факторами может быть снижен. Те, у кого есть генетическая предрасположенность, могут получить пользу от скрининга. Эта группа высокого риска выиграла благодаря более раннему выявлению.[19][17][55]
Рак яичников имеет низкую распространенность даже в группе женщин высокого риска в возрасте от 50 до 60 лет (примерно одна в 2000 году), и скрининг женщин со средним риском с большей вероятностью даст неоднозначные результаты, чем обнаружение проблемы, требующей лечения. . Поскольку неоднозначные результаты более вероятны, чем обнаружение поддающейся лечению проблемы, и поскольку обычным ответом на неоднозначные результаты является инвазивное вмешательство, у женщин среднего риска потенциальный вред прохождения скрининга без показаний перевешивает потенциальные преимущества. Цель скрининга - диагностировать рак яичников на ранней стадии, когда вероятность успешного лечения выше.[17][55]
Скрининг с трансвагинальное УЗИ, тазовое обследование и определение уровня CA-125 можно использовать вместо профилактического хирургического вмешательства у женщин с мутациями BRCA1 или BRCA2. Эта стратегия показала определенный успех.[20]
Профилактика
Люди с высоким генетическим риском рака яичников могут рассматривать хирургическое удаление яичников как профилактическую меру. Часто это делают после завершения детородного возраста. Это снижает вероятность развития как рака груди (примерно на 50%), так и рака яичников (примерно на 96%) у людей из группы высокого риска. Женщины с BRCA при мутациях генов обычно одновременно удаляют фаллопиевы трубы (сальпингоофорэктомия), поскольку они также имеют повышенный риск Рак фаллопиевых труб. Однако эти статистические данные могут переоценить снижение риска из-за того, как они были изучены.[17][55]
Людей со значительным семейным анамнезом рака яичников часто направляют в генетический консультант чтобы увидеть, будет ли полезно тестирование на мутации BRCA.[20] Использование оральных контрацептивов, отсутствие «периодов» во время менструального цикла и перевязка маточных труб снижают риск.[56]Во время лечения бесплодия может возникнуть связь между развитием рака яичников и стимуляцией яичников. Эндометриоз был связан с раком яичников. Папилломавирусная инфекция, курение и тальк не были идентифицированы как повышающие риск развития рака яичников.[19]
Управление
После определения наличия рака яичников, маточной трубы или первичного рака брюшины гинеколог-онколог (врач, обученный лечению рака репродуктивной системы женщины) назначает лечение. Онколог-гинеколог может провести операцию и назначить химиотерапию женщинам с раком яичников. Разработан план лечения.[57]
Лечение обычно включает хирургия и химиотерапия, и иногда лучевая терапия независимо от подтипа рака яичников.[47][58] Хирургического лечения может быть достаточно при хорошо дифференцированных злокачественных опухолях, ограниченных яичником. При более агрессивных опухолях яичника может потребоваться дополнительная химиотерапия. Для пациентов с запущенным заболеванием стандартным является сочетание хирургического вмешательства с режимом комбинированной химиотерапии. Пограничные опухоли даже после распространения за пределы яичника хорошо поддаются хирургическому лечению, а химиотерапия не считается полезной.[59] Вторая операция и поддерживающая химиотерапия не показали, что приносят пользу.[20]
Хирургия
Хирургия является стандартом лечения на протяжении десятилетий и может потребоваться при получении образца для диагноз. Операция зависит от степени инвазии рака в другие ткани на момент его диагностики. Эта степень рака описывается путем присвоения ему стадии, предполагаемого типа и степени рака. Хирург-гинеколог может удалить один (односторонняя овариэктомия) или оба яичника (двусторонняя овариэктомия). Фаллопиевы трубы (сальпингэктомия), матка (гистерэктомия) и сальник (оментэктомия) также может быть удалена. Обычно все эти органы удаляются.[60]
При низком уровне злокачественности одностороннего рака стадии IA удаляются только пораженный яичник (который должен быть неразорванным) и фаллопиевы трубы. Это можно сделать особенно молодыми людьми, которые хотят сохранить свою фертильность. Однако существует риск микроскопических метастазов, поэтому необходимо определить стадию.[19] Если обнаружены какие-либо метастазы, необходима вторая операция по удалению оставшихся яичников и матки.[59] Транексамовая кислота можно вводить до операции, чтобы уменьшить потребность в переливании крови из-за потери крови во время операции.[22]
Если опухоль у женщины в пременопаузе определяется как опухоль с низким потенциалом злокачественности во время операции, и это явно рак I стадии, удаляется только пораженный яичник. Для женщин в постменопаузе с опухолями с низким потенциалом злокачественности гистерэктомия с двусторонней сальпингоофорэктомией по-прежнему является предпочтительным вариантом. Во время постановки аппендикс можно исследовать или удалить. Это особенно важно при муцинозных опухолях.[20] У детей или подростков с раком яичников хирурги обычно пытаются сохранить один яичник, чтобы можно было завершить операцию. половое созревание, но если рак распространился, это не всегда возможно. В частности, дисгерминомы поражают оба яичника: 8–15% дисгермином присутствуют в обоих яичниках.[24] Людей с низкодифференцированными (хорошо дифференцированными) опухолями обычно лечат только хирургическим путем.[17] который часто бывает лечебным.[47] В общем, опухоли половых клеток можно лечить с помощью одностороннего хирургического вмешательства, если только рак не является широко распространенным или фертильность не является фактором.[23] Исследования показывают, что у женщин с прогрессирующим эпителиальным раком яичников с хирургической стадией (стадии III и IV) должны быть предприняты все попытки для достижения полной циторедукции (хирургические усилия по удалению основной части опухоли).[61]
При запущенных формах рака, когда полное удаление невозможно, как можно больше опухоли удаляется с помощью процедуры, называемой разрушение хирургия. Эта операция не всегда бывает успешной и с меньшей вероятностью будет успешной у женщин с обширными метастазами в брюшину, заболеванием IV стадии, раком в брюшине. поперечная трещина печени, брыжейка, или диафрагма, и большие участки асцита. Операция по удалению массы тела обычно проводится только один раз.[19] Компьютерная томография (КТ брюшной полости) часто используется для оценки возможности первичного хирургического удаления опухоли, но доказательства с низкой степенью достоверности также предполагают, что ПЭТ / КТ с фтордезоксиглюкозой-18 (ФДГ) и МРТ могут быть полезны в качестве дополнения для оценки макроскопического неполного удаления опухоли.[62] Более полное удаление массы тела связано с лучшими результатами: женщины без макроскопических признаков заболевания после удаления массы тела имеют среднюю выживаемость 39 месяцев по сравнению с 17 месяцами при менее полной операции.[17] Удаляя метастазы, удаляются многие клетки, устойчивые к химиотерапии, а также удаляются любые скопления умерших клеток. Это позволяет химиотерапии лучше воздействовать на оставшиеся раковые клетки, которые с большей вероятностью будут быстрорастущими и, следовательно, химиочувствительными.[20]
Другой используемый протокол - интервальная операция по уменьшению объема, при которой проводится неоадъювантная химиотерапия, выполняется операция по уменьшению объема и химиотерапия заканчивается после этого.[59] Хотя никаких окончательных исследований не было завершено, показано, что оно приблизительно эквивалентно первичной операции по удалению опухоли с точки зрения выживаемости и показывает несколько более низкую заболеваемость.[20]
Есть несколько различных хирургических процедур, которые можно использовать для лечения рака яичников. При раке I и II стадии может использоваться лапараскопическая операция («замочная скважина»), но метастазы могут не обнаруживаться. При запущенном раке лапароскопия не используется, поскольку для удаления метастазов требуется доступ ко всей брюшной полости. В зависимости от степени рака процедуры могут включать двустороннюю сальпингоофорэктомию, биопсию брюшины и лимфатической системы брюшной полости, оментэктомия, спленэктомия, резекция кишечника, удаление или резекция диафрагмы, аппендэктомия, или даже задний экзентерация таза.[20]
Чтобы полностью диагностировать рак яичников, лимфаденэктомия могут быть включены в операцию, но при этом не может быть значительного увеличения выживаемости.[19] Это особенно важно при опухолях половых клеток, поскольку они часто метастазируют в близлежащие лимфатические узлы.[17]
Если рак яичников рецидивирует, вторичная операция иногда является вариантом лечения. Это зависит от того, насколько легко можно удалить опухоль, сколько жидкости накопилось в брюшной полости и от общего состояния здоровья.[19] Эффективность этой операции зависит от хирургической техники, полноты циторедукции и степени заболевания.[63]. Это также может быть полезно для людей, которым первая операция была сделана врачом общего профиля, и при эпителиальном раке яичников.[22] Вторичная хирургия может быть эффективной при дисгерминомах и незрелых тератомах.[23] Данные свидетельствуют о том, что хирургическое вмешательство при рецидивирующем эпителиальном раке яичников может быть связано с продлением жизни у некоторых женщин с болезнью, чувствительной к платине.[64]
Основным побочным эффектом овариэктомии у молодых женщин является раннее менопауза, что может вызвать остеопороз. После операции можно рассмотреть возможность заместительной гормональной терапии, особенно у молодых женщин. Эта терапия может состоять из комбинации эстрогена и прогестерона или одного эстрогена. Только эстроген безопасен после гистерэктомии; когда матка все еще присутствует, беспрепятственный эстроген резко повышает риск рак эндометрия.[19] Терапия эстрогенами после операции не меняет выживаемость.[22] Людей, перенесших операцию по поводу рака яичников, обычно впоследствии госпитализируют на 3–4 дня и около месяца проводят дома на восстановлении.[65] Наилучшие результаты хирургических вмешательств достигаются в больницах, в которых проводится большое количество операций по поводу рака яичников.[20]
Неясно, если лапароскопия или же лапаротомия лучше или хуже при раке яичников I стадии по FIGO.[66] Также нет очевидной разницы между тотальной абдоминальной гистерэктомией и супрацервикальной гистерэктомией при запущенных формах рака. Примерно 2,8% людей, перенесших первую операцию по поводу запущенного рака яичников, умирают в течение двух недель после операции (2,8% периоперационная смертность ставка).[22] Более агрессивные операции связаны с лучшими результатами при запущенном (III или IV стадия) раке яичников.[20]
Химиотерапия
Химиотерапия был генералом стандарт заботы для рака яичников в течение десятилетий, хотя и с различными протоколами. Химиотерапия используется после операции для лечения любого остаточного заболевания, если это необходимо. В некоторых случаях может быть причина сначала провести химиотерапию, а затем операцию. Это называется «неоадъювантной химиотерапией» и является обычным явлением, когда опухоль не может быть полностью удалена или оптимально удалена хирургическим путем. Хотя не было доказано, что он увеличивает выживаемость, он может снизить риск осложнений после операции. Если выполняется односторонняя сальпингоофорэктомия или другая операция, может быть назначена дополнительная химиотерапия, называемая «адъювантной химиотерапией».[19][22] Адъювантная химиотерапия используется при раке 1 стадии, как правило, если опухоль имеет высокий гистологический класс (3 степень) или самую высокую подстадию (стадия 1c), при условии, что стадия рака оптимальна во время операции.[22][59] Бевацизумаб может использоваться в качестве адъювантной химиотерапии, если опухоль полностью не удалена во время операции или если рак находится на стадии IV; он может увеличивать выживаемость без прогрессирования заболевания, но не было показано, что он увеличивает общую выживаемость.[22] Химиотерапия лечит примерно 20% запущенных форм рака яичников;[20] он более эффективен при злокачественных опухолях половых клеток, чем при эпителиальных опухолях.[23] Было обнаружено, что адъювантная химиотерапия улучшает выживаемость и снижает риск рецидива рака яичников по сравнению с отсутствием адъювантной терапии у женщин с эпителиальным раком яичников на ранней стадии.[67]
Химиотерапия при раке яичников обычно состоит из: платины, группа платина на основе препаратов в сочетании с неплатинами. Общие методы лечения могут включать: паклитаксел, цисплатин, топотекан, доксорубицин, эпирубицин, и гемцитабин. Карбоплатин обычно дается в сочетании с паклитаксел или же доцетаксел; типичной комбинацией является карбоплатин с паклитакселом.[19][22] Карбоплатин превосходит цисплатин в том, что он менее токсичен и имеет меньше побочных эффектов, что обычно позволяет улучшить качество жизни по сравнению с ним, хотя оба препарата одинаково эффективны.[22] Схемы из трех препаратов не оказались более эффективными,[19] и только платины или только неплатины менее эффективны, чем платины и неплатины в сочетании.[22] Химиотерапия на основе платины дает небольшое преимущество по сравнению с терапией без использования платины.[68] Комбинации платины могут улучшить выживаемость по сравнению с одной платиной. Имеющиеся данные свидетельствуют о том, что у людей с рецидивом рака яичников топотекан оказывает такое же влияние на общую выживаемость, как паклитаксел и топотекан плюс талидомид, в то время как он превосходит треосульфан и не так эффективен, как пегилированный липосомальный доксорубицин у людей, чувствительных к платине.[69]
Может быть назначена химиотерапия внутривенно или же в брюшной полости.[17] Хотя внутрибрюшинная химиотерапия связана с более длительной выживаемостью без прогрессирования заболевания и общей выживаемостью, она также вызывает более неблагоприятные побочные эффекты, чем внутривенная химиотерапия.[22] Он в основном используется, когда рак оптимально удален. Внутрибрюшинная химиотерапия может быть очень эффективной, поскольку рак яичников в основном распространяется внутри брюшной полости, и таким образом более высокие дозы лекарств могут достигать опухоли.[20]
Химиотерапия может вызвать анемия; внутривенное введение железа оказалось более эффективным, чем пероральное введение. добавки железа в снижении потребности в переливание крови.[22] Типичные циклы лечения включают одно лечение каждые 3 недели, повторение в течение 6 недель или более.[70] Менее 6 недель (циклов) лечения менее эффективны, чем 6 недель и более.[22] Злокачественные новообразования половых клеток лечат иначе, чем другие виды рака яичников - режим лечения блеомицин, этопозид и цисплатин (BEP) используется с 5-дневной химиотерапией, проводимой каждые 3 недели в течение 3-4 циклов.[17][23] Химиотерапия при опухолях половых клеток не вызывает аменорея, бесплодие, врожденные дефекты, или же выкидыш.[23] Поддерживающая химиотерапия не было показано, чтобы быть эффективным.[22]
У людей с BRCA мутации, химиотерапия платиной более эффективна.[19] Зародышевые опухоли и злокачественные опухоли полового канатика / стромы лечат химиотерапией, хотя дисгерминомы и опухоли полового канатика обычно не очень эффективны.[17][24]
Чувствительность к платине или устойчивость к платине
Если рак яичников рецидивирует, он считается частично чувствительным к платине или резистентным к платине в зависимости от времени, прошедшего с момента последнего рецидива, леченного платинами: частично чувствительный к платине рак рецидивировал через 6–12 месяцев после последнего лечения, а устойчивый к платине рак имеет интервал менее 6 месяцев. Химиотерапия второй линии может быть назначена после того, как рак станет симптоматическим, поскольку не наблюдается разницы в выживаемости между лечением бессимптомных (повышенный CA-125) и симптоматических рецидивов.[требуется медицинская цитата ]
При опухолях, чувствительных к платине, платины являются препаратами выбора для химиотерапии второй линии в сочетании с другими цитотоксическими агентами. Схемы включают карбоплатин в сочетании с пегилированный липосомальный доксорубицин, гемцитабин, или же паклитаксел.[17] Карбоплатин-дублетную терапию можно комбинировать с паклитакселом для повышения эффективности в некоторых случаях. Еще одна потенциальная адъювантная терапия при рецидивах, чувствительных к платине, - это олапариб, что может улучшить выживаемость без прогрессирования но не было показано улучшения Общая выживаемость.[22] (Olaparib, а Ингибитор PARP, был одобрен США FDA для использования при BRCA-ассоциированном раке яичников, который ранее лечился химиотерапией.[71][72]) Для рецидивирующих опухолей половых клеток дополнительные 4 цикла химиотерапии BEP являются лечением первой линии для тех, кто лечился хирургическим путем или платинами.
Если установлено, что опухоль резистентна к платине, винкристин, дактиномицин, и циклофосфамид (VAC) или некоторая комбинация паклитаксела, гемцитабина и оксалиплатин может использоваться как терапия второй линии.[23]
Для резистентных к платине опухолей не существует вариантов высокоэффективной химиотерапии. Режимы приема одного препарата (доксорубицин или топотекан ) не имеют высокой скорости отклика,[19] но в некоторых случаях используются монотерапевтические схемы топотекана, пегилированного липосомального доксорубицина или гемцитабина.[17][22] Топотекан нельзя применять людям с кишечной непроходимостью. Другой возможный режим лечения - паклитаксел, или его можно комбинировать с липосомальным доксорубицином, гемцитабином, цисплатином, топотеканом, этопозид, или же циклофосфамид.[70] (См. Также Паллиативную помощь ниже.)
Новые агенты разрабатываются для ингибирования развития новых кровеносных сосудов (ангиогенеза) у женщин с раком яичников, у которых развивается устойчивость к химиотерапевтическим препаратам. По состоянию на 2011 год доступны только предварительные результаты.[73]
Радиационная терапия
Дисгерминомы наиболее эффективно лечат лучевой терапией,[24] хотя это может вызвать бесплодие и постепенно отменяется в пользу химиотерапии.[17] Лучевая терапия не улучшает выживаемость людей с хорошо дифференцированными опухолями.[17]
При раке 1c и 2 стадии лучевая терапия используется после операции, если есть вероятность остаточного поражения в тазу, но брюшная полость свободна от рака. Лучевая терапия также может использоваться в паллиативной помощи при запущенных формах рака. Типичный курс лучевой терапии рака яичников составляет 5 дней в неделю в течение 3-4 недель. Общие побочные эффекты лучевой терапии включают диарею, запор и частое мочеиспускание.[74]
Гормональная терапия
Несмотря на то, что 60% опухолей яичников имеют рецепторы эстрогена, рак яичников редко поддается лечению гормональными препаратами. В Кокрановском обзоре было обнаружено отсутствие доказательств эффективности тамоксифена у людей с рецидивом рака яичников.[75]Сам по себе эстроген не влияет на рак, и тамоксифен и летрозол редко бывают эффективными.[19] «Некоторые женщины с пограничным раком яичников и стромальным раком яичников могут получать гормональную терапию».[60]
Иммунотерапия
Иммунотерапия - это тема текущих исследований рака яичников. В некоторых случаях препарат антитела бевацизумаб, хотя до сих пор является предметом активных исследований, он используется для лечения запущенного рака наряду с химиотерапией.[59] Он был одобрен для использования в Европейском Союзе.[76]
Следовать за
Конкретное наблюдение зависит, например, от типа и стадии рака яичников, лечения и наличия каких-либо симптомов. Обычно контрольный осмотр назначается сначала каждые 2–3 месяца, а затем два раза в год на срок до 5 лет.[77] При эпителиальном раке яичников наиболее частым тестом при последующем наблюдении является определение уровня СА-125. Однако лечение, основанное только на повышенных уровнях CA-125, а не на каких-либо симптомах, может усилить побочные эффекты без какого-либо продления жизни, поэтому последствия теста CA-125 можно обсудить до его проведения.[78] Рекомендация с 2014 года - рецидив рака может присутствовать, если уровень CA-125 вдвое выше нормы.[19] Лечение рецидива, обнаруженного CA-125, не улучшает выживаемость.[22]
Для женщин с опухоли половых клеток, контрольные тесты обычно включают альфа-фетопротеин (AFP) и / или хорионический гонадотропин человека. Для женщин с стромальный рак, тесты на гормоны, такие как эстроген, тестостерон и ингибин иногда бывают полезны.[78] Ингибин также может быть полезен для мониторинга развития опухолей полового канатика, наряду с вещество, ингибирующее мюллериан. AFP также можно использовать для мониторинга опухолей Сертоли-Лейдига.[17] При дисгерминомах лактатдегидрогеназа и его два изоферменты (ЛДГ-1 и ЛДГ-2 ) используются для проверки на повторение.[23]
Женщинам с раком яичников может не потребоваться стандартная визуализация для наблюдения за раком, если не появятся новые симптомы или онкомаркеры начать подниматься.[79] Визуализация без этих показаний не рекомендуется, потому что она вряд ли позволит обнаружить рецидив, улучшить выживаемость, а также потому, что она имеет свои собственные затраты и побочные эффекты.[79] Однако при желании можно использовать компьютерную томографию, хотя это нечасто.[19] Если опухоль легко визуализируется, визуализация может использоваться для контроля за ходом лечения.[80]
Паллиативная помощь
Паллиативная помощь направлен на облегчение симптомов и повышение или поддержание качества жизни. Цель такого лечения не в том, чтобы вылечить рак, а в том, чтобы сделать женщину более комфортной, живя с неизлечимым раком. Он рекомендован как часть плана лечения для любого человека с запущенным раком яичников или пациентов со значительными симптомами.[81] В случаях, резистентных к платине и резистентных к платине, основным лечением является другая паллиативная химиотерапия.[20][60]
Паллиативная помощь может включать лечение симптомов и осложнений рака, включая боль, тошноту, запор, асцит, непроходимость кишечника, отек, плевральный выпот, и мукозит. Особенно если рак прогрессирует и становится неизлечимым, лечение симптомов становится одной из основных целей терапии. Паллиативная помощь также может включать помощь в принятии решений, например, если и когда: хоспис является подходящим и предпочтительным местом для пациента в конце жизни.[22]
Непроходимость кишечника можно лечить с помощью паллиативная хирургия (колостома, илеостомия, или внутренний обходной анастомоз) или лекарство, но было показано, что операция увеличивает время выживания.[19][22] Паллиативная операция может привести к синдром короткой кишки, кожно-кишечный свищ, или повторная обструкция; или может быть невозможно из-за степени препятствия.[20] Другие методы лечения осложнений могут включать: полное парентеральное питание, а диета с низким содержанием остатков, паллиативный гастростомия и адекватный контроль боли.[19] Непроходимость кишечника также можно лечить с помощью октреотид когда паллиативная операция невозможна. Рак также может блокировать мочеточники, что может быть устранено нефростомия или мочеточниковый стент. Асцит можно облегчить повторным парацентез или размещение осушать для повышения комфорта.[82] Аналогичным образом можно лечить плевральный выпот с повторным плевроцентез, плевродез, или размещение слива.[20]
Лучевая терапия может использоваться как часть паллиативной помощи при запущенном раке яичников, поскольку она может помочь уменьшить опухоли, вызывающие симптомы.[60] Паллиативная лучевая терапия обычно длится всего несколько процедур, что намного короче, чем непаллиативная лучевая терапия.[74] Он также используется для паллиативной терапии устойчивых к химиотерапии опухолей половых клеток.[23]
Психосоциальная помощь
Рак яичников оказывает значительное влияние на качество жизни, психологическое здоровье и благополучие. Доступны вмешательства, чтобы помочь с потребностями и социальной поддержкой. Многие выжившие после рака яичников сообщают о хорошем качестве жизни и оптимизм. Другие сообщили о «духовном изменении», которое помогло им найти смысл во время их опыта. Другие рассказали, что потеряли веру после того, как им поставили диагноз «рак яичников». Те, кто прошел лечение, иногда испытывают социальная изоляция но получайте выгоду от отношений с другими выжившими. Разочарование и чувство вины были описаны некоторыми людьми, которые заявили о своей неспособности заботиться о своей семье.[83]
Самооценка и образ тела изменения могут произойти из-за потеря волос, удаление яичников и других репродуктивных структур, и шрамы. После отрастания волос наступает некоторое улучшение. Могут развиться сексуальные проблемы. Удаление яичников приводит к хирургическому вмешательству. менопауза что может привести к болезненный половой акт, сухость влагалища, потеря сексуальное желание и устал. Хотя прогноз лучше для более молодых выживших, влияние на сексуальность все же может быть значительным.[83]
Беспокойство, депрессия и бедствие чаще встречается у выживших после рака яичников, чем среди населения в целом.[83][84] Те же психосоциальные проблемы могут развиться у членов семьи. Эмоциональные эффекты могут включать страх смерти, грусть, проблемы с памятью и трудности с концентрацией внимания. Когда люди в начале лечения перенимали оптимизм, вероятность развития дистресса у них снижалась. Тем, кто боится рецидива рака, может быть трудно выразить радость даже без болезней. Чем больше процедур проходит женщина, тем больше вероятность потери надеяться выражается. Женщины часто могут справиться с негативными психосоциальными эффектами и уменьшить их с помощью ряда стратегий. Такие занятия, как путешествия, дополнительное время с семьей и друзьями, игнорирование статистика, ведение журнала и более активное участие в духовный События на основе y адаптивны.[83]
Женщины с раком яичников также могут испытывать трудности с питанием и подвержены риску недоедания.[85]
Прогноз
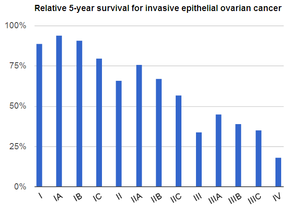
Рак яичников обычно плохо переносится прогноз. Это непропорционально смертельно, потому что в нем отсутствуют какие-либо четкие тесты на раннее выявление или скрининг, а это означает, что большинство случаев не диагностируются, пока они не достигнут продвинутой стадии.[79][19]
Рак яичников метастазирует на ранней стадии своего развития, часто еще до того, как его диагностируют. Опухоли высокой степени злокачественности метастазируют быстрее, чем опухоли низкой степени злокачественности. Обычно опухолевые клетки начинают метастазировать, разрастаясь в брюшной полости.[17] Более 60% женщин с раком яичников имеют рак III или IV стадии, когда он уже распространился за пределы яичников. При раке яичников клетки выделяются в естественную жидкость брюшной полости. Эти клетки могут затем имплантироваться в другие брюшные (перитонеальные) структуры, включая матку, мочевой пузырь, кишечник, выстилка стенки кишечника, и сальник, формируя новые опухоли еще до того, как заподозрят рак.
Пятилетняя выживаемость при всех стадиях рака яичников составляет 46%; одногодичная выживаемость составляет 72%, а десятилетняя выживаемость - 35%.[87] В случаях, когда диагноз ставится на ранней стадии заболевания, когда рак все еще ограничен первичным очагом, пятилетняя выживаемость составляет 92,7%.[88] Около 70% женщин с запущенным заболеванием отвечают на начальное лечение, большинство из которых достигают полной ремиссии, но у половины этих женщин через 1–4 года после лечения наблюдается рецидив.[17] Метастазы в мозг чаще встречается при раке III / IV стадии, но может возникать при раке I / II стадии. Люди с метастазами в головной мозг выживают в среднем 8,2 месяца, несмотря на операции, химиотерапию и лучевая терапия всего мозга может улучшить выживаемость.[22]
Выживаемость рака яичников значительно зависит от подтипа. Дисгерминомы имеют очень благоприятный прогноз. На ранних стадиях пятилетняя выживаемость у них составляет 96,9%.[24] Примерно две трети дисгермином диагностируются на стадии I.[23] Дисгерминомы III стадии имеют пятилетнюю выживаемость 61%; при лечении химиотерапией BEP после неполного хирургического удаления дисгерминомы имеют двухлетнюю выживаемость 95%. Злокачественные новообразования полового канатика и стромы также имеют благоприятный прогноз; поскольку они растут медленно, даже больные метастазами могут прожить десятилетие и более.[17] Опухоли с низким потенциалом злокачественности обычно имеют плохой прогноз только тогда, когда в брюшной полости обнаруживаются имплантаты инвазивной опухоли.[20]
Осложнения рака яичников могут включать распространение рака на другие органы, прогрессирующую потерю функций различных органов, асцит и кишечную непроходимость, что может быть фатальным. Непроходимость кишечника в нескольких местах является наиболее частой непосредственной причиной смерти.[19] Кишечная непроходимость при раке яичников может быть истинной непроходимостью, когда опухоль блокирует просвет кишечника, или псевдообструкция, когда опухоль препятствует нормальному перистальтика.[89] Постоянное накопление асцита можно вылечить, установив дренажный самодренаж.[19]
Прогностические факторы
Есть ряд прогностические факторы при раке яичников. Положительные прогностические факторы, указывающие на лучшие шансы на выживание, включают отсутствие остаточной болезни после операции (стадия III / IV), полная макроскопическая резекция (стадия IV), мутации BRCA2, молодой возраст (до 45 лет), несерозный тип, низкий гистологический класс, ранняя стадия, сочетание с раком эндометрия и низкий уровень CA-125. Существуют противоречивые данные о том, что BRCA1 является прогностическим фактором. И наоборот, отрицательные прогностические факторы - те, которые указывают на худшие шансы на выживание - включают разрыв капсулы яичника во время операции, пожилой возраст (старше 45 лет), муцинозный тип, стадия IV, высокий гистологический класс, светлоклеточный тип, поражение верхних отделов брюшной полости, высокий уровень CA-125, наличие опухолевых клеток в крови и повышенный циклооксигеназа-2.[22]
Экспрессия различных мРНК также может быть прогностическим фактором рака яичников. Высокий уровень Дроша и Дайсер связаны с улучшением выживаемости, тогда как высокий уровень лет-7б, HIF1A, EphA1, и поли (АДФ-рибоза) полимераза связаны с худшей выживаемостью. Раки, положительные для WT1 несут худший прогноз; Раковые опухоли, положительные по рецепторам эстрогена, имеют лучший прогноз.[22]
Показатели выживаемости
Общая пятилетняя выживаемость для всех типов рака яичников представлена ниже по стадиям и гистологическим классам:[17]
| Этап | Выживание |
|---|---|
| я | 90–95% |
| II | 70–80% |
| III | 20–50% |
| IV | 1–5% |
| Гистологический класс | Выживание |
|---|---|
| Низкая оценка | 88% |
| Промежуточный сорт | 58% |
| Высокий класс | 27% |
Приведенные ниже показатели выживаемости относятся к различным типам рака яичников в соответствии с Американское онкологическое общество.[86] Они происходят из Национальный институт рака, SEER, и основаны на пациентах, диагностированных с 2004 по 2010 год.
| Инвазивный эпителиальный рак яичников | |
|---|---|
| Этап | Относительный пятилетний процент выживаемости |
| я | 90% |
| Я | 94% |
| IB | 92% |
| IC | 85% |
| II | 70% |
| IIA | 78% |
| МИБ | 73% |
| III | 39% |
| IIIA | 59% |
| IIIB | 52% |
| IIIC | 39% |
| IV | 17% |
| Опухоли стромы яичников | |
|---|---|
| Этап | Относительный пятилетний процент выживаемости |
| я | 95% |
| II | 78% |
| III | 65% |
| IV | 35% |
| Зародышевые опухоли яичника | |
|---|---|
| Этап | Относительный пятилетний Процент выживаемости |
| я | 98% |
| II | 94% |
| III | 87% |
| IV | 69% |
| Карцинома фаллопиевых труб | |
|---|---|
| Этап | Относительный пятилетний процент выживаемости |
| я | 87% |
| II | 86% |
| III | 52% |
| IV | 40% |
| Опухоли с низким потенциалом злокачественности[20] | |
|---|---|
| Этап | Относительный пятилетний процент выживаемости |
| я | 99% |
| II | 98% |
| III | 96% |
| IV | 77% |
Частота рецидивов
После лечения часто возникает рецидив рака яичников. В целом, за 5-летний период 20% случаев рака I и II стадии повторяются. Большинство рецидивов происходит в брюшной полости.[20] Если рецидив возникает на запущенной стадии заболевания, он обычно возникает в течение 18 месяцев после начального лечения (18 месяцев выживаемость без прогрессирования ). Рецидивы можно лечить, но интервал без признаков болезни имеет тенденцию сокращаться, а химиорезистентность увеличивается с каждым рецидивом.[19] Когда дисгерминома рецидивирует, она, скорее всего, рецидивирует в течение года после постановки диагноза, а другие злокачественные опухоли половых клеток рецидивируют в течение 2 лет в 90% случаев. Опухоли зародышевых клеток, отличные от дисгермином, имеют плохой прогноз, когда они рецидивируют, с 10% долгосрочной выживаемостью.[23] Опухоли с низким потенциалом злокачественности редко рецидивируют, даже если предпочтительным методом лечения является хирургическое вмешательство. 15% опухолей LMP рецидивируют после односторонней операции на ранее не пораженном яичнике, и они обычно легко поддаются хирургическому лечению. Для более продвинутых опухолей может потребоваться до 20 лет для рецидива, если они вообще рецидивируют, и их лечат только хирургическим путем, если опухоль не изменила свои гистологические характеристики или не выросла очень быстро. В этих случаях и при значительном асците также может использоваться химиотерапия. На рецидив обычно указывает повышение уровня CA-125, которое затем переходит в симптоматический рецидив в течение 2–6 месяцев.[20] Рецидивирующие опухоли стромы полового канатика обычно не поддаются лечению, но не агрессивны.[23]
Это самый смертоносный гинекологический рак.[20]
Эпидемиология
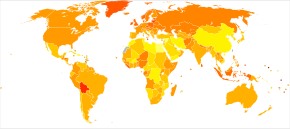
В 2014 году количество новых случаев заболевания в развитых странах составляло около 9,4 на 100 000 человек по сравнению с 5,0 на 100 000 в развивающихся странах.[19] В 2010 году во всем мире от рака яичников умерло около 160 000 человек. Это больше, чем 113 000 в 1990 году.[91] Число новых случаев заболевания в год в Европе составляет примерно 5–15 на 100 000 женщин.[22] В Европе, Литва, Латвия, Ирландия, Словакия, а Чехия имеют самый высокий уровень заболеваемости раком яичников, тогда как Португалия и Кипр имеют самую низкую заболеваемость.[22] В 2008 году пятилетняя выживаемость составила 44%. Это число увеличилось с 1977 года, когда выживаемость составляла 36%.[83]
Соединенные Штаты

В 2010 году в Соединенных Штатах было диагностировано 21 880 новых случаев заболевания, и 13 850 женщин умерли от рака яичников. Около 1800 из новых диагнозов были опухолями полового канатика или стромы.[17]
В 2014 году ежегодно ставилось более 220 000 диагнозов эпителиального рака яичников.[19] Общий риск для жизни в США составляет около 1,6%.[17][22] В США рак яичников поражает 1,3–1,4% женщин и является причиной смерти около 1% женщин.[20][92] В Соединенных Штатах это также пятое место по распространенности рака у женщин, но четвертое место среди причин смерти от рака.[22] Это снижение сделало его девятым по распространенности раком у женщин.[20]
Риски развития определенных типов рака яичников различны. Опухоли зародышевых клеток и опухоли стромы полового канатика встречаются реже, чем эпителиальные опухоли. Количество новых случаев заболевания в год в США составляет 0,4 на 100 000 женщин и 0,2 на 100 000 женщин, соответственно. У молодых людей опухоли стромы полового канатика и опухоли половых клеток составляют 1% от общего числа случаев рака яичников.[23] Рак яичников составляет примерно 4% случаев рака, диагностированных у женщин.[22]
объединенное Королевство
Это 5-й по частоте рак у женщин в Великобритании.[22][25] В Великобритании уровень заболеваемости среди всего населения составляет 21,6 на 100 000 человек.
В Соединенном Королевстве по состоянию на 2014 год примерно 7 000–7 100 диагнозов ежегодно и 4200 летальных исходов.[19][25] Риск в Великобритании такой же - 1,7%. Евреи ашкенази женщины несут мутировавшие BRCA аллели в пять раз чаще, чем у остального населения, что повышает риск развития рака яичников.[19] Рак яичников является пятым по распространенности раком у женщин в Великобритании (около 7100 женщин было диагностировано это заболевание в 2011 году) и пятым по частоте причиной смерти от рака у женщин (около 4300 женщин умерли в 2012 году).[93]
Этническая принадлежность
У чернокожих женщин риск развития опухолей стромы полового пуповины в два раза выше, чем у не чернокожих женщин.[23]
Пожилые женщины
В США уровень заболеваемости среди женщин старше 50 составляет примерно 33 на 100 000 человек.[94] Частота рака яичников в период с 1993 по 2008 гг. Снизилась у женщин в возрастной когорте 40–49 лет и в возрастной группе 50–64 года.[19] Рак яичников чаще всего диагностируется после менопаузы,[25] в возрасте от 60 до 64 лет. Девяносто процентов случаев рака яичников встречается у женщин старше 45 лет и 80 процентов - у женщин старше 50 лет.[22] У пожилых женщин чаще развивается рак яичников.[16]
При беременности
Злокачественные опухоли половых клеток - это тип рака яичников, который чаще всего возникает во время беременность. Их обычно диагностируют, когда при осмотре обнаруживается образование придатков (в 1-2% всех беременностей), опухоль выявляется на УЗИ или повышается уровень альфа-фетопротеина у родителей. Дермоидные кисты и дисгерминомы - самые распространенные опухоли половых клеток во время беременности. Опухоли из зародышевых клеток, диагностированные во время беременности, вряд ли будут метастазировать, и их можно лечить хирургическим путем, а в некоторых случаях - химиотерапией, что сопряжено с риском врожденных дефектов. Опухоли желточного мешка и незрелые тератомы растут особенно быстро и обычно лечатся химиотерапией даже во время беременности; однако дисгерминомы, которые были оптимально удалены, можно лечить после родов.[23]
Другие животные
Опухоли яичников были зарегистрированы в лошадь кобылы. Сообщенные типы опухолей включают тератому,[95][96] цистаденокарцинома,[97] и особенно гранулезно-клеточная опухоль.[98][99][100][101][102]
Исследование
Скрининг
Разрабатывается скрининг с помощью гистероскопии для получения образцов клеток для гистологического исследования. Это похоже на текущий мазок Папаниколау, который используется для выявления рака шейки матки.[103] Британское совместное испытание скрининга рака яичников тестирует методику скрининга, сочетающую анализы крови CA-125 с трансвагинальным ультразвуком.[19] Другие исследования показывают, что эта процедура скрининга может быть эффективной.[76] Хотя результаты, опубликованные в 2015 году, не были окончательными, были некоторые свидетельства того, что скрининг может спасти жизни в долгосрочной перспективе.[104] В результате испытание было продлено, и окончательные результаты будут опубликованы в конце 2019 года. Одна из основных проблем скрининга заключается в том, что не наблюдается явного прогрессирования заболевания от стадии I (неинвазивная) до стадии III (инвазивная), и это может невозможно обнаружить рак до того, как он достигнет стадии III. Другая проблема заключается в том, что методы скрининга, как правило, обнаруживают слишком много подозрительных поражений, большинство из которых не являются раком, а злокачественность можно оценить только хирургическим путем.[19] Метод ROCA в сочетании с трансвагинальной ультрасонографией изучается на женщинах из группы высокого риска, чтобы определить, является ли он жизнеспособным методом скрининга. Он также изучается на женщинах с нормальным риском, поскольку показал себя многообещающим для более широкого населения.[20] Также ведутся исследования, чтобы определить, помогает ли скрининг выявлять рак раньше у людей с мутациями BRCA.[76]
Прогноз исследования
Исследования различных прогностические факторы для рака яичников тоже продолжается. Недавние исследования показывают, что тромбоцитоз предсказывает более низкую выживаемость и более высокую стадию рака.[19] Текущие исследования также изучают преимущества хирургического вмешательства при рецидивирующем раке яичников.[76]
Иммунотерапия
Хотя это активная область исследований, по состоянию на 2018 г. нет убедительных доказательств того, что иммунотерапия эффективен при раке яичников.[105] Однако испытания антител и VEGF ингибитор бевацизумаб, что может замедлить рост новых кровеносных сосудов при раке показали многообещающие результаты, особенно в сочетании с пазопаниб, что также замедляет процесс роста кровеносных сосудов. Бевацизумаб оказался особенно эффективным в предварительных исследованиях рака III и IV стадии.[19] и был отмечен как минимум 15% ответов.[17] В частности, он исследуется при муцинозном раке яичников.[76]
Фармакология
ингибиторы mTOR были хорошо изученным потенциальным лечением в 2000-х и 2010-х годах, но побочные эффекты этих препаратов (особенно гипергликемия и гиперлипидемия ) плохо переносились, и улучшение выживаемости не подтверждалось. Ингибиторы киназы PI3 представляли интерес, но они, как правило, очень токсичны и вызывают понос. Другой исследуемый препарат - селуметиниб, а MAPK ингибитор. Это улучшило выживаемость, но не коррелировало с какими-либо мутациями, обнаруженными в опухолях.[19]
Бевацизумаб также можно комбинировать с химиотерапией платиной, комбинацией, которая дала положительные предварительные результаты в отношении ВБП, но неоднозначные результаты в отношении общей выживаемости. Одним из недостатков этих методов лечения является профиль побочных эффектов, который включает: высокое кровяное давление и протеинурия. Препарат также может обострить заболевание кишечника, приводя к свищи или же перфорация кишечника. Винтафолид, который состоит из антифолат в сочетании с винбластин, также проходит клинические испытания; это может оказаться полезным, потому что рецепторы фолиевой кислоты сверхэкспрессируются при многих формах рака яичников.[19] Еще одна потенциальная иммунотерапия: трастузумаб, который активен против опухолей, положительных по мутациям Her2 / neu.[17] Другие ингибиторы ангиогенеза также исследуются в качестве потенциальных средств лечения рака яичников. Комбретастатин и пазопаниб исследуются в сочетании с рецидивирующим раком яичников. Требананиб и таскинимод исследуются другие ингибиторы ангиогенеза. В моноклональное антитело фарлетузумаб исследуется как адъювант к традиционной химиотерапии. Другой вид иммунотерапии включает: вакцина, включая TroVax.[76]
Альтернатива химиотерапии BEP, схема из 3 циклов карбоплатин и этопозид, является актуальной темой исследований злокачественных новообразований половых клеток.[23]
Внутрибрюшинная химиотерапия в течение 2000-х и 2010-х годов также изучалась его способность доставлять более высокие дозы цитотоксического агента к опухолям. Предварительные испытания цисплатина и паклитаксела показали, что он плохо переносится, но действительно улучшает выживаемость, и исследуются более переносимые схемы.[19] Цисплатин и паклитаксел исследуются как внутрибрюшинные химиотерапевтические агенты. Также изучается особый режим химиотерапии для редких видов светлоклеточного рака: иринотекан в сочетании с цисплатином.[76]
Ингибиторы PARP также показали многообещающие результаты в ранних испытаниях, особенно у людей с BRCA генные мутации, поскольку белок BRCA взаимодействует с путем PARP. Он также изучается при рецидивирующем раке яичников в целом, где предварительные исследования показали более длительную ВБП. Конкретно, олапариб показал большую выживаемость по сравнению с доксорубицином, хотя это лечение все еще исследуется. Пока не ясно, какой биомаркеры предсказывают чувствительность к ингибиторам PARP.[19] Рукапариб - еще один ингибитор PARP, который исследуется при BRCA-положительном и BRCA-отрицательном рецидивирующем распространенном раке яичников. Нирапариб представляет собой ингибитор PARP, который тестируется при рецидивирующем раке яичников с положительным результатом по BRCA.[76]
Ингибиторы тирозинкиназы - еще один класс исследуемых препаратов, которые могут применяться при раке яичников. Ингибиторы ангиогенеза в рецепторная тирозинкиназа группа ингибиторов, в том числе пазопаниб, седираниб, и нинтеданиб, также было показано, что они увеличивают выживаемость без прогрессирования (ВБП), но их польза для общей выживаемости не исследовалась по состоянию на 2015 год.[19] Предварительные исследования показали, что цедираниб в сочетании с платинами при рецидивирующем раке яичников увеличивает время до второго рецидива на 3–4 месяца и увеличивает выживаемость на 3 месяца.[76] МК-1775 представляет собой ингибитор тирозинкиназы, который используется в комбинации с паклитакселом и карбоплатином при лечении чувствительных к платине опухолей с мутациями р53. Нинтеданиб исследуется как потенциальная терапия в сочетании с циклофосфамидом для людей с рецидивами.[76]
Ингибиторы гистон-деацетилазы (HDACi) - еще одна область исследований.
Гормоны и радиация
Гормональная терапия является темой текущих исследований рака яичников, в частности, оценки стоимости некоторых лекарств, используемых для лечения рака груди. К ним относятся тамоксифен, летрозол, и анастрозол. Предварительные исследования показали пользу тамоксифена у небольшого числа людей с запущенным раком яичников. Летрозол может помочь замедлить или остановить рост рецептор эстрогена положительный рак яичников. Анастрозол изучается у людей в постменопаузе с раком, положительным по рецепторам эстрогена.[76]
Также продолжаются исследования по уменьшению побочных эффектов лечения рака яичников. Лучевой фиброз, образование рубцовой ткани в области, обработанной радиацией, можно уменьшить с помощью гипербарическая кислородная терапия, но исследования в этой области не завершены. Лечение рака яичников также может вызывать у людей психические расстройства, в том числе: депрессия. Продолжаются исследования, чтобы определить, как консультирование и психотерапия могут помочь людям с раком яичников во время лечения.[76]
Воспаление
Есть некоторые признаки того, что воспалительные заболевания органов малого таза могут быть связаны с раком яичников, особенно в незападных странах. Это может быть связано с воспалительным процессом при воспалительном заболевании органов малого таза.[106]
Клинические испытания
Клинические испытания контролируются и финансируются правительственными организациями США для тестирования вариантов лечения, чтобы убедиться, что они безопасны и эффективны. К ним относятся клинические исследования NIH и вы (Национальные институты здоровья ),[107] Узнайте о клинических испытаниях (Национальный институт рака ),[108] Поиск клинических испытаний (Национальный институт рака),[109] ClinicalTrials.gov (Национальные институты здравоохранения).[110][57] Клинические испытания также проводятся в Канаде.[111]
Рекомендации
- ^ а б c d е ж грамм час я j «Лечение эпителиального рака яичников». NCI. 2014-05-12. В архиве из оригинала 5 июля 2014 г.. Получено 1 июля 2014.
- ^ а б «Каковы факторы риска рака яичников?». www.cancer.org. 2016-02-04. В архиве из оригинала 17 мая 2016 г.. Получено 18 мая 2016.
- ^ а б c d е ж грамм час я j k л м Всемирный доклад о раке 2014 г.. Всемирная организация здоровья. 2014. Глава 5.12. ISBN 978-9283204299. В архиве из оригинала от 19.09.2016.
- ^ а б c d «Профилактика рака яичников». NCI. 6 декабря 2013 г. В архиве из оригинала от 6 июля 2014 г.. Получено 1 июля 2014.
- ^ а б c «Профилактика рака яичников». NCI. 2014-06-20. В архиве из оригинала от 6 июля 2014 г.. Получено 1 июля 2014.
- ^ а б "Информационные бюллетени SEER Stat: рак яичника". NCI. В архиве из оригинала от 6 июля 2014 г.. Получено 18 июн 2014.
- ^ а б Соавторы исследования ГББ 2015 по заболеваемости и распространенности заболеваний и травм (октябрь 2016 г.). «Глобальная, региональная и национальная заболеваемость, распространенность и годы, прожитые с инвалидностью для 310 заболеваний и травм, 1990–2015 годы: систематический анализ для исследования глобального бремени болезней 2015». Ланцет. 388 (10053): 1545–1602. Дои:10.1016 / S0140-6736 (16) 31678-6. ЧВК 5055577. PMID 27733282.
- ^ а б ГББ 2015 «Смертность и причины смерти соавторов» (октябрь 2016 г.). «Ожидаемая продолжительность жизни на глобальном, региональном и национальном уровнях, смертность от всех причин и смертность от конкретных причин для 249 причин смерти, 1980–2015 годы: систематический анализ для исследования глобального бремени болезней 2015 года». Ланцет. 388 (10053): 1459–1544. Дои:10.1016 / S0140-6736 (16) 31012-1. ЧВК 5388903. PMID 27733281.
- ^ Сейден, Майкл (2015). «Гинекологические злокачественные новообразования, Глава 117». MGraw-Hill Medical. В архиве из оригинала 10 сентября 2017 г.. Получено 24 июня, 2017.
- ^ «Определение рака». Национальный институт рака. 2007-09-17. В архиве из оригинала 25 июня 2014 г.. Получено 10 июн 2014.
- ^ Эбелл М.Х., Калп МБ, Радке Т.Дж. (март 2016 г.). «Систематический обзор симптомов для диагностики рака яичников». Американский журнал профилактической медицины. 50 (3): 384–394. Дои:10.1016 / j.amepre.2015.09.023. PMID 26541098.
- ^ Раддон RW (2007). Биология рака (4-е изд.). Оксфорд: Издательство Оксфордского университета. п. 223. ISBN 9780195175431. В архиве из оригинала от 15.09.2015.
- ^ Пик Дж. М., ван Дист П. Дж., Верхейен Р. Х. (2008). «Канцерогенез яичников: альтернативная гипотеза». Рак яичников. Adv. Exp. Med. Биол. Успехи экспериментальной медицины и биологии. 622. стр.79–87. Дои:10.1007/978-0-387-68969-2_7. ISBN 978-0-387-68966-1. PMID 18546620.

- ^ Маоз, Асаф; Мацуо, Кодзи; Чикконе, Марсия А .; Мацузаки, Шинья; Клар, Максимилиан; Роман, Линда Д .; Суд, Анил К .; Гершенсон, Дэвид М. (29 мая 2020 г.). «Молекулярные пути и таргетная терапия злокачественных опухолей зародышевых клеток яичников и стромальных опухолей полового шнура: современный обзор». Рак. 12 (6): 1398. Дои:10.3390 / раки12061398. ISSN 2072-6694. ЧВК 7353025. PMID 32485873.
- ^ а б Гроссман Д.К., Карри С.Дж., Оуэнс Д.К., Барри М.Дж., Дэвидсон К.В., Дубени К.А. и др. (Февраль 2018). «Скрининг рака яичников: Рекомендация рабочей группы США по профилактическим услугам». JAMA. 319 (6): 588–594. Дои:10.1001 / jama.2017.21926. PMID 29450531.
- ^ а б c Гибсон С.Дж., Флеминг Г.Ф., Темкин С.М., Чейз Д.М. (2016). «Применение и результаты стандартной медицинской помощи для пожилых женщин с раком яичников: обзор литературы за последние 10 лет». Границы онкологии. 6: 63. Дои:10.3389 / fonc.2016.00063. ЧВК 4805611. PMID 27047797.
- ^ а б c d е ж грамм час я j k л м п о п q р s т ты v ш Икс у z аа ab ac объявление ае аф аг ах ай эй ак аль являюсь ан ао ap водный ар в качестве в au средний ау топор ай az ба bb до н.э bd Сайден М.В. (2012). «Гинекологические злокачественные новообразования». В Longo DL, Kasper DL, Jameson JL, Fauci AS, Hauser SL, Loscalzo J (ред.). Принципы внутренней медицины Харрисона (18-е изд.). Макгроу-Хилл. ISBN 978-0-07-174889-6.
- ^ а б c d "Рак яичников, изнутри, узнайте факты о гинекологическом раке" (PDF). Центры по контролю и профилактике заболеваний. Сентябрь 2016 г. В архиве (PDF) из оригинала 16 июня 2017 г.. Получено 17 июня, 2017.
 Эта статья включаетматериалы общественного достояния с веб-сайтов или документов Центры по контролю и профилактике заболеваний.
Эта статья включаетматериалы общественного достояния с веб-сайтов или документов Центры по контролю и профилактике заболеваний. - ^ а б c d е ж грамм час я j k л м п о п q р s т ты v ш Икс у z аа ab ac объявление ае аф аг ах ай эй ак аль являюсь ан ао ap водный ар в качестве в au средний ау топор ай az ба bb до н.э bd быть парень bg бх Джейсон Г.К., Кон Э.С., Китченер ХК, Ледерманн Д.А. (октябрь 2014 г.). "Рак яичников". Ланцет. 384 (9951): 1376–88. Дои:10.1016 / S0140-6736 (13) 62146-7. PMID 24767708. S2CID 205971030.
- ^ а б c d е ж грамм час я j k л м п о п q р s т ты v ш Икс у z аа ab ac объявление ае аф аг ах ай эй ак аль являюсь ан ао ap водный ар в качестве в au средний ау топор ай az ба bb до н.э bd быть парень bg бх би Ъ bk бл бм млрд бо бп бк br bs bt Хоффман Б.Л., Шорге Дж.О., Шаффер Дж.И., Халворсон Л.М., Брэдшоу К.Д., Каннингем Ф.Г. (2012). «Эпителиальный рак яичников». Гинекология Уильямса (2-е изд.). McGraw Hill Medical. С. 853–878. ISBN 978-0-07-171672-7.
- ^ «Симптомы рака яичников». www.cancerresearchuk.org. В архиве из оригинала на 2015-05-12. Получено 2015-05-16.
- ^ а б c d е ж грамм час я j k л м п о п q р s т ты v ш Икс у z аа ab ac объявление ае аф аг ах ай эй ак аль являюсь ан ао ap водный ар в качестве в au средний ау топор ай az ба bb до н.э bd быть парень bg бх би Ъ bk бл бм млрд бо бп бк br bs bt "Рак яичников". DynaMed. 18 июня 2015 года. В архиве с оригинала от 21 июня 2015 г.
- ^ а б c d е ж грамм час я j k л м п о п q р s т ты v ш Икс у z аа ab ac объявление ае аф аг ах ай эй ак аль являюсь ан ао Гинекология Уильямса 2012
- ^ а б c d е ж грамм ДеЧерни А., Натан Л., Гудвин TM, Лауфер Н., Роман А. (2012). «Детская и подростковая гинекология». Текущая диагностика и лечение Акушерство и гинекология (11-е изд.). ISBN 978-0071638562.
- ^ а б c d е ж грамм час я j k л м п о п «Риски и причины рака яичников». Cancer Research UK. 15 января 2014 г. В архиве из оригинала 21 февраля 2015 г.. Получено 29 января 2015.
- ^ Гонг Т.Т., Ву QJ, Фогтманн Э., Линь Б., Ван Ю.Л. (июнь 2013 г.). «Возраст менархе и риск рака яичников: метаанализ эпидемиологических исследований». Международный журнал рака. 132 (12): 2894–900. Дои:10.1002 / ijc.27952. ЧВК 3806278. PMID 23175139.
- ^ Мэнсон Дж. Э., Бассук С. С. (2012). "Переходный период менопаузы и гормональная терапия в постменопаузе". В Longo DL, Kasper DL, Jameson JL, Fauci AS, Hauser SL, Loscalzo J (ред.). Принципы внутренней медицины Харрисона (18-е изд.). Макгроу-Хилл. ISBN 978-0-07-174889-6.
- ^ «Профилактика рака яичников (PDQ®)». Национальный институт рака. 2013. В архиве из оригинала 31.12.2013. Получено 2013-12-30.
- ^ Кириакидис I, Папайоанниду П. (2016). «Бета-рецептор эстрогена и рак яичников: ключ к патогенезу и ответ на терапию». Арка Гинеколь Онкол. 293 (6): 1161–8. Дои:10.1007 / s00404-016-4027-8. PMID 26861465. S2CID 25627227.
- ^ Норквист Б.М., Харрелл М.И., Брэди М.Ф., Уолш Т., Ли М.К., Гульсунер С., Бернардс С.С., Касадей С., Йи К., Бургер Р.А., Чан Дж. К., Дэвидсон С.А., Маннел Р.С., ДиСильвестро П.А., Ланкес Н.А., Рамирес Северная Каролина, Кинг М.С. , Свишер Э.М., Биррер MJ (2015). «Наследственные мутации у женщин с карциномой яичников». JAMA Oncol. 30 (4): 1–9. Дои:10.1001 / jamaoncol.2015.5495. ЧВК 4845939. PMID 26720728.
- ^ Куусисто К.М., Бебель А., Вихинен М., Шлейткер Дж., Саллинен С.Л. (2011). «Скрининг мутаций BRCA1, BRCA2, CHEK2, PALB2, BRIP1, RAD50 и CDH1 у лиц с высоким риском мутации финского основателя BRCA1 / 2 с отрицательными мутациями рака груди и / или рака яичников». Рак груди Res. 13 (1): R20. Дои:10.1186 / bcr2832. ЧВК 3109589. PMID 21356067.
- ^ Салехи Ф., Данфилд Л., Филлипс К.П., Кревски Д., Вандерхайден, Британская Колумбия (март 2008 г.). «Факторы риска рака яичников: обзор с акцентом на гормональные факторы». Журнал токсикологии и гигиены окружающей среды, часть B: критические обзоры. 11 (3–4): 301–21. Дои:10.1080/10937400701876095. PMID 18368558. S2CID 5589506.
- ^ "Знаем ли мы, что вызывает рак яичников?". www.cancer.org. В архиве из оригинала от 10.11.2016.
- ^ Хьяртокер А., Мео М.С., Weiderpass E (январь 2010 г.). «Алкоголь и гинекологические онкологические заболевания: обзор». Европейский журнал профилактики рака. 19 (1): 1–10. Дои:10.1097 / CEJ.0b013e328333fb3a. PMID 19926999. S2CID 27570587.
- ^ Чжан X, Никосия SV, Бай В. (2006). «Рецептор витамина D - новая лекарственная мишень для лечения рака яичников». Цели лекарств от рака Curr. 6 (3): 229–44. Дои:10.2174/156800906776842939. PMID 16712459.
- ^ Бисвас А., О, П. И., Фолкнер Г. Е., Баджадж Р. Р., Сильвер М. А., Митчелл М. С., Альтер Д. А. (2015). «Сидячий образ жизни и его связь с риском заболеваемости, смертности и госпитализации у взрослых: систематический обзор и метаанализ». Анналы внутренней медицины. 162 (2): 123–32. Дои:10.7326 / M14-1651. PMID 25599350. S2CID 7256176.
- ^ а б Одунси К., Пейович Т., Андерсон М.Л. (2011). Молекулярная биология гинекологического рака. Рак ДеВиты, Хеллмана и Розенберга: принципы и практика онкологии. Уолтерс Клувер / Липпинкотт Уильямс и Уилкинс. С. 1302–1310. ISBN 978-1-4511-0545-2.
- ^ «Генетика рака груди и яичников (PDQ®)». Национальный институт рака. 2 октября 2014 г. В архиве из оригинала 22 октября 2014 г.. Получено 27 октября 2014.
- ^ «Можно ли рано обнаружить рак яичников?». Американское онкологическое общество.
- ^ Россинг М.А., Виклунд К.Г., Кушинг-Хауген К.Л., Вайс Н.С. (28 января 2010 г.). «Прогностическая ценность симптомов для раннего выявления рака яичников». J Natl Cancer Inst. 102 (4): 222–9. Дои:10.1093 / jnci / djp500. ЧВК 2826180. PMID 20110551.
- ^ а б c Миллер RW, Ueland FR (март 2012 г.). «Риск злокачественного новообразования при опухолях яичников, подтвержденных сонографией». Клиническое акушерство и гинекология. 55 (1): 52–64. Дои:10.1097 / GRF.0b013e31824970cf. PMID 22343229.
- ^ «Тесты на рак яичников». www.cancerresearchuk.org. В архиве из оригинала 18.05.2015. Получено 2015-05-16.
- ^ «Рекомендация CG122. Рак яичников: Распознавание и начальное лечение рака яичников, Приложение D: Индекс риска злокачественности (RMI I)». Клинические рекомендации NICE. Апрель 2011. Архивировано с оригинал 22 сентября 2013 г.
- ^ Geomini P, Kruitwagen R, Bremer GL, Cnossen J, Mol BW (февраль 2009 г.). «Точность оценок риска в прогнозировании злокачественных новообразований яичников: систематический обзор». Акушерство и гинекология. 113 (2 Pt 1): 384–94. Дои:10.1097 / AOG.0b013e318195ad17. PMID 19155910. S2CID 24585101.
- ^ Kaijser J, Bourne T., De Rijdt S, Van Holsbeke C, Sayasneh A, Valentin L, et al. (Август 2012 г.). «Основные результаты исследования Международного анализа опухолей яичников (IOTA): подход к оптимальной ультразвуковой характеристике патологии придатков». Австралазийский журнал ультразвука в медицине. 15 (3): 82–86. Дои:10.1002 / j.2205-0140.2012.tb00011.x. ЧВК 5025098. PMID 28191150.
- ^ а б Косары К.Л. (2007). «Глава 16: Рак яичника» (PDF). In Baguio RN, Young JL, Keel GE, Eisner MP, Lin YD, Horner MJ (ред.). Монография по выживанию SEER: Выживание от рака среди взрослых: Программа SEER США, 1988–2001 гг., Характеристики пациентов и опухолей. Программа SEER. NIH Pub. № 07-6215. Bethesda, MD: Национальный институт рака. С. 133–144. В архиве с оригинала от 10.10.2013.
- ^ а б c d е ж грамм час я «Виды рака яичников». www.cancerresearchuk.org. В архиве из оригинала 18.05.2015. Получено 2015-05-16.
- ^ а б c Леви Г., Перселл, Карен (2013). ДеЧерни А.Х., Натан Л., Лауфер Н., Роман А.С. (ред.). Предраковые и злокачественные заболевания яичников и яйцеводов. ТЕКУЩИЕ Диагностика и лечение: акушерство и гинекология, 11e. Макгроу-Хилл. ISBN 978-0-07-163856-2. В архиве из оригинала от 10.09.2017.
- ^ Нуччи, Мариса Р. (3 февраля 2020 г.). Гинекологическая патология: выпуск из серии Основы диагностической патологии (Второе изд.). п. 946. ISBN 978-0-323-35909-2.
- ^ Нуччи, Мариса Р. (3 февраля 2020 г.). Гинекологическая патология: выпуск из серии Основы диагностической патологии (Второе изд.). п. 946. ISBN 978-0-323-35909-2.
- ^ «Первичная карцинома брюшины». www.cancerresearchuk.org. В архиве из оригинала на 2015-05-20. Получено 2015-05-16.
- ^ а б «Стадия рака яичников» (PDF). Общество гинекологической онкологии. 1 января 2014 г. В архиве (PDF) из оригинала от 5 ноября 2014 г.
- ^ "Как ставится рак яичников?". Американское онкологическое общество. В архиве с оригинала 24 ноября 2016 г.. Получено 17 июня, 2017.
- ^ «Стадии рака яичников». www.cancerresearchuk.org. В архиве из оригинала 18.05.2015. Получено 2015-05-16.
- ^ а б c Кросвелл Дж. М., Броули О. В., Крамер Б. С. (2012). «Профилактика и раннее выявление рака». В Longo DL, Kasper DL, Jameson JL, Fauci AS, Hauser SL, Loscalzo J (ред.). Принципы внутренней медицины Харрисона (18-е изд.). Макгроу-Хилл. ISBN 978-0-07-174889-6.
- ^ Цибула Д., Видшвендтер М., Маек О., Дусек Л. (2010). «Перевязка маточных труб и риск рака яичников: обзор и метаанализ». Обновление репродукции человека. 17 (1): 55–67. Дои:10.1093 / humupd / dmq030. PMID 20634209.
- ^ а б «Как лечится рак яичников?». Центры по контролю и профилактике заболеваний. 13 февраля 2017 года. В архиве из оригинала 16 июня 2017 г.. Получено 17 июня, 2017.
 Эта статья включаетматериалы общественного достояния с веб-сайтов или документов Центры по контролю и профилактике заболеваний.
Эта статья включаетматериалы общественного достояния с веб-сайтов или документов Центры по контролю и профилактике заболеваний. - ^ Маркетти К., Пизано С., Факкини Дж., Бруни Г.С., Magazzino FP, Losito S, Pignata S (январь 2010 г.). «Лечение первой линии распространенного рака яичников: текущие исследования и перспективы». Экспертный обзор противоопухолевой терапии. 10 (1): 47–60. Дои:10.1586 / era.09.167. PMID 20014885. S2CID 40586650.
- ^ а б c d е «Виды лечения рака яичников». www.cancerresearchuk.org. В архиве из оригинала на 2015-05-12. Получено 2015-05-16.
- ^ а б c d «Лечение рака яичников». Канадское онкологическое общество. В архиве из оригинала 26 октября 2016 г.. Получено 17 июн 2017.
- ^ Элаттар А., Брайант А., Винтер-Роуч Б.А., Хатем М., Наик Р. (август 2011 г.). «Оптимальное первичное хирургическое лечение запущенного эпителиального рака яичников». Кокрановская база данных систематических обзоров (8): CD007565. Дои:10.1002 / 14651858.cd007565.pub2. ЧВК 6457688. PMID 21833960.
- ^ Roze JF, Hoogendam JP, van de Wetering FT, Spijker R, Verleye L, Vlayen J, et al. (Октябрь 2018 г.). «Позитронно-эмиссионная томография (ПЭТ) и магнитно-резонансная томография (МРТ) для оценки резектабельности опухоли при запущенном эпителиальном раке яичников / маточной трубы / первичном раке брюшины». Кокрановская база данных систематических обзоров. 10: CD012567. Дои:10.1002 / 14651858.cd012567.pub2. ЧВК 6517226. PMID 30298516.
- ^ Сегура-Сампедро, Хуан Хосе; Моралес-Сориано, Рафаэль; Арйона-Санчес, Альваро; Каскалес-Кампос, Педро (11 мая 2020 г.). «Вторичную хирургическую циторедукцию необходимо оценивать с учетом хирургической техники, полноты циторедукции и степени заболевания». Всемирный журнал хирургической онкологии. 18 (1): 92. Дои:10.1186 / s12957-020-01853-4. ЧВК 7216587. PMID 32393274.
- ^ Аль-Равахи Т., Лопес А.Д., Бристоу Р.Э., Брайант А., Элаттар А., Чаттопадхьяй С., Галаал К. (февраль 2013 г.). «Хирургическая циторедукция при рецидивирующем эпителиальном раке яичников». Кокрановская база данных систематических обзоров (2): CD008765. Дои:10.1002 / 14651858.cd008765.pub3. ЧВК 6457850. PMID 23450588.
- ^ «Хирургия рака яичников». www.cancerresearchuk.org. В архиве из оригинала 18.05.2015. Получено 2015-05-16.
- ^ Falcetta FS, Lawrie TA, Medeiros LR, da Rosa MI, Edelweiss MI, Stein AT и др. (Октябрь 2016 г.). «Сравнение лапароскопии и лапаротомии при раке яичников I стадии по FIGO». Кокрановская база данных систематических обзоров. 10: CD005344. Дои:10.1002 / 14651858.CD005344.pub4. ЧВК 6464147. PMID 27737492.
- ^ Лори Т.А., Винтер-Роуч Б.А., Хеус П., Китченер ХК (декабрь 2015 г.). «Адъювантная (послеоперационная) химиотерапия при ранней стадии эпителиального рака яичников». Кокрановская база данных систематических обзоров (12): CD004706. Дои:10.1002 / 14651858.cd004706.pub5. ЧВК 6457737. PMID 26676202.
- ^ Стюарт Л. (1999-01-25). «Химиотерапия при распространенном раке яичников. Группа продвинутых исследователей рака яичников». Кокрановская база данных систематических обзоров (2): CD001418. Дои:10.1002 / 14651858.cd001418. PMID 10796788.
- ^ Лихуа П., Чен Си, Ву, Техас (апрель 2008 г.). «Топотекан при раке яичников». Кокрановская база данных систематических обзоров (2): CD005589. Дои:10.1002 / 14651858.cd005589.pub2. ЧВК 6905487. PMID 18425923.
- ^ а б «Лекарства, применяемые при раке яичников». www.cancerresearchuk.org. Архивировано из оригинал на 2015-05-18. Получено 2015-05-16.
- ^ Яо, Стефани (19 декабря 2014 г.). «FDA одобрило Lynparza для лечения распространенного рака яичников: первый сопутствующий диагностический тест LDT также одобрен для выявления подходящих пациентов». Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. В архиве из оригинала 14 сентября 2015 г.
- ^ «Инновационное лечение гинекологического рака одобрено Фондом противораковых препаратов». Получено 2019-08-14.
- ^ Гайтскелл К., Мартинек И., Брайант А., Кехо С., Никум С., Моррисон Дж. (Сентябрь 2011 г.). «Ингибиторы ангиогенеза для лечения рака яичников». Кокрановская база данных систематических обзоров (9): CD007930. Дои:10.1002 / 14651858.cd007930.pub2. ЧВК 4167846. PMID 21901715.
- ^ а б «Лучевая терапия при раке яичников». www.cancerresearchuk.org. В архиве из оригинала 18.05.2015. Получено 2015-05-16.
- ^ Уильямс К., Симера I, Брайант А. (март 2010 г.). «Тамоксифен при рецидиве рака яичников». Кокрановская база данных систематических обзоров (3): CD001034. Дои:10.1002 / 14651858.cd001034.pub2. ЧВК 4235755. PMID 20238312.
- ^ а б c d е ж грамм час я j k л «Исследование рака яичников». www.cancerresearchuk.org. В архиве из оригинала на 2015-05-09. Получено 2015-05-16.
- ^ «Наблюдение за раком яичников». Cancer Research UK. 2017-08-30. В архиве из оригинала от 29.08.2014.
- ^ а б Последующий уход В архиве 2013-12-25 в Wayback Machine из Американское онкологическое общество. Последняя медицинская проверка: 21.03.2013. Последняя редакция: 06.02.2014
- ^ а б c Общество гинекологической онкологии (Февраль 2014), «Пять вещей, которые должны задать вопросы врачам и пациентам», Мудрый выбор: инициатива Фонд ABIM, Общество гинекологической онкологии, в архиве из оригинала на 1 декабря 2013 г., получено 19 февраля 2013, который цитирует
- Bhosale P, Peungjesada S, Wei W, Levenback CF, Schmeler K, Rohren E, Macapinlac HA, Iyer RB (август 2010 г.). «Клиническая полезность позитронно-эмиссионной томографии / компьютерной томографии в оценке подозрения на рецидив рака яичников при нормальных уровнях CA-125». Международный журнал гинекологического рака. 20 (6): 936–944. Дои:10.1111 / IGC.0b013e3181e82a7f. PMID 20683399. S2CID 13542187.
- ^ «Химиотерапия при раке яичников». www.cancerresearchuk.org. В архиве из оригинала 18.05.2015. Получено 2015-05-16.
- ^ «Предварительное клиническое заключение ASCO: интеграция паллиативной помощи в стандартную онкологическую помощь». ASCO. Архивировано из оригинал 21 августа 2014 г.. Получено 20 августа 2014.
- ^ «Лечение рака яичников на поздней стадии». www.cancerresearchuk.org. В архиве из оригинала от 19.05.2015. Получено 2015-05-16.
- ^ а б c d е Роланд КБ, Родригес Дж. Л., Паттерсон Дж. Р., Триверс К. Ф. (ноябрь 2013 г.). «Обзор литературы о социальных и психологических потребностях выживших после рака яичников». Психоонкология. 22 (11): 2408–18. Дои:10.1002 / pon.3322. PMID 23760742.
- ^ Уоттс С., Прескотт П., Мейсон Дж., Маклеод Н., Льюит Дж. (Ноябрь 2015 г.). «Депрессия и тревожность при раке яичников: систематический обзор и метаанализ показателей распространенности». BMJ Open. 5 (11): e007618. Дои:10.1136 / bmjopen-2015-007618. ЧВК 4679843. PMID 26621509.
- ^ Billson HA, Holland C, Curwell J, Davey VL, Kinsey L, Lawton LJ и др. (Сентябрь 2013). «Периоперационные диетологические вмешательства для женщин с раком яичников». Кокрановская база данных систематических обзоров (9): CD009884. Дои:10.1002 / 14651858.cd009884.pub2. PMID 24027084.
- ^ а б «Показатели выживаемости при раке яичников по стадиям». Американское онкологическое общество. В архиве из оригинала 29 октября 2014 г.. Получено 29 октября 2014.
- ^ «Статистика и перспективы рака яичников». www.cancerresearchuk.org. В архиве из оригинала 18.05.2015. Получено 2015-05-16.
- ^ а б Показатели выживаемости, основанные на статистике заболеваемости SEER и смертности от NCHS, по данным Национального института рака в Информационные бюллетени SEER Stat - Рак яичника В архиве 2014-07-06 в Wayback Machine
- ^ Гукальп Р., Датчер Дж. (2012). «Онкологические неотложные состояния». В Longo DL, Kasper DL, Jameson JL, Fauci AS, Hauser SL, Loscalzo J (ред.). Принципы внутренней медицины Харрисона (18-е изд.). Макгроу-Хилл. ISBN 978-0-07-174889-6.
- ^ «Страновые оценки ВОЗ по заболеваниям и травмам». Всемирная организация здоровья. 2009. Получено 15 июня, 2017. Статистика за 2004 год. Эта ссылка открывается при автоматической загрузке файла Excel.
- ^ Лозано Р., Нагави М., Форман К., Лим С., Сибуя К., Абояс В. и др. (Декабрь 2012 г.). «Глобальная и региональная смертность от 235 причин смерти для 20 возрастных групп в 1990 и 2010 годах: систематический анализ для исследования глобального бремени болезней 2010 года». Ланцет. 380 (9859): 2095–128. Дои:10.1016 / S0140-6736 (12) 61728-0. HDL:10536 / DRO / DU: 30050819. PMID 23245604. S2CID 1541253.
- ^ Рамирес П.Т., Гершенсон Д.М. (сентябрь 2013 г.). "Рак яичников". Руководство компании Merck для специалистов здравоохранения.

- ^ «Статистика рака яичников». Cancer Research UK. В архиве из оригинала 6 октября 2014 г.. Получено 28 октября 2014.
- ^ Хеннесси БТ, Сух Г.К., Маркман М (2011). Kantarjian HM, Wolff RA, Koller CA (ред.). Рак яичников. Руководство по медицинской онкологии доктора медицины Андерсона (2-е изд.). Макгроу-Хилл. ISBN 978-0-07-170106-8. В архиве из оригинала от 10.09.2017.
- ^ Catone G, Marino G, Mancuso R, Zanghì A (апрель 2004 г.). «Клинико-патологические особенности тератомы яичника лошади». Репрод. Внутренний. Аним. 39 (2): 65–9. Дои:10.1111 / j.1439-0531.2003.00476.x. PMID 15065985.
- ^ Лефевр Р., Теорет С, Доре М., Жирар С., Лаверти С., Вайланкур Д. (ноябрь 2005 г.). «Тератома яичника и эндометрит у кобылы». Может. Вет. J. 46 (11): 1029–33. ЧВК 1259148. PMID 16363331.
- ^ Сон Ю.С., Ли С.С., Чон В.И., Хонг И.Х., Пак С.Дж., Ким Т.Х., Чо Э.М., Пак Т.И., Чон К.С. (май 2005 г.). «Цистаденокарцинома яичника чистокровной кобылы». Aust. Вет. J. 83 (5): 283–4. Дои:10.1111 / j.1751-0813.2005.tb12740.x. PMID 15957389.
- ^ Фредерико Л.М., Жерар М.П., Пинто К.Р., Градил К.М. (май 2007 г.). «Двустороннее возникновение опухолей из клеток гранулезы у арабской кобылы». Может. Вет. J. 48 (5): 502–5. ЧВК 1852596. PMID 17542368.
- ^ Хоке С., Дерар Р., Осава Т., Тая К., Ватанабэ Г., Мияке И. (июнь 2003 г.). «Самопроизвольное восстановление атрофического контралатерального яичника без овариэктомии в случае кобылы, пораженной гранулезной тека-клеточной опухолью (GTCT)». J. Vet. Med. Наука. 65 (6): 749–51. Дои:10.1292 / jvms.65.749. PMID 12867740.
- ^ Седриш С.А., МакКлюр Дж. Р., Пинто С., Оливер Дж., Бурба Д. Д. (ноябрь 1997 г.). «Перекрут яичника, связанный с опухолью из клеток гранулезы у кобылы». Варенье. Вет. Med. Assoc. 211 (9): 1152–4. PMID 9364230.
- ^ Moll HD, Slone DE, Juzwiak JS, Garrett PD (1987). «Диагональный парамедианный доступ для удаления опухолей яичников у кобылы». Вет Сург. 16 (6): 456–8. Дои:10.1111 / j.1532-950X.1987.tb00987.x. PMID 3507181. Архивировано из оригинал на 2012-10-10.
- ^ Доран Р., Аллен Д., Гордон Б. (январь 1988 г.). «Использование сшивающих инструментов для удаления опухолей яичников у кобыл». Equine Vet. J. 20 (1): 37–40. Дои:10.1111 / j.2042-3306.1988.tb01450.x. PMID 2835223.
- ^ Gizzo S, Noventa M, Quaranta M, Vitagliano A, Saccardi C, Litta P, Antona D (февраль 2017 г.). «Новый гистероскопический подход для скрининга / ранней диагностики рака яичников». Письма об онкологии. 13 (2): 549–553. Дои:10.3892 / ol.2016.5493. ЧВК 5351187. PMID 28356928. требуется подписка
- ^ Джейкобс И.Дж., Менон Ю., Райан А., Джентри-Махарадж А., Бернелл М., Калси Дж. К. и др. (Март 2016 г.). «Скрининг рака яичников и смертность в Совместном испытании Великобритании по скринингу рака яичников (UKCTOCS): рандомизированное контролируемое исследование». Ланцет. 387 (10022): 945–956. Дои:10.1016 / S0140-6736 (15) 01224-6. ЧВК 4779792. PMID 26707054.
- ^ Paijens ST, Leffers N, Daemen T., Helfrich W., Boezen HM, Cohlen BJ, Melief CJ, de Bruyn M, Nijman HW (сентябрь 2018 г.). «Антигенспецифическая активная иммунотерапия рака яичников». Кокрановская база данных Syst Rev. 9: CD007287. Дои:10.1002 / 14651858.CD007287.pub4. ЧВК 6513204. PMID 30199097.
- ^ Ингерслев К., Хогдалл Э, Шнак Т.Х., Сковридер-Румински В., Хогдалл С., Блаакаер Дж. (2017). «Потенциальная роль инфекционных агентов и воспалительных заболеваний органов малого таза в канцерогенезе яичников». Инфекционные агенты и рак. 12 (1): 25. Дои:10.1186 / s13027-017-0134-9. ЧВК 5437405. PMID 28529540.
- ^ «Клинические исследования NIH и вы». В архиве из оригинала 8 июня 2017 г.. Получено 17 июн 2017.
- ^ «Информация о клинических испытаниях для пациентов и лиц, осуществляющих уход». Национальный институт рака. В архиве из оригинала 16 июня 2017 г.. Получено 17 июн 2017.
- ^ «Найдите клинические испытания, поддерживаемые NCI». Национальный институт рака. 2016-06-23. В архиве с оригинала на 1 июля 2017 г.. Получено 17 июн 2017.
- ^ "Главная - ClinicalTrials.gov". www.clinicaltrials.gov. В архиве из оригинала 16 июня 2017 г.. Получено 17 июн 2017.
- ^ "Главная - Канадские исследования рака". www.canadiancancertrials.ca. В архиве из оригинала 26 июня 2017 г.. Получено 17 июн 2017.
дальнейшее чтение
- Cannistra SA (декабрь 2004 г.). «Рак яичника». N. Engl. J. Med. 351 (24): 2519–29. Дои:10.1056 / NEJMra041842. PMID 15590954.
- Петручелли Н., Дали МБ, Фельдман Г.Л. (2013). «Наследственный рак груди и яичников, ассоциированный с BRCA1 и BRCA2». BRCA1 и BRCA2 Наследственный рак груди / яичников. Вашингтонский университет, Сиэтл. PMID 20301425. NBK1247.
внешняя ссылка
- «Рак яичников, маточной трубы и первичного рака брюшины - версия для пациентов». Национальный институт рака. Получено 30 марта 2017.
- Что такое инфографика рака яичников, информация о раке яичников - Больница Маунт-Синай, Нью-Йорк
| Классификация | |
|---|---|
| Внешние ресурсы |




