ANAVEX2-73 - ANAVEX2-73
Эта статья поднимает множество проблем. Пожалуйста помоги Улучши это или обсудите эти вопросы на страница обсуждения. (Узнайте, как и когда удалить эти сообщения-шаблоны) (Узнайте, как и когда удалить этот шаблон сообщения)
|
 | |
| Легальное положение | |
|---|---|
| Легальное положение |
|
| Идентификаторы | |
| |
| Количество CAS | |
| ChemSpider | |
| UNII | |
| Панель управления CompTox (EPA) | |
| Химические и физические данные | |
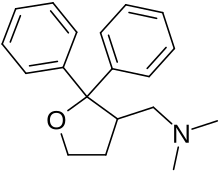
| Формула | C19ЧАС23NО |
| Молярная масса | 281.399 г · моль−1 |
| 3D модель (JSmol ) | |
| |
| |
ANAVEX2-73 это экспериментальный препарат в Испытания фазы II за Болезнь Альцгеймера, фаза I испытаний за эпилепсия, И в доклинические испытания за боковой амиотрофический склероз, болезнь Паркинсона, Синдром Ретта, Инсульт.[1][2] ANAVEX2-73 действует как мускариновый рецептор и умеренный рецептор сигма1 агонист.[1] ANAVEX2-73 может функционировать как пролекарство за ANAVEX19-144 а также сам препарат. ANAVEX19-144 является активным метаболитом ANAVEX 1-41, который похож на ANAVEX2-73, но не так селективен в отношении сигма-рецептора.[2]
Свойства и использование
ANAVEX2-73 был первоначально протестирован на мышах в отношении действия антагониста мускариновых рецепторов. скополамин, что вызывает ухудшение обучения.[1] Известно, что агонисты рецептора M1 обращают вспять амнезию, вызванную скополамином.[3] Скополамин используется при лечении болезнь Паркинсона и морская болезнь за счет уменьшения секреции желудка и кишечника, а также может уменьшить нервные сигналы к желудку.[3] Это через конкурентное торможение мускариновых рецепторов.[3] Мускариновые рецепторы участвуют в образовании обоих в ближайщем будущем и долгосрочные воспоминания.[1] Эксперименты на мышах показали, что агонисты рецепторов M1 и M3 ингибируют образование амилоид-бета и цель ГСК-3Б.[требуется разъяснение ] Кроме того, стимуляция рецептора M1 активирует AF267B, что в свою очередь блокирует β-секретаза, который расщепляет белок-предшественник амилоида произвести амилоид-бета пептид. Эти пептиды бета-амилоида объединяются вместе с образованием бляшек. Этот фермент[требуется разъяснение ] участвует в формировании Бляшки тау, которые распространены в Болезнь Альцгеймера.[требуется разъяснение ][4] Следовательно. Активация рецептора M1 снижает тау гиперфосфорилирование и накопление бета-амилоида.[4]
Sigma1 активация, по-видимому, участвует только в процессах долговременной памяти. Это частично объясняет, почему ANAVEX2-73, по-видимому, более эффективен в устранении проблем с долговременной памятью, вызванных скополамином, по сравнению с дефицитом краткосрочной памяти.[1] Рецептор сигма-1 расположен на митохондрии -ассоциированный эндоплазматический ретикулум мембран и модулирует стрессовую реакцию ER и локальный обмен кальция с митохондриями. ANAVEX2-73 предотвратил Aβ25-35 -индуцированное увеличение перекисное окисление липидов уровни Bax /Bcl-2 соотношение и цитохром с выпуск в цитозоль, которые указывают на повышенную токсичность.[требуется разъяснение ] ANAVEX2-73 подавляет митохондриальную респираторную дисфункцию и, следовательно, предотвращает окислительный стресс и апоптоз. Этот препарат предотвращал появление окислительного стресса. ANAVEX2-73 также проявляет антиапоптотическую и антиоксидантную активность. Частично это связано с тем, что агонисты сигма-1 стимулируют антиапоптозный фактор Bcl-2 из-за зависимой от активных форм кислорода транскрипционной активации ядерный фактор кБ.[5] Результаты Мориса (2016) демонстрируют, что соединения sigma1 обладают защитным потенциалом как сами по себе, так и, возможно, с другими агентами, такими как донепезил, ацетилхолинэстераза ингибитор, или мемантин, а Рецептор NMDA антагонист.[6]
Рекомендации
- ^ а б «АНАВЭКС 2-73». Adis Insight. Springer Nature Switzerland AG. Получено 2016-05-25.
- ^ а б c Малвия М., Кумар Ю.К., Аша Д., Чандра Дж. Н., Субхаш М. Н., Рангаппа К. С. (август 2008 г.). «Агонистическая активность мускаринового рецептора 1 новых производных N-арилтиомочевин, замещенных 3-морфолиноареколина в моделях пресенильной деменции при болезни Альцгеймера». Биоорганическая и медицинская химия. 16 (15): 7095–101. Дои:10.1016 / j.bmc.2008.06.053. PMID 18640043.
- ^ а б Леал Н.С., Шрейнер Б., Пинхо С.М., Филади Р., Вихагер Б., Карлстрём Н. и др. (Сентябрь 2016 г.). «Нокдаун митофузина-2 увеличивает контакт ER-митохондрий и снижает продукцию амилоидного β-пептида». Журнал клеточной и молекулярной медицины. 20 (9): 1686–95. Дои:10.1111 / jcmm.12863. ЧВК 4988279. PMID 27203684.
- ^ Лами В, Лонг Р., Морин Д., Виллар В., Морис Т. (2015-09-28). «Защита митохондрий с помощью смешанного мускаринового / σ1 лиганда ANAVEX2-73, производного тетрагидрофурана, у мышей, которым инъецировали пептид Aβ25-35, модель нетрансгенной болезни Альцгеймера». Границы клеточной неврологии. 8: 463. Дои:10.3389 / fncel.2014.00463. ЧВК 4299448. PMID 25653589.
- ^ Морис Т. (январь 2016 г.). «Защита агонистами рецептора сигма-1 синергетична с донепезилом, но не с мемантином, на мышиной модели нарушений памяти, вызванных амилоидом». Поведенческие исследования мозга. 296: 270–278. Дои:10.1016 / j.bbr.2015.09.020. PMID 26386305.
