Наследственная геморрагическая телеангиэктазия - Википедия - Hereditary hemorrhagic telangiectasia
| Наследственная геморрагическая телеангиэктазия | |
|---|---|
 | |
| Характерные телеангиэктазы губ. | |
| Специальность | Медицинская генетика |
Наследственная геморрагическая телеангиэктазия (HHT), также известный как Болезнь Ослера – Вебера – Ренду и Синдром Ослера – Вебера – Ренду, является редким аутосомно-доминантным генетическое расстройство что приводит к аномальному образованию кровеносных сосудов в кожа, слизистые оболочки, и часто в таких органах, как легкие, печень, и мозг.[1][2]
Это может привести к кровотечение из носа, острое и хроническое кровотечение пищеварительного тракта, и различные проблемы, связанные с вовлечением других органов. Лечение направлено на уменьшение кровотечения из поражений кровеносных сосудов, а иногда и на хирургия или другие целевые меры для удаления артериовенозные мальформации в органах. Хроническое кровотечение часто требует добавки железа и иногда переливание крови. HHT передается в аутосомно-доминантный мода и встречается у каждого 5000–8000 человек в Северной Америке.[1][2]
Болезнь носит имена сэра Уильям Ослер, Анри Жюль Луи Мари Ренду, и Фредерик Паркс Вебер, описавшие его в конце 19 - начале 20 вв.[3]
Признаки и симптомы
Телеангиэктазии

Телеангиэктазии (небольшие сосудистые мальформации) могут возникать на коже и слизистых оболочках носа и желудочно-кишечного тракта. Самая частая проблема - это кровотечение из носа (носовое кровотечение), которые часто происходят с детства и затрагивают около 90–95% людей с ГГ. Поражения на коже и во рту кровоточат реже, но могут считаться косметически неприятными; они затрагивают около 80%.[1][2] Поражения кожи обычно возникают на губы, то нос и пальцы, а также на коже лица в местах, подверженных воздействию солнечных лучей. Они появляются внезапно, и их количество со временем увеличивается.[2]
Около 20% страдают симптоматическими поражениями пищеварительного тракта, хотя более высокий процент имеют поражения, не вызывающие симптомов. Эти поражения могут периодически кровоточить, что редко бывает достаточно значительным, чтобы быть замеченным (в виде кровавая рвота или же черный табурет ), но в конечном итоге может привести к истощению утюг в теле, в результате чего железодефицитная анемия.[1][2]
Артериовенозная мальформация
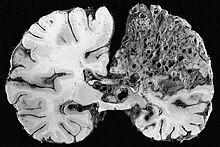
Артериовенозные мальформации (АВМ, более крупные сосудистые мальформации) возникают в более крупных органах, преимущественно в легких (легочные АВМ ) (50%), печень (30–70%) и мозг (церебральные АВМ, 10%), с очень небольшой долей (<1%) АВМ в спинной мозг.[1][2]
Сосудистые мальформации в легких могут вызвать ряд проблем. Легкие обычно «фильтруются» бактерии и сгустки крови из кровотока; АВМ обходят капиллярную сеть легких и позволяют им мигрировать в мозг, где бактерии могут вызвать абсцесс мозга и тромбы могут привести к Инсульт.[1] ГГТ является наиболее частой причиной АВМ легких: из всех людей, у которых обнаружены АВМ легких, 70–80% вызваны ГГТ.[4][5] Кровотечение из АВМ легких относительно необычно, но может вызвать кровохарканье (кашляет кровью) или гемоторакс (скопление крови в грудной полости).[1][2][4] Крупные сосудистые мальформации в легких позволяют поступать крови с низким содержанием кислорода. Правый желудочек чтобы обойти альвеолы, что означает, что эта кровь не имеет возможности поглощать свежий кислород. Это может привести к одышка.[4][5] Большие AVM могут привести к плоскостопие затруднение дыхания, которое более выражено в положении сидя, чем в положении лежа; это, вероятно, отражает изменения кровотока, связанные с позиционированием.[4] Очень большие АВМ вызывают заметную неспособность абсорбировать кислород, что может быть отмечено цианоз (посинение губ и кожи), избиение ногтей (часто встречается при хронически низком уровне кислорода) и гудящий шум над пораженной частью легкого обнаруживается стетоскоп.[4][5]
Симптомы, вызываемые АВМ в печени, зависят от типа аномального соединения, которое они образуют между кровеносными сосудами. Если связь между артерии и вены, большое количество крови обходит органы тела, что сердце компенсирует увеличением сердечный выброс. В итоге застойная сердечная недостаточность развивается («сердечная недостаточность с высоким выбросом») с одышкой и отеками ног среди других проблем.[1][6] Если AVM создает соединение между воротная вена и кровеносные сосуды печени, результат может быть портальная гипертензия (повышенное давление в воротной вене), при котором коллатеральные кровеносные сосуды образуются в пищевод (варикоз пищевода ), которые могут сильно кровоточить; кроме того, повышенное давление может вызвать скопление жидкости в брюшной полости (асцит ). Если поток в АВМ находится в другом направлении, кровь из воротной вены течет непосредственно в вены, а не через печень; это может привести к печеночная энцефалопатия (спутанность сознания из-за раздражающих мозг продуктов распада портальных ворот). В редких случаях желчные протоки лишаются крови, что приводит к тяжелым холангит (воспаление желчных протоков).[1][6] АВМ печени обнаруживаются более чем у 70% людей с ГГТ, но только 10% в результате испытывают проблемы.[2]
В головном мозге АВМ иногда оказывают давление, что приводит к головные боли. Они также могут увеличить риск припадки, как и любая аномальная ткань в головном мозге. Наконец, кровотечение из АВМ может привести к внутримозговое кровоизлияние (кровотечение в мозг), вызывающее любые симптомы инсульта, такие как слабость в части тела или затруднение речи. Если кровотечение происходит в субарахноидальное пространство (субарахноидальное кровоизлияние ) обычно есть сильная внезапная головная боль и снижение уровня сознания и часто слабость в части тела.[1][2]
Другие проблемы
Очень небольшая часть (те, кто подвержен SMAD4 (MADH4) мутации, см. Ниже) имеют множественные доброкачественные полипы в толстая кишка, который может истекать кровью или превращаться в колоректальный рак. Так же небольшая часть испытывает легочная гипертония, состояние, в котором давление в легочных артериях увеличивается, оказывая давление на правая сторона сердца и вызывая периферический отек (отек ног), обморок и атаки грудная боль. Было замечено, что риск тромбоз (особенно венозный тромбоз, в виде глубокие венозные тромбы или же легочная эмболия ) может быть увеличен. Есть подозрение, что у людей с HHT может быть легкое иммунодефицит и поэтому подвергаются несколько повышенному риску заражения.[1]
Генетика

HHT - это генетическое расстройство с аутосомно-доминантный образец наследования. У людей с симптомами HHT, у которых нет родственников с этим заболеванием, может быть новая мутация.[7] Гомозиготность оказывается фатальной внутриутробно.[1]
Различают пять генетических типов HHT. Из них три были связаны в частности гены, в то время как два оставшихся в настоящее время связаны только с определенным локус. Более 80% всех случаев HHT связаны с мутациями в любом ENG или же ACVRL1.[8] Всего известно более 600 различных мутаций. Вероятно преобладание того или иного типа в отдельных популяциях, но данные противоречивы. MADH4 мутации, которые вызывают полипоз толстой кишки в дополнение к HHT, составляют около 2% болезнетворных мутаций. Помимо MADH4, неясно, есть ли мутации в ENG и ACVRL1 привести к определенным симптомам,[1] хотя некоторые отчеты предполагают, что ENG мутации чаще вызывают проблемы с легкими, когда ACVRL1 мутации могут вызвать больше проблем с печенью,[2][5] и легочная гипертензия может быть особой проблемой у людей с ACVRL1 мутации.[8] Люди с одинаковыми мутациями могут иметь разную природу и тяжесть симптомов, что позволяет предположить, что дополнительные гены или другие факторы риска могут определять скорость развития поражений; они еще не идентифицированы.[2][8]
| Имя | OMIM | Ген | Locus | Описание |
|---|---|---|---|---|
| HHT1 | 187300 | ENG | 9q34.1 | ENG коды на эндоглин, а рецептор из TGF-β1 (трансформирующий фактор роста бета 1) и TGF-β3; генетическая связь была выявлена в 1994 году.[9] Высокая доля мутации сдвига рамки считывания наблюдалось.[1] Практически все мутации происходят во внеклеточной части белка (той части, которая находится на поверхность клетки ).[8] |
| HHT2 | 600376 | ACVRL1 | 12q11-q14 | ACVRL1 коды для Алк-1 (ACVR1, подобная рецептору активина киназа 1), рецептор TGF-β1; генетическая связь была выявлена в 1996 году.[10] |
| HHT3 | 601101 | Неизвестный | 5q31 | Функция неизвестна, связь выявлена в 2005 году.[11] |
| HHT4 | 610655 | Неизвестный | 7стр. 14. | Функция неизвестна, связь выявлена в 2006 г.[12] |
| JPHT | 175050 | MADH4 | 18q21.1 | MADH4 кодирует SMAD4, внутриклеточный сигнальный белок для рецепторов суперсемейства TGF. Мутации в этом гене вызывают HHT и ювенильный полипоз. Связь была выявлена в 2004 году.[13] Мутации в основном в экзонах 8–11, часто de novo (новоприобретенный, не переданный по наследству).[1] |
Патофизиология

Считается, что телеангиэктазии и артериовенозные мальформации при HHT возникают из-за изменений в ангиогенез, развитие кровеносных сосудов из существующих. Развитие нового кровеносного сосуда требует активации и миграции различных типов клеток, в основном эндотелий, гладкая мышца и перициты. Точный механизм, с помощью которого мутации HHT влияют на этот процесс, еще не ясен, и вполне вероятно, что они нарушают баланс между про- и антиангиогенными сигналами в кровеносных сосудах. Стенка телеангиэктазий необычно рыхлый, что объясняет тенденцию этих поражений к кровотечению.[1]
Все известные до сих пор гены связаны с кодом HHT для белков в Путь передачи сигналов TGF-β. Это группа белков, которая участвует в преобразование сигнала гормонов трансформирующий фактор роста бета суперсемейство (в трансформирующий фактор роста бета, костный морфогенетический белок и фактор дифференциации роста классы), в частности BMP9 / GDF2 и BMP10. Гормоны не попадают в клетку, а связываются с рецепторами на клеточной мембране; затем они активируют другие белки, в конечном итоге влияя на клеточное поведение разными способами, такими как клеточное выживание, пролиферация (увеличение числа) и дифференциация (становление более специализированным).[1] Для адекватной трансдукции гормонального сигнала необходима комбинация белков: по два каждого из двух типов серин / треонин-специфический тип киназы мембранные рецепторы и эндоглин. При связывании с гормоном рецепторные белки типа II фосфорилат (передача фосфат ) на рецепторные белки типа I (одним из которых является Alk-1), которые, в свою очередь, фосфорилируют комплекс SMAD белки (в основном SMAD1, SMAD5 и SMAD8 ). Они привязываются к SMAD4 и переносятся на ядро клетки где они действуют как факторы транскрипции и участвовать в транскрипция определенных генов. Помимо пути SMAD, мембранные рецепторы также действуют на Путь MAPK, который имеет дополнительные действия на поведение ячеек.[2] И Alk-1, и эндоглин являются выразил преимущественно в эндотелии, что, возможно, объясняет, почему мутации, вызывающие HHT, в этих белках приводят преимущественно к проблемам с кровеносными сосудами.[2][8] Обе ENG и ACVRL1 мутации приводят преимущественно к недостаточной продукции родственных белков, а не к неправильному функционированию белков.[8]
Диагностика
Диагностические исследования могут проводиться по разным причинам. Во-первых, необходимы некоторые анализы, чтобы подтвердить или опровергнуть диагноз. Во-вторых, некоторые необходимы для выявления возможных осложнений.[7]
Телеангиэктазии

Телеангиэктазии кожи и полости рта визуально идентифицируются на физический осмотр, и точно так же поражения в носу можно увидеть на эндоскопия из носоглотка или на ларингоскопия. Тяжесть носовых кровотечений может быть объективно количественно оценена с помощью анкеты в виде сетки, в которой записывается количество эпизодов носовых кровотечений и их продолжительность.[2]
Телеангиэктазии пищеварительного тракта можно выявить на эзофагогастродуоденоскопия (эндоскопия пищевода, желудка и первой части тонкой кишки). Эта процедура обычно проводится только при наличии анемии, более выраженной, чем ожидалось, из-за тяжести носового кровотечения или при наличии признаков сильного кровотечения (рвота кровью, черный стул). Если количество поражений, видимых при эндоскопии, неожиданно мало, оставшуюся часть тонкой кишки можно исследовать с помощью капсульная эндоскопия, в котором пациент проглатывает устройство в форме капсулы, содержащее миниатюрную камеру, которая передает изображения пищеварительного тракта на портативный цифровой рекордер.[2]
Артериовенозные мальформации
Для идентификации AVM требуется подробное медицинская визуализация органов, наиболее часто поражаемых этими поражениями. Не все АВМ вызывают симптомы или подвержены риску их возникновения, и, следовательно, между специалистами существует определенная степень разницы в том, будут ли проводиться такие исследования и с помощью каких методов; часто решение по этому вопросу принимается вместе с пациентом.[1]
Заподозрить наличие АВМ легких можно из-за ненормального внешнего вида легких на рентгенограмма грудной клетки, или же гипоксия (низкий уровень кислорода) на пульсоксиметрия или же газ артериальной крови решимость. Пузырьковая контрастная эхокардиография (пузырьковое эхо) может использоваться в качестве инструмента скрининга для выявления аномальных связей между легочные артерии и вены. Это включает инъекцию взволнованного физиологический раствор в вену с последующим ультразвуковым сканированием сердца. Обычно легкие удаляют небольшие пузырьки воздуха из кровотока, поэтому они видны только в легких. правое предсердие и Правый желудочек. Если AVM присутствует, пузырьки появляются в левое предсердие и левый желудочек, обычно 3–10 сердечные циклы после правой стороны; это медленнее, чем в пороки сердца, в котором есть прямая связь между правой и левой половиной сердца. Большее количество пузырьков с большей вероятностью указывает на наличие АВМ. Пузырьковое эхо - не идеальный инструмент для скрининга, поскольку он может пропустить более мелкие АВМ и не идентифицирует местонахождение АВМ. Часто контраст -повышенная компьютерная томография (КТ-ангиография) используется для выявления поражений легких; эта модальность имеет чувствительность более 90%.[1][2] На современных компьютерных томографах можно не вводить контраст.[5] Эхокардиография также используется при подозрении на легочную гипертензию или сердечную недостаточность с высоким выбросом из-за больших поражений печени, иногда за которыми следует катетеризация сердца для измерения давления в различных камерах сердца.[1]

Заподозрить АВМ печени можно из-за аномального функциональные пробы печени в крови, потому что развиваются симптомы сердечной недостаточности, или из-за желтуха или другие симптомы нарушения функции печени. Самый надежный первичный скрининговый тест - это Допплерография печени; это имеет очень высокую чувствительность для выявления сосудистых поражений в печени. При необходимости КТ с контрастным усилением может использоваться для дальнейшей характеристики АВМ.[1][2][6] Очень часто при сканировании печени обнаруживаются случайные узелки, чаще всего из-за: очаговая узловая гиперплазия (FNH), так как они в сотни раз чаще встречаются у HHT по сравнению с населением в целом. FNH считается безвредным. В общем, онкомаркеры и дополнительные методы визуализации используются для дифференциации FNH и злокачественных опухолей печени. Биопсия печени не рекомендуется для людей с HHT, так как риск кровотечения из АВМ печени может быть значительным.[6][7] Сканирование печени может быть полезно, если у кого-то есть подозрение на ГГТ, но оно не соответствует критериям (см. Ниже), если не могут быть продемонстрированы поражения печени.[7]
АВМ головного мозга могут быть обнаружены на компьютерная томографическая ангиография (КТА или КТ ангио) или магнитно-резонансная ангиография (MRA); КТА лучше показывает сами сосуды, а МРА дает более подробную информацию о взаимосвязи между АВМ и окружающей тканью мозга.[14] В целом рекомендуется МРТ.[2][7] Могут встречаться различные типы сосудистых мальформаций: АВМ, микро-АВМ, телеангиэктазии и артериовенозные свищи.[7] Если предполагается операция, эмболизация или другое лечение (см. Ниже), церебральная ангиография может потребоваться получить достаточную информацию о судах. Эта процедура сопряжена с небольшим риском инсульта (0,5%) и поэтому ограничена конкретными обстоятельствами.[7][14] Последние профессиональные руководства рекомендуют всем детям с подозрением или определенным диагнозом ГГТ в раннем возрасте пройти МРТ головного мозга для выявления АВМ, которые могут вызвать серьезные осложнения.[7] Другие предполагают, что скрининг на АВМ головного мозга, вероятно, не нужен тем, кто не испытывает никаких неврологических симптомов, потому что большинство поражений, обнаруженных при скрининговом сканировании, не требуют лечения, создавая нежелательные загадки.[1]
Генетическое тестирование
Генетические тесты доступны для ENG, ACVRL1 и MADH4 мутации. Тестирование не всегда необходимо для постановки диагноза, поскольку симптомов достаточно, чтобы отличить болезнь от других диагнозов. Есть ситуации, в которых тестирование может быть особенно полезным. Во-первых, дети и молодые люди, родители которых имеют определенную ГГТ, могут иметь ограниченные симптомы, но при этом подвержены риску некоторых из упомянутых выше осложнений; если известна мутация у пораженного родителя, отсутствие этой мутации у ребенка предотвратит необходимость скрининговых тестов. Кроме того, генетическое тестирование может подтвердить диагноз у людей с ограниченными симптомами, которых в противном случае назвали бы «возможными HHT» (см. Ниже).[7]
Генетическая диагностика при HHT затруднена, так как мутации происходят во многих различных местах связанных генов, при этом определенные мутации не встречаются очень часто (в отличие, например, от ΔF508 мутация в кистозный фиброз ). Анализ последовательности Поэтому наиболее полезным подходом является использование вовлеченных генов (чувствительность 75%), за которым следует дополнительное тестирование для обнаружения больших делеций и дупликаций (дополнительные 10%). Не все мутации в этих генах связаны с заболеванием.[7]
Мутации в MADH4 ген обычно связан с ювенильным полипозом, и обнаружение такой мутации указывает на необходимость обследования пациента и пораженных родственников на полипы и опухоли толстой кишки.[7]
Критерии
Диагноз может быть поставлен в зависимости от наличия четырех критериев, известных как "Кюрасао критерии ".[15] Если соблюдаются три или четыре, у пациента «определенная HHT», а два - «возможная HHT»:
- Спонтанный рецидивирующий носовое кровотечение
- Множественные телеангиэктазии в типичных местах (см. Выше)
- Проверенная висцеральная АВМ (легкие, печень, мозг, позвоночник)
- Член семьи первой степени с HHT
Несмотря на обозначение «возможный», человек с висцеральной АВМ и семейным анамнезом, но без носовых кровотечений или телеангиэктазий, по-прежнему имеет высокую вероятность ГГТ, потому что эти АВМ очень редко встречаются в общей популяции. В то же время того же нельзя сказать о носовых кровотечениях и редких телеангиэктазиях, которые возникают у людей без ГГТ в отсутствие АВМ. Диагностический статус человека может измениться с течением жизни, так как маленькие дети могут еще не проявлять всех симптомов; в возрасте 16 лет тринадцать процентов все еще не определены, в то время как в возрасте 60 лет подавляющее большинство (99%) имеет определенную диагностическую классификацию. Таким образом, детей от установленных пациентов с ГГТ можно отнести к категории «возможных ГГТ», так как у 50% может оказаться, что ГГТ будет развиваться в течение их жизни.[1]
Уход
Лечение HHT - это симптоматический (он имеет дело с симптомами, а не с самой болезнью), поскольку не существует терапии, которая напрямую останавливает развитие телеангиэктазий и АВМ. Кроме того, применяются некоторые методы лечения, чтобы предотвратить развитие общих осложнений.[7] Хроническое носовое кровотечение и кровотечение из пищеварительного тракта могут привести к анемии; если само кровотечение не может быть полностью остановлено, анемия требует лечения добавки железа. Тем, кто не переносит таблетки или растворы железа, может потребоваться введение внутривенный железо и переливание крови если анемия вызывает тяжелые симптомы, требующие быстрого улучшения анализа крови.[2][7]
Большинство методов лечения, используемых при ГГТ, были описаны у взрослых, и опыт лечения детей более ограничен.[7] Женщины с HHT, у которых беременная подвержены повышенному риску осложнений и внимательно наблюдаются, хотя абсолютный риск все еще низкий (1%).[1]
Носовые кровотечения
Острое носовое кровотечение можно контролировать с помощью различных мер, например, тампоны носовой полости абсорбирующими тампонами или гелями. Удаление пакетов после кровотечения может привести к повторному открытию хрупких сосудов, поэтому рекомендуется использовать смазку или атравматическую упаковку.[7] Некоторые пациенты могут захотеть научиться упаковывать себя, чтобы справиться с кровотечением из носа, не прибегая к медицинской помощи.[16]
Частые носовые кровотечения можно предотвратить частично, поддерживая влажность ноздрей и применяя физиологический раствор, эстроген -содержащие кремы или транексамовая кислота; они имеют мало побочных эффектов и могут иметь небольшую пользу.[7] Был использован ряд дополнительных методов для предотвращения повторного кровотечения, если простые меры оказались безуспешными. Лечебные методы лечения включают пероральный прием транексамовой кислоты и эстрогена; в свидетельство поскольку они относительно ограничены, а эстроген плохо переносится мужчинами и, возможно, несет риск рака и сердечных заболеваний у женщин после менопаузы.[2][7] Носовая коагуляция и прижигание может уменьшить кровотечение из телеангиэктазий и рекомендуется перед операцией. Однако настоятельно рекомендуется использовать наименьшее количество тепла и времени, чтобы предотвратить перфорацию перегородки и чрезмерную травму слизистой оболочки носа, которая уже подвержена кровотечению.[нужна цитата ] Склеротерапия - еще один способ остановить кровотечение. Этот процесс включает введение небольшого количества аэрированного раздражителя (детергент, такой как тетрадецилсульфат натрия) непосредственно в телеангиэктазии. Моющее средство заставляет сосуд разрушаться и затвердевать, в результате чего остается рубцовая ткань. Эта же процедура используется для лечения варикозного расширения вен и подобных заболеваний.[нужна цитата ]
Может быть возможно эмболизировать сосудистые поражения через интервенционная радиология; для этого необходимо провести катетер через большую артерию и найти верхнечелюстная артерия под Рентгеновское наведение с последующей инъекцией в сосуд частиц, закупоривающих кровеносные сосуды. Польза от процедуры, как правило, недолговечна.[7] и это может быть наиболее подходящим при эпизодах сильного кровотечения.[16]
Чтобы более эффективно минимизировать рецидивы и тяжесть носовых кровотечений, можно использовать другие варианты в сочетании с методами лечения, перечисленными выше. Внутривенно вводимые вещества против VEGF, такие как бевацизумаб (торговая марка Avastin), пазопинаб и талидомид или его производные, препятствуют образованию новых кровеносных сосудов, которые являются слабыми и, следовательно, склонными к кровотечению. В связи с прошлым опытом назначения талидомида беременным женщинам для облегчения симптомов тошноты и ужасных врожденных дефектов, которые последовали за этим, талидомид является последним средством лечения. Кроме того, талидомид может вызвать невропатию. Хотя это можно смягчить, изменив дозировку и назначив его производные, такие как ленолидомид и помалидомид, многие врачи предпочитают альтернативные ингибиторы VEGF. Было показано, что бевацизумаб значительно снижает тяжесть носового кровотечения без побочных эффектов.[нужна цитата ]
Если другие вмешательства оказались безуспешными, сообщалось, что несколько операций принесли пользу. Один из них - это дермопластика перегородки или процедура Сондерса,[17] в которой кожа пересаживается в ноздри, а другая - процедура Юнга,[18] при котором ноздри полностью закрыты.[7][16]
Кожа и пищеварительный тракт
Поражения кожи при HHT могут быть обезображивающими и могут поддаваться лечению с помощью длинноимпульсных Nd: YAG лазер.[2] Поражения кожи на кончиках пальцев могут иногда кровоточить и вызывать боль. Пересадка кожи иногда требуется для лечения этой проблемы.[2]
Что касается поражений пищеварительного тракта, легкое кровотечение и умеренная анемия лечатся добавками железа, и никакого специального лечения не назначается. Имеются ограниченные данные о лечении гормонами и транексамовой кислотой для уменьшения кровотечений и анемии. Тяжелая анемия или эпизоды сильного кровотечения лечат эндоскопическими методами. коагуляция аргоновой плазмой (APC) или лазерное лечение любых выявленных поражений; это может снизить потребность в поддерживающем лечении. Ожидаемые преимущества не таковы, что рекомендуются повторные попытки лечения поражений.[7] Внезапное очень сильное кровотечение встречается редко - при обнаружении альтернативных причин (например, язвенная болезнь ) необходимо учитывать[7]- но в таких случаях можно использовать эмболизацию.[1]
Легочные АВМ
После выявления поражений легких обычно лечат, чтобы предотвратить кровотечения и, что более важно, эмболию головного мозга. Это особенно актуально для поражений с питающим кровеносным сосудом 3 мм или больше, поскольку они с наибольшей вероятностью могут вызвать долгосрочные осложнения, если не будут лечить. Наиболее эффективная современная терапия - эмболизация съемными металлическими катушками или пробками.[19] Процедура включает пункцию большой вены (обычно под общий наркоз ), с последующим продвижение катетера через правый желудочек и в легочная артерия, после которого радиоконтраст вводится для визуализации АВМ (легочная ангиография ). После того, как поражение было идентифицировано, развертываются спирали, которые препятствуют кровотоку и позволяют поражению регрессировать. В опытных руках процедура имеет тенденцию быть очень эффективной и с ограниченными побочными эффектами, но поражения могут повторяться, и могут потребоваться дальнейшие попытки. Сканирование CTA повторяется для отслеживания повторения.[2][4][5][7] От хирургического удаления в настоящее время по существу отказались из-за успеха эмболотерапии.[5][7]
Считается, что пациенты с определенными легочными АВМ или аномальной контрастной эхокардиограммой без четко видимых поражений подвержены риску эмболии головного мозга. Поэтому им рекомендуется избегать подводное плавание с аквалангом, во время которого в кровотоке могут образовываться небольшие пузырьки воздуха, которые могут мигрировать в мозг и вызвать инсульт. По аналогии, антимикробная профилактика рекомендуется во время процедур, при которых бактерии могут попасть в кровоток, таких как стоматологическая работа и предотвращение образования пузырьков воздуха во время внутривенная терапия.[2][5][7]
АВМ печени
Учитывая, что АВМ печени обычно вызывают сердечную недостаточность с высоким выбросом, основное внимание уделяется лечению этого заболевания с помощью мочегонные средства для уменьшения объема циркулирующей крови, ограничения потребления соли и жидкости, а также антиаритмические средства в случае аритмия. Этого может быть достаточно для лечения симптомов отека и одышки. Если это лечение неэффективно или приводит к побочным эффектам или осложнениям, остается единственный вариант: трансплантация печени. Это зарезервировано для людей с тяжелыми симптомами, так как несет смертность около 10%, но дает хорошие результаты в случае успеха.[6][7] Точная точка, в которой должна быть предложена трансплантация печени, еще полностью не установлена.[6] Была предпринята попытка лечения эмболизацией, но она приводит к серьезным осложнениям у части пациентов и не рекомендуется.[5][6][7]
Другие связанные с печенью осложнения (портальная гипертензия, варикозное расширение вен пищевода, асцит, печеночная энцефалопатия) лечат теми же методами, что и цирроз, хотя использование трансъюгулярный внутрипеченочный портосистемный шунт лечение не рекомендуется из-за отсутствия документально подтвержденной пользы.[6]
АВМ головного мозга
Решение лечить мозг артериовенозные мальформации зависит от симптомов, которые они вызывают (например, судорог или головных болей). Риск кровотечения определяется предыдущими эпизодами кровотечения, а также наличием CTA или же MRA При сканировании AVM выглядит глубоко укоренившимся или имеет дренаж из глубоких вен. Размер АВМ и наличие аневризмы кажется, имеет меньшее значение.[14] При HHT некоторые поражения (артериовенозные фистулы с высоким потоком), как правило, вызывают больше проблем, и лечение необходимо. Другие АВМ могут со временем регрессировать без вмешательства.[7] В зависимости от локализации АВМ и ее размера доступны различные методы: хирургическое вмешательство, лучевое лечение и эмболизация. Иногда для одного и того же поражения используются несколько методов.[2][14]
Хирургия (автор краниотомия, открытая операция на головном мозге) может быть предложена на основании рисков лечения, определенных по шкале Спецлера – Мартина (степень I-V); этот балл выше при более крупных поражениях, которые находятся рядом с важными структурами головного мозга и имеют глубокий венозный дренаж. Поражения высокой степени (IV и V) имеют недопустимо высокий риск, и в таких случаях хирургическое вмешательство обычно не предлагается. Радиохирургия (с использованием целевых радиационная терапия например, гамма-нож ) можно использовать, если поражение небольшое, но близко к жизненно важным структурам. Наконец, эмболизация может использоваться на небольших поражениях, имеющих только один питательный сосуд.[14]
Экспериментальные методы лечения
Несколько анти-ангиогенез препараты, одобренные для лечения других заболеваний, например рака, были исследованы в небольших клинических испытаниях.[20] Анти-VEGF антитело бевацизумаб, например, был использован не по назначению в нескольких исследованиях. В крупном клиническом исследовании инфузия бевацизумаба была связана со снижением сердечного выброса и уменьшением продолжительности и количества эпизодов носового кровотечения у пролеченных пациентов с ГГТ.[21] Талидомид, еще один анти-ангиогенез также сообщалось, что он оказывает благотворное влияние на пациентов с HHT.[22] Было обнаружено, что лечение талидомидом вызывает созревание сосудов в экспериментальной модели HHT на мышах и снижает тяжесть и частоту носовых кровотечений у большинства небольшой группы пациентов с HHT. Уровни гемоглобина в крови этих пролеченных пациентов повысились в результате уменьшения кровотечения и улучшения стабилизации кровеносных сосудов.[23]
Эпидемиология

Популяционные исследования во многих регионах мира показали, что HHT встречается примерно с одинаковой скоростью почти во всех популяциях: где-то около 1 на 5000. В некоторых регионах это встречается гораздо чаще; например, в Французский регион Haut Jura частота составляет 1: 2351 - в два раза чаще, чем в других популяциях. Это было связано с эффект основателя, в котором популяция, происходящая от небольшого числа предков, имеет высокий уровень определенного генетического признака, потому что один из этих предков носил этот признак.[8] В Верхней Юре это стало результатом особого ACVRL1 мутация (названная c.1112dupG или c.1112_1113insG).[2] Самый высокий уровень HHT составляет 1: 1331, сообщается в Бонэйр и Кюрасао, два острова в Карибский бассейн принадлежащий к Нидерландские Антильские острова.[8]
Большинство людей с HHT имеют нормальную продолжительность жизни.[1] Поражения кожи и носовые кровотечения, как правило, развиваются в детстве. АВМ, вероятно, присутствуют с рождения, но не обязательно вызывают какие-либо симптомы. Частые носовые кровотечения являются наиболее частым симптомом и могут существенно повлиять на качество жизни.[7]
История
Несколько английских врачей XIX века, начиная с Генри Гавен Саттон (1836–1891)[24] а затем Бенджамин Гай Бабингтон (1794–1866)[25] и Легг Джона Уикхема (1843–1921),[26] описал наиболее общие черты HHT, в частности, повторяющиеся носовые кровотечения и наследственную природу болезни. Французский врач Анри Жюль Луи Мари Ренду (1844–1902) наблюдал за поражениями кожи и слизистых оболочек и отличал это состояние от гемофилия.[27] Канадец по происхождению Сэр Уильям Ослер (1849–1919), затем в Больница Джона Хопкинса а позже в Оксфордский университет, внес дальнейший вклад в отчет 1901 года, в котором он описал характерные поражения в пищеварительный тракт.[28] Английский врач Фредерик Паркс Вебер (1863–1962) сообщил об этом заболевании в 1907 году с рядом случаев.[29] Термин «наследственная геморрагическая телеангиэктазия» впервые был использован американским врачом Фредериком М. Хейнсом (1883–1946) в статье 1909 года об этом заболевании.[3][30]
Диагноз HHT оставался клиническим, пока генетические дефекты, вызывающие HHT, не были определены исследовательской группой в Медицинский центр Университета Дьюка, в 1994 и 1996 годах соответственно.[9][10] В 2000 году международный научный консультативный комитет HHT Foundation International опубликовал широко используемые в настоящее время критерии Кюрасао.[7][15] В 2006 году группа международных экспертов встретилась в Канада и сформулировал доказательный руководство, спонсируется HHT Foundation International.[7]
Рекомендации
- ^ а б c d е ж грамм час я j k л м п о п q р s т ты v ш Икс у z Говани Ф.С., Шовлин С.Л. (июль 2009 г.). «Наследственная геморрагическая телеангиэктазия: клинический и научный обзор». Европейский журнал генетики человека. 17 (7): 860–71. Дои:10.1038 / ejhg.2009.35. ЧВК 2986493. PMID 19337313.
- ^ а б c d е ж грамм час я j k л м п о п q р s т ты v ш Икс у z Dupuis-Girod S, Bailly S, Plauchu H (март 2010 г.). «Наследственная геморрагическая телеангиэктазия (HHT): от молекулярной биологии до ухода за пациентами». J. Thromb. Haemost. 8 (7): 1447–56. Дои:10.1111 / j.1538-7836.2010.03860.x. PMID 20345718.
- ^ а б Фучизаки У, Миямори Х, Китагава С., Канеко С., Кобаяши К. (ноябрь 2003 г.). «Наследственная геморрагическая телеангиэктазия (болезнь Ренду – Ослера – Вебера)». Ланцет. 362 (9394): 1490–4. Дои:10.1016 / S0140-6736 (03) 14696-X. PMID 14602446. S2CID 5304256.
- ^ а б c d е ж Gossage JR, Kanj G (август 1998 г.). «Легочные артериовенозные мальформации. Обзор современного состояния». Являюсь. J. Respir. Крит. Care Med. 158 (2): 643–61. Дои:10.1164 / ajrccm.158.2.9711041. PMID 9700146.
- ^ а б c d е ж грамм час я Faughnan ME, Granton JT, Young LH (май 2009 г.). «Легочно-сосудистые осложнения наследственной геморрагической телеангиэктазии». Евро. Респир. J. 33 (5): 1186–94. Дои:10.1183/09031936.00061308. PMID 19407052.
- ^ а б c d е ж грамм час Бускарини Э., Плаучу Х., Гарсия Цао Г. и др. (Ноябрь 2006 г.). «Поражение печени при наследственной геморрагической телеангиэктазии: согласованные рекомендации». Печень Инт. 26 (9): 1040–6. Дои:10.1111 / j.1478-3231.2006.01340.x. PMID 17032403.
- ^ а б c d е ж грамм час я j k л м п о п q р s т ты v ш Икс у z аа ab ac объявление Faughnan ME, Palda VA, Garcia-Tsao G, et al. (2011). «Международные рекомендации по диагностике и лечению наследственной геморрагической телеангиэктазии». Журнал медицинской генетики. 48 (2): 73–87. Дои:10.1136 / jmg.2009.069013. PMID 19553198. S2CID 18957466.
- ^ а б c d е ж грамм час Абдалла С.А., Летарте М (февраль 2006 г.). «Наследственная геморрагическая телеангиэктазия: современные взгляды на генетику и механизмы заболевания». Журнал медицинской генетики. 43 (2): 97–110. Дои:10.1136 / jmg.2005.030833. ЧВК 2603035. PMID 15879500.
- ^ а б Макаллистер К.А., Грогг К.М., Джонсон Д.В. и др. (Декабрь 1994 г.). «Эндоглин, TGF-бета-связывающий белок эндотелиальных клеток, является геном наследственной геморрагической телеангиэктазии 1 типа». Nat. Genet. 8 (4): 345–51. Дои:10.1038 / ng1294-345. PMID 7894484. S2CID 21623340.
- ^ а б Джонсон Д. В., Берг Дж. Н., Болдуин М. А. и др. (Июнь 1996 г.). «Мутации в гене киназы 1, подобной рецептору активина, при наследственной геморрагической телеангиэктазии 2 типа». Nat. Genet. 13 (2): 189–95. Дои:10.1038 / ng0696-189. PMID 8640225. S2CID 21379604.
- ^ Коул С.Г., Бегби М.Э., Уоллес Г.М., Шовлин С.Л. (2005). «Новый локус наследственной геморрагической телеангиэктазии (HHT3) отображается на хромосоме 5». Журнал медицинской генетики. 42 (7): 577–82. Дои:10.1136 / jmg.2004.028712. ЧВК 1736109. PMID 15994879.
- ^ Байрак-Тойдемир П., Макдональд Дж., Акарсу Н. и др. (2006). «Четвертый локус наследственной геморрагической телеангиэктазии отображается на хромосоме 7». Американский журнал медицинской генетики. 140 (20): 2155–62. Дои:10.1002 / ajmg.a.31450. PMID 16969873. S2CID 7393654.
- ^ Галлионе С.Дж., Репетто Г.М., Легиус Э. и др. (Март 2004 г.). «Комбинированный синдром ювенильного полипоза и наследственной геморрагической телеангиэктазии, связанный с мутациями в MADH4 (SMAD4)». Ланцет. 363 (9412): 852–9. Дои:10.1016 / S0140-6736 (04) 15732-2. PMID 15031030. S2CID 29539536.
- ^ а б c d е Фридлендер Р.М. (июнь 2007 г.). «Клиническая практика. Артериовенозные мальформации головного мозга». N. Engl. J. Med. 356 (26): 2704–12. Дои:10.1056 / NEJMcp067192. PMID 17596605.
- ^ а б Шовлин С.Л., Гутмахер А.Е., Бускарини Е. и др. (Март 2000 г.). «Диагностические критерии наследственной геморрагической телеангиэктазии (синдром Ренду – Ослера – Вебера)». Американский журнал медицинской генетики. 91 (1): 66–7. Дои:10.1002 / (SICI) 1096-8628 (20000306) 91: 1 <66 :: AID-AJMG12> 3.0.CO; 2-P. PMID 10751092.
- ^ а б c Гейстхофф UW, Fiorella ML, Fiorella R (2006). «Лечение рецидивирующего носового кровотечения при HHT». Curr. Pharm. Des. 12 (10): 1237–42. Дои:10.2174/138161206776361255. PMID 16611115.
- ^ Сондерс WH (1963). «Дермопластика перегородки: новая оперативная процедура для контроля носовых кровотечений у пациентов с наследственной геморрагической телеангиэктазией». J. Laryngol. Отол. 77 (1): 69–76. Дои:10.1017 / S0022215100060382. PMID 13986828.
- ^ Янг А. (май 1967). «Закрытие ноздрей при атрофическом рините». J. Laryngol. Отол. 81 (5): 515–24. Дои:10.1017 / S0022215100067426. PMID 6024992.
- ^ Cusumano, Lucas R .; Даквилер, Гэри Р.; Робертс, Дастин Дж .; МакВильямс, Джастин П. (30 августа 2019 г.). «Лечение рецидивирующих легочных артериовенозных мальформаций: сравнение проксимальной и дистальной техники эмболизации». Сердечно-сосудистая и интервенционная радиология. 43 (1): 29–36. Дои:10.1007 / s00270-019-02328-0. PMID 31471718. S2CID 201675132.
- ^ Шовлин С.Л. (2010). «Наследственная геморрагическая телеангиэктазия: патофизиология, диагностика и лечение» (PDF). Blood Rev. 24 (6): 203–19. Дои:10.1016 / j.blre.2010.07.001. HDL:10044/1/22167. PMID 20870325.
- ^ Dupuis-Girod S, Ginon I, Saurin JC, Marion D, Guillot E, Decullier E, Roux A, Carette MF, Gilbert-Dussardier B, Hatron PY, Lacombe P, Lorcerie B, Rivière S, Corre R, Giraud S, Bailly S, Paintaud G, Ternant D, Valette PJ, Plauchu H, Faure F (2012). «Бевацизумаб у пациентов с наследственной геморрагической телеангиэктазией и тяжелыми сосудистыми мальформациями печени и высоким сердечным выбросом». JAMA. 307 (9): 948–55. Дои:10.1001 / jama.2012.250. PMID 22396517.
- ^ Франчини М., Фраттини Ф, Крестани С., Бонфанти С. (2012). «Новые методы лечения носового кровотечения при наследственной геморрагической телеангиэктазии: систематический обзор клинического опыта применения талидомида». J Тромб Тромболизис. 36 (3): 355–7. Дои:10.1007 / s11239-012-0840-5. PMID 23143669. S2CID 33837604.
- ^ Лебрин Ф., Срун С., Раймонд К., Мартин С., ван ден Бринк С., Фрейтас С., Бреан С., Мативе Т., Ларриве Б., Томас Дж. Л., Артур Х. М., Вестерманн С. Дж., Диш Ф, Магер Дж. Дж., Снайдер Р. Дж., Эйхман А., Mummery CL (2010). «Талидомид стимулирует созревание сосудов и уменьшает носовое кровотечение у людей с наследственной геморрагической телеангиэктазией». Нат Мед. 16 (4): 420–8. Дои:10,1038 / нм.2131. PMID 20364125. S2CID 10649281.
- ^ Саттон HG (1864). «Носовое кровотечение как признак нарушения питания и дегенерации сосудистой системы». Med. Зеркало: 769–81.
- ^ Бабингтон Б.Г. (1865 г.). «Наследственное носовое кровотечение». Ланцет. 2 (2195): 362–363. Дои:10.1016 / S0140-6736 (02) 55197-7.
- ^ Легг W (1876 г.). «Случай гемофилии, осложненной множественными невусами». Ланцет. 2 (2781): 856–7. Дои:10.1016 / S0140-6736 (02) 49594-3.
- ^ Ренду HJ (1896). "Épistaxis répétées chez un sujet porteur de petits angiomes cutanés et muqueux". Газ. Прыгать.: 1322–3.
- ^ Ослер В. (1901). «О семейной форме рецидивирующего носового кровотечения, связанного с множественными телеангиэктазами кожи и слизистых оболочек». Бык. Больница Джонса Хопкинса. 12: 333–7.
- ^ Вебер Ф.П. (1907). «Множественные наследственные ангиомы развития (телеангиэктазы) кожи и слизистых оболочек, связанные с повторяющимися кровотечениями». Ланцет. 2 (4377): 160–162. Дои:10.1016 / S0140-6736 (00) 32590-9.
- ^ Ханес FM (1909). «Множественные наследственные телеангиэктазии, вызывающие кровотечение (наследственные геморрагические телеангиэктазии)». Бык. Больница Джонса Хопкинса. 20: 63–73.
| Классификация | |
|---|---|
| Внешние ресурсы |
