Хориидеремия - Choroideremia
| Хориидеремия | |
|---|---|
| Другие имена | CHM, тапетохориоидальная дистрофия |
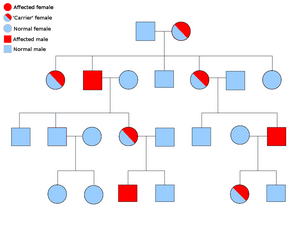 | |
| Примерная родословная, показывающая наследование связанного с полом расстройства, такого как хоридеремия. | |
| Специальность | Офтальмология |
| Симптомы | Прогрессирующая потеря зрения |
| Обычное начало | Детство |
| Продолжительность | Хронический |
| Причины | Генетический |
| Диагностический метод | Генетическое тестирование, семейный анамнез, осмотр глазного дна |
Хориидеремия (/kɒˌрɔɪdɪˈрямяə/; CHM) является редким, Х-сцепленный рецессивный форма наследственного сетчатка дегенерация, которая поражает примерно 1 из 50 000 мужчин. Заболевание вызывает постепенную потерю зрения, начиная с детства. куриная слепота с последующей потерей периферического зрения и прогрессирующей потерей центрального зрения в более позднем возрасте. Прогресс продолжается на протяжении всей жизни человека, но как скорость изменений, так и степень потери зрения различны среди пострадавших, даже в пределах одной семьи.[1]
Хориидеремия вызывается Потеря функции мутация в CHM ген который кодирует Rab escort протеин 1 (REP1), белок, участвующий в модификации липидов Rab белки. Хотя полный механизм заболевания до конца не изучен, недостаток функционального белка в сетчатке приводит к гибели клеток и постепенному ухудшению их состояния. пигментный эпителий сетчатки (RPE), фоторецепторы и сосудистая оболочка.[2][3]
По состоянию на 2019 год лечения хориидеремии не существует; тем не мение, сетчатка генная терапия клинические испытания продемонстрировали возможное лечение.[4]
Презентация
Поскольку CHM ген находится на Х хромосома, симптомы наблюдаются почти исключительно у мужчин. Хотя есть несколько исключений, женщины перевозчики имеют заметное отсутствие пигментации в РПЭ, но не испытывают никаких симптомов.[5] Женщины-носители имеют 50% шанс иметь либо пораженного сына, либо дочь-носителя, в то время как мужчина с хоридеремией будет иметь всех дочерей-носителей и здоровых сыновей.
Несмотря на то, что течение болезни может значительно варьироваться,[1][6] есть общие тенденции. Первый симптом, который замечают многие люди с хориидеремией, - это значительная потеря ночного зрения, которая начинается в молодости.[7] Периферийное зрение потеря зрения происходит постепенно, начиная с кольцевой потери зрения и переходя к «туннельному зрению» во взрослом возрасте.[8] Лица с хориидеремией обычно хорошо себя чувствуют. Острота зрения до 40 лет, но в конечном итоге теряют из виду в какой-то момент в возрасте 50–70 лет.[8] Исследование 115 человек с хориидеремией показало, что у 84% пациентов в возрасте до 60 лет острота зрения 20/40 или лучше, тогда как 33% пациентов старше 60 лет имели остроту зрения 20/200 или хуже. Наиболее серьезное нарушение остроты зрения (только умение считать пальцы или хуже) не наблюдалось до седьмого десятилетия жизни. В том же исследовании было установлено, что средняя скорость потери остроты зрения составляет около 0,09. logMAR за 5 лет, что составляет примерно 1 строку на Диаграмма Снеллена.[2]
Диагностика
Диагноз хориоидеремии может быть поставлен на основании семейного анамнеза, симптомов и характерного внешнего вида глазное дно.[9] Однако хориидеремия имеет несколько общих клинических признаков с пигментный ретинит, аналогичная, но более широкая группа дегенеративных заболеваний сетчатки, затрудняющая постановку конкретного диагноза без генетического тестирования. Из-за этого хоридеремию часто изначально ошибочно принимают за пигментный ретинит.[10] Множество разных генетическое тестирование методы могут быть использованы для проведения дифференциального диагноза.[11][12]
Управление
Хотя в настоящее время ничего нельзя сделать, чтобы остановить или обратить вспять дегенерацию сетчатки, есть шаги, которые можно предпринять, чтобы замедлить скорость потери зрения. Рекомендуются солнцезащитные очки, блокирующие УФ-излучение, для использования на открытом воздухе, соответствующее диетическое потребление свежих фруктов и листовых зеленых овощей, антиоксидантные витаминные добавки и регулярный прием диетических жирных кислот омега-3 с очень длинной цепью.[8] Одно исследование показало, что пищевая добавка лютеин увеличивается макулярный пигмент уровни у пациентов с хориидеремией. В течение длительного периода времени эти повышенные уровни пигментации «могли» замедлить дегенерацию сетчатки.[13] Дополнительные вмешательства, которые могут потребоваться, включают хирургическую коррекцию отслоения сетчатки и катаракты, услуги по лечению слабовидящих и консультирование, чтобы помочь справиться с депрессией, потерей независимости и беспокойством по поводу потери работы.[8]
Генная терапия
Генная терапия в настоящее время не является вариантом лечения, однако клинические испытания как для хориоидеремии, так и для Врожденный амавроз Лебера (LCA) дали несколько многообещающие результаты.[14]
Клинические испытания генной терапии для пациентов с LCA начались в 2008 году в трех разных центрах.[15][16][17][18] В целом, эти исследования показали, что терапия безопасна, в некоторой степени эффективна и многообещающа в качестве будущего лечения подобных заболеваний сетчатки.
В 2011 году был проведен первый курс генной терапии хориидеремии.[19] Операцию провел Роберт Макларен, Профессор офтальмологии Оксфордского университета и руководитель исследовательской группы клинической офтальмологии в лаборатории офтальмологии Наффилда (NLO).[14][20][21] В исследовании 2 дозы AAV Вектор .REP1 вводили субретинально 12 пациентам с хориидеремией. Исследование преследовало 2 цели:
- для оценки безопасности и переносимости вектора AAV.REP1
- для наблюдения терапевтического эффекта или замедления дегенерации сетчатки генной терапии во время исследования и через 24 месяца после лечения[22]
Несмотря на отслоение сетчатки, вызванное инъекцией, исследование показало первоначальное улучшение функции палочек и колбочек, что требует дальнейшего изучения.
В 2016 году исследователи были оптимистичны в отношении того, что положительные результаты 32 пациентов с хориидеремией, получавших генную терапию в течение четырех с половиной лет в четырех странах, могут быть долгосрочными.[23]
Преимплантационная генетическая диагностика
Для женщин с мутацией в гене CHM: предимплантационная генетическая диагностика можно использовать во время экстракорпоральное оплодотворение процесс отбора незатронутых эмбрионов для имплантации.[24] Этот вызов процесса можно применить к любому моногенный болезнь.
Другие возможные методы лечения
Хотя хориидеремия - идеальный кандидат для генной терапии[2] есть и другие потенциальные методы лечения, которые могут восстановить зрение после его утраты в более позднем возрасте. Прежде всего это стволовая клетка терапия. Клиническое исследование, опубликованное в 2014 году, показало, что субретинальная инъекция эмбриональные стволовые клетки человека у пациентов с возрастная дегенерация желтого пятна и Болезнь Штаргардта был безопасным и улучшил зрение у большинства пациентов. Из 18 пациентов зрение улучшилось у 10, улучшилось или осталось таким же у 7 и снизилось у 1 пациента, в то время как на необработанных глазах улучшения не наблюдалось. Исследование не обнаружило «никаких доказательств неблагоприятного распространения, отторжения или серьезных глазных или системных проблем безопасности, связанных с трансплантированной тканью».[25][26] В исследовании 2015 г. использовалось CRISPR / Cas9 исправить мутации в полученных от пациентов индуцированные плюрипотентные стволовые клетки которые вызывают пигментный Х-сцепленный ретинит.[27] Это исследование предполагает, что собственные восстановленные клетки пациента могут быть использованы для терапии, что снижает риск иммунного отторжения и этические вопросы которые происходят с использованием эмбриональных стволовых клеток.
Исследование
История
Хориидеремия была впервые описана в 1872 году австрийским офтальмологом, Людвиг Маутнер.[9] Первоначально считалось, что это нарушение развития, которое вызвало отсутствие большей части сосудистой оболочки (отсюда вероятное использование древнегреческого суффикса «эремия», означающего бесплодную землю или пустыню).[9] Спустя несколько десятилетий непрогрессивный характер заболевания был поставлен под сомнение, и в конечном итоге был отвергнут Paymerer et al. в 1960 г.[9][28] В CHM ген был идентифицирован и клонирован в 1990 году Франсом П.М. Кремерс.[29]
Фундаментальные исследования
При многих наследственных заболеваниях сетчатки белок, затронутый мутацией, напрямую участвует в светочувствительной функции глаза, однако это не относится к хориидеремии.[9] REP1 помогает пренилирование G-белков Rab путем связывания и представления их Субъединица рабгеранилгеранилтрансферазы.[30] REP1 также сопровождает пренилированные Rab через цитоплазму, связывая гидрофобный пренил группы и доставляя их к определенной мембране назначения.[30]
У здоровых людей REP1 обнаруживается во всех клетках тела, однако пациенты с хоридеремией испытывают только потерю зрения, а не более широкие системные симптомы (за исключением исследования, в котором были обнаружены кристаллы и жирная кислота аномалии в лейкоциты ).[31] REP2, белок, который на 75% идентичен и на 90% похожий к REP1, способен существенно компенсировать потерю REP1 вне глаза.[9][32] Считается, что REP2 не может полностью компенсировать потерю REP1 в сетчатке.[9] RAB27A, Rab, который выполняет важные функции в сетчатке,[33] было показано, что он предпочтительно пренилируется REP1.[34] Кроме того, Rab27a-REP1 и Rab27a-REP2 комплексы иметь разные родство для фермента Rab геранилгеранилтрансферазы, возможно, объясняя неспособность REP2 полностью компенсировать REP1 в сетчатке.[34]
Культура
Некоторые люди, занимающие общественные должности, страдают хориодермией, а некоторые участвовали в сборе средств на борьбу с этой болезнью. Бывший UK Labor Член парламента Сион Симон заведомо страдает этим заболеванием.[35] Комик и активист Э.Дж. Скотт, партнер Сорвиголова актриса Дебора Энн Уолл, также страдает хоридеремией и регулярно занимается сбором средств.[36][37]
Рекомендации
- ^ а б Кярня, J (1986). «Хориидеремия. Клинико-генетическое исследование 84 финских пациентов и 126 женщин-носителей». Дополнение Acta Ophthalmologica. 176: 1–68. PMID 3014804.
- ^ а б c Робертс, MF; Фишман, Джорджия; Робертс, ДК; Heckenlively, JR; Велебер, Р.Г .; Андерсон, Р.Дж.; Гровер, S (июнь 2002 г.). «Ретроспективное, продольное и поперечное исследование ухудшения остроты зрения при хоридеремии». Британский журнал офтальмологии. 86 (6): 658–62. Дои:10.1136 / bjo.86.6.658. ЧВК 1771148. PMID 12034689.
- ^ Алеман, Т.С.; Вешать; Серрано, LW; Fuerst, NM; Чарлсон, ES; Пирсон, диджей; Чанг, округ Колумбия; Traband, A; Пан, Вт; Инь, GS; Беннетт, Дж; Магуайр, AM; Морган, JI (13 декабря 2016 г.). «Естественная история центральных структурных аномалий при хориидеремии: проспективное поперечное исследование». Офтальмология. 124 (3): 359–373. Дои:10.1016 / j.ophtha.2016.10.022. ЧВК 5319901. PMID 27986385.
- ^ Эбигейл Билл, 2014 г., «Генная терапия восстанавливает зрение у людей с заболеваниями глаз». Новый ученый (онлайн), 16 января 2014 г., см. [1], по состоянию на 21 января 2017 г.
- ^ Дугель, Правин У .; Циммер, Шерил Н .; Шахиди, Айда М. (июль 2016 г.). «Пример носителя хориидеремии - Использование мультиспектральной визуализации для выявления клинических признаков». Американский журнал офтальмологических историй болезни. 2: 18–22. Дои:10.1016 / j.ajoc.2016.04.003. ЧВК 5757363. PMID 29503891.
- ^ Струнникова, Н; Зейн, WM; Сильвин, С; Макдональд, И.М. (2012). Биомаркеры сыворотки и дефекты транспорта в периферических тканях отражают тяжесть ретинопатии у трех братьев, страдающих хоридеремией. Достижения экспериментальной медицины и биологии. 723. С. 381–7. Дои:10.1007/978-1-4614-0631-0_49. ISBN 978-1-4614-0630-3. PMID 22183356.
- ^ Хан, Камрон Н .; Ислам, Фарра; Мур, Энтони Т .; Михаэлидис, Мишель (октябрь 2016 г.). «Клинико-генетические особенности хориидеремии в детстве». Офтальмология (Представлена рукопись). 123 (10): 2158–2165. Дои:10.1016 / j.ophtha.2016.06.051. PMID 27506488.
- ^ а б c d Макдональд, Ян М .; Хьюм, Стейси; Чан, Стефани; Сибра, Мигель С. (26 февраля 2015 г.). «Хороидеремия». GeneReviews. Вашингтонский университет, Сиэтл.
- ^ а б c d е ж грамм Barnard, A.R .; Groppe, M .; Макларен, Р. Э. (30 октября 2014 г.). «Генная терапия хориидеремии с использованием вектора аденоассоциированного вируса (AAV)». Перспективы Колд-Спринг-Харбор в медицине. 5 (3): a017293. Дои:10.1101 / cshperspect.a017293. ЧВК 4355255. PMID 25359548.
- ^ Го, Хуэй; Ли, Джишэн; Гао, Фэй; Ли, Цзянся; У, Синьи; Лю, Цицзи (28 июля 2015 г.). «Секвенирование всего экзома выявляет новую мутацию гена CHM в семье с хориидеремией, первоначально диагностированной как пигментный ретинит». BMC офтальмология. 15 (1): 85. Дои:10.1186 / s12886-015-0081-4. ЧВК 4517409. PMID 26216097.
- ^ Санчес-Алькудиа, Росио; Гарсия-Ойос, Мария; Лопес-Мартинес, Мигель Анхель; Санчес-Боливар, Ноэлия; Зурита, Ольга; Гименес, Вознесение; Вильяверде, Кристина; Родригес-Жаси да Силва, Лучиана; Кортон, Марта; Перес-Карро, Ракель; Торриано, Симона; Калатзис, Василики; Риволта, Карло; Авила-Фернандес, Альмудена; Лорда, Изабель; Трухильо-Тиебас, Мария Дж .; Гарсия-Сандовал, Бланка; Лопес-Молина, Мария Изабель; Бланко-Келли, Фиона; Ривейро-Альварес, Роза; Аюсо, Кармен; Янеке, Андреас Р. (12 апреля 2016 г.). «Комплексный анализ хориидеремии: от генетической характеристики до клинической практики». PLOS ONE. 11 (4): e0151943. Bibcode:2016PLoSO..1151943S. Дои:10.1371 / journal.pone.0151943. ЧВК 4829155. PMID 27070432.
- ^ Фургоч, MJ; Mewes-Arès, J; Радзивон, А; Макдональд, И.М. (25 апреля 2014 г.). «Методы молекулярно-генетической диагностики при хориидеремии». Молекулярное зрение. 20: 535–44. ЧВК 4000712. PMID 24791138.
- ^ Дункан, JL; Алеман, Т.С.; Гарднер, Л. М.; Де Кастро, Э; Маркс, Д.А. Эммонс, Дж. М.; Бибер, ML; Steinberg, JD; Беннетт, Дж; Камень, ЭМ; Макдональд, И. М.; Cideciyan, AV; Магуайр, MG; Якобсон, С.Г. (март 2002 г.). «Макулярный пигмент и добавление лютеина при хориидеремии». Экспериментальные исследования глаз. 74 (3): 371–81. Дои:10.1006 / exer.2001.1126. PMID 12014918.
- ^ а б Паллаб Гош, 2011 г., «Здоровье: генная терапия, используемая для спасения зрения человека», на Новости BBC (онлайн), 27 октября 2011 г., см. [2], по состоянию на 23 апреля 2015 г.
- ^ Cideciyan A. V .; Hauswirth W. W .; Алеман Т. С .; Kaushal S .; Schwartz S. B .; Boye S.L .; Виндзор Э. А. М .; и другие. (2009). «Генная терапия человека RPE65 для лечения врожденного амавроза Лебера: сохранение ранних улучшений зрения и безопасность через 1 год». Генная терапия человека. 20 (9): 999–1004. Дои:10.1089 / hum.2009.086. ЧВК 2829287. PMID 19583479.
- ^ Simonelli F .; Магуайр А. М .; Testa F .; Пирс Э. А .; Mingozzi F .; Bennicelli J. L .; Росси С .; и другие. (2010). «Генная терапия врожденного амавроза Лебера безопасна и эффективна через 1,5 года после введения вектора». Молекулярная терапия. 18 (3): 643–650. Дои:10.1038 / мт.2009.277. ЧВК 2839440. PMID 19953081.
- ^ Магуайр А. М .; Высокий К. А .; Auricchio A .; Райт Дж. Ф .; Пирс Э. А .; Testa F .; Мингоцци Ф .; и другие. (2009). «Возрастозависимые эффекты генной терапии RPE65 при врожденном амаврозе Лебера: испытание фазы 1 с увеличением дозы». Ланцет. 374 (9701): 1597–1605. Дои:10.1016 / S0140-6736 (09) 61836-5. ЧВК 4492302. PMID 19854499.
- ^ Bainbridge J. W. B .; Smith A. J .; Баркер С. С .; Робби С .; Хендерсон Р .; Балагган К .; Вишванатан А .; и другие. (2008). «Влияние генной терапии на зрительную функцию при врожденном амаврозе Лебера». Медицинский журнал Новой Англии. 358 (21): 2231–2239. CiteSeerX 10.1.1.574.4003. Дои:10.1056 / NEJMoa0802268. PMID 18441371.
- ^ MacLaren, RE; Гроппе, М; Барнард, штат Арканзас; Cottriall, CL; Толмачева, Т; Сеймур, L; Кларк, КР; Во время, MJ; Cremers, FP; Черный, GC; Лотери, Эй Джей; Даунс, С.М. Вебстер, штат Арканзас; Сибра, МС (29 марта 2014 г.). «Генная терапия сетчатки у пациентов с хориидеремией: первые результаты клинического исследования фазы 1/2». Ланцет. 383 (9923): 1129–37. Дои:10.1016 / с0140-6736 (13) 62117-0. ЧВК 4171740. PMID 24439297.
- ^ Эбигейл Билл, 2014 г., «Генная терапия восстанавливает зрение у людей с заболеваниями глаз». Новый ученый (онлайн), 16 января 2014 г., см. [3], по состоянию на 23 апреля 2015 г.
- ^ Юэн Каллэуэй, 2008 г., «Успех генной терапии« обращает »слепоту вспять». Новый ученый (онлайн), 28 апреля 2008 г., см. [4] и [5] и [6], по состоянию на 23 апреля 2015 г.
- ^ CT.gov, 2014, «Генная терапия слепоты, вызванной хоридеремией (спонсор: Оксфордский университет): NCT01461213», at ClinicalTrials.gov, видеть [7], по состоянию на 23 апреля 2015 г.
- ^ Гош, Паллаб (28 апреля 2016 г.). «Генная терапия предотвращает потерю зрения и длится долго». BBC News, Наука и окружающая среда. Получено 29 апреля 2016.
- ^ «Преимплантационная генетическая диагностика: (ПГД)». www.americanpregnancy.org. 2012-04-24. Получено 23 июн 2018.
- ^ Шварц, SD; Regillo, CD; Lam, BL; Элиотт, доктор философии; Розенфельд, П.Дж.; Грегори, Новая Зеландия; Hubschman, JP; Дэвис, JL; Heilwell, G; Спирн, М; Магуайр, Дж; Гей, R; Бейтман, Дж; Острик, РМ; Моррис, Д.; Винсент, М; Anglade, E; Del Priore, LV; Ланца, Р. (7 февраля 2015 г.). «Пигментный эпителий сетчатки, полученный из эмбриональных стволовых клеток, у пациентов с возрастной дегенерацией желтого пятна и макулярной дистрофией Штаргардта: наблюдение за двумя открытыми исследованиями фазы 1/2». Ланцет. 385 (9967): 509–16. Дои:10.1016 / с0140-6736 (14) 61376-3. PMID 25458728. S2CID 85799.
- ^ Даффи, Морин. «Обновленные результаты клинических испытаний стволовых клеток при болезни Штаргардта и сухой макулярной дегенерации - блог VisionAware - VisionAware». www.visionaware.org. Получено 23 января 2017.
- ^ Басюк, Александр Г .; Чжэн, Эндрю; Ли, Яо; Цанг, Стивен Х .; Махаджан, Винит Б. (27 января 2016 г.). «Точная медицина: генетическое восстановление пигментного ретинита в стволовых клетках, полученных от пациентов». Научные отчеты. 6: 19969. Bibcode:2016НатСР ... 619969Б. Дои:10.1038 / srep19969. ЧВК 4728485. PMID 26814166.
- ^ Pameyer, J. K .; Waardenburg, P.J .; Хенкес, Х. Э. (1 декабря 1960 г.). «ХОРИДЕРЕМИЯ». Британский журнал офтальмологии. 44 (12): 724–738. Дои:10.1136 / bjo.44.12.724. ISSN 0007-1161. ЧВК 510030. PMID 13732369.
- ^ Cremers, Frans P.M .; van de Pol, Dorien J. R .; ван Керкхофф, Лисбет П. М .; Виеринга, Беренд; Роперс, Ханс-Хильгер (18 октября 1990 г.). «Клонирование гена, который перестраивается у пациентов с хориидеремией». Природа. 347 (6294): 674–677. Bibcode:1990Натура.347..674C. Дои:10.1038 / 347674a0. PMID 2215697. S2CID 4347627.
- ^ а б Пилипенко, О; Рак, А; Reents, R; Никулае, А; Сидорович, В; Cioaca, MD; Бессолицына, Е; Thomä, NH; Waldmann, H; Schlichting, I; Гуди, RS; Александров, К (февраль 2003 г.). «Структура Rab-эскорт-белка-1 в комплексе с Rab геранилгеранилтрансферазой». Молекулярная клетка. 11 (2): 483–94. Дои:10.1016 / с1097-2765 (03) 00044-3. PMID 12620235.
- ^ Чжан А.Ю., Майсур Н., Вали Х., Коенекуп Дж., Цао С. Н., Ли С., Рен Х, Кесер В., Лопес-Солаче И., Сиддики С. Н., Хан А., Муй Дж., Сирс К., Диксон Дж., Шварцентрубер Дж., Маевски Дж., Браверман Н., Коенекоп Р.К. (2015). «Хоридеремия - системное заболевание с кристаллами лимфоцитов и аномалиями липидов плазмы и мембран эритроцитов». Инвестируйте офтальмол Vis Sci. 56 (13): 8158–8165. Дои:10.1167 / iovs.14-15751. ЧВК 4699407. PMID 26720468.
- ^ Cremers, FP; Армстронг, SA; Сибра, МС; Браун, MS; Гольдштейн, Дж. Л. (21 января 1994 г.). «REP-2, белок сопровождения Rab, кодируемый геном, подобным хориидеремии». Журнал биологической химии. 269 (3): 2111–7. PMID 8294464.
- ^ Толмачева, Т; Ramalho, JS; Анант, JS; Шульц, РА; Хаксли, CM; Сибра, МС (18 октября 1999 г.). «Клонирование, картирование и характеристика гена RAB27A человека». Ген. 239 (1): 109–16. Дои:10.1016 / s0378-1119 (99) 00371-6. PMID 10571040.
- ^ а б Лариджани, Б; Хьюм, АН; Тарафдер, АК; Сибра, МС (21 ноября 2003 г.). «Множественные факторы способствуют неэффективному пренилированию Rab27a при заболеваниях пренилирования Rab». Журнал биологической химии. 278 (47): 46798–804. Дои:10.1074 / jbc.m307799200. PMID 12941939.
- ^ "BBC NEWS | Великобритания | Политика | Сион Саймон". news.bbc.co.uk. 2002-10-21. Получено 2017-01-20.
- ^ Билл Дуайр, 2013, «Несмотря на слепоту, Э.Дж. Скотт продолжает смотреть вперед, двигаться вперед». L.A. Times (онлайн), 11 января 2013 г., см. [8], по состоянию на 23 апреля 2015 г.
- ^ E.J. Скотт, 2015, «Это мои 40: бег по 7 континентам за 1 год с завязанными глазами», на Crowdrise (онлайн-краудсорсинг), без даты, см. [9], по состоянию на 23 апреля 2015 г.
дальнейшее чтение
- Дэнни Борен, 2015, «Первое в США клиническое испытание генной терапии для лечения хориидеремии, начатое в Филадельфии», Фонд исследования хориидеремии (онлайн), Резюме пресс-релиза, 20 января 2015 г., см. [10], по состоянию на 23 апреля 2015 г.
- Кори Макдональд, 2015, «Nightstar получает статус орфанного лекарства в США и Европе для генной терапии для лечения хориидеремии», Фонд исследований хориидеремии (онлайн), Резюме пресс-релиза, 24 марта 2015 г. (дата выпуска - 11 января), см. [11], по состоянию на 23 апреля 2015 г.
- FFB, 2015, «Исследование генной терапии хориидеремии на людях в США, начатое компанией Spark Therapeutics», Фонд Борьба со слепотой (онлайн), 27 января 2015 г., см. [12], по состоянию на 23 апреля 2015 г.
- NLO, 2014, «Первые результаты испытаний генной терапии хориидеремии (2014)», Лаборатория офтальмологии Наффилда (онлайн), пресс-релиз, без даты, см. [13], по состоянию на 23 апреля 2015 г.
внешняя ссылка
| Классификация |
|---|
