Ингибитор обратного захвата серотонина и норэпинефрина - Serotonin–norepinephrine reuptake inhibitor
| Ингибитор обратного захвата серотонина и норэпинефрина | |
|---|---|
| Класс препарата | |
 Дулоксетин, пример SNRI. | |
| Идентификаторы класса | |
| Синонимы | Селективный ингибитор обратного захвата серотонина и норадреналина; SNaRI |
| Использовать | Депрессия; Тревога; Боль; Ожирение; Симптомы менопаузы |
| Биологическая мишень | Переносчик серотонина; Транспортер норэпинефрина |
| внешние ссылки | |
| MeSH | D000068760 |
| В Викиданных | |
Ингибиторы обратного захвата серотонина и норэпинефрина (ИОНИИ) являются классом антидепрессант наркотики это лечить сильное депрессивное расстройство (MDD), тревожные расстройства, обсессивно-компульсивное расстройство (ОКР), социофобия, Синдром дефицита внимания и гиперактивности (СДВГ), хронический невропатическая боль, синдром фибромиалгии (ФМС), и менопаузальный симптомы. ИОНИС ингибиторы обратного захвата моноаминов; в частности, они подавлять то обратный захват из серотонин и норэпинефрин. Эти нейротрансмиттеры считается, что они играют важную роль в регулировании настроения. ИОНИС можно противопоставить более широко используемым селективные ингибиторы обратного захвата серотонина (СИОЗС), которые действуют только на серотонин.
Человек переносчик серотонина (SERT) и переносчик норэпинефрина (NET) являются мембранные транспортные белки которые отвечают за обратный захват серотонина и норэпинефрина из синаптическая щель обратно в пресинаптический нервный терминал. Двойное ингибирование обратного захвата серотонина и норадреналина может дать преимущества перед другими антидепрессантами, поскольку лечит более широкий спектр симптомов.[1] Они могут быть особенно полезны при сопутствующем хроническом или невропатическая боль.[2]
ИОЗСН, а также ИОЗС и ингибиторы обратного захвата норэпинефрина (NRIs), являются антидепрессанты второго поколения. За последние два десятилетия антидепрессанты второго поколения просто заменили антидепрессанты первого поколения, такие как трициклические антидепрессанты (TCAs) и ингибиторы моноаминоксидазы (ИМАО) как препараты выбора для лечения БДР благодаря их улучшенной переносимости и профилю безопасности.[3]
Лекарства

В Соединенных Штатах существует восемь одобренных FDA SNRIs, при этом венлафаксин является первым лекарством, разработанным в 1993 году, а левомилнаципран - последним лекарством, разработанным в 2013 году. эффективность.[4]
Годы утверждения для ИОНИС:[4]
- 1993: Венлафаксин
- 1998: Сибутрамин
- 2004 год: дулоксетин
- 2008 год: десвенлафаксин
- 2009: Милнаципран
- 2013: Левомилнаципран
| Медикамент | Название бренда | Показания FDA | Год утверждения | Химическая структура | Заметки |
|---|---|---|---|---|---|
| Атомоксетин | Страттера | 2002 | 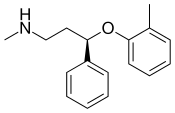 | ИОЗСН с преобладанием норадреналина, используемый для лечения СДВГ и, не по назначению, большая депрессия. Был одобрен FDA в 2002 году. Первоначально считался селективным ингибитор обратного захвата норэпинефрина, но впоследствии исследования показали, что он также значительно подавляет обратный захват серотонина в клинических дозах.[6] | |
| Десвенлафаксин[7] | Пристик Хедезла (ER) |
| 2007 |  | Активный метаболит венлафаксина. Считается, что он действует аналогичным образом, хотя некоторые данные свидетельствуют о более низкой частоте ответа по сравнению с венлафаксином и дулоксетином. Он был введен Уайетом в мае 2008 года и был тогда третьим утвержденным ИОНИС.[8] |
| Дулоксетин[9] | Cymbalta Иренка |
| 2004 |  | Одобрено для лечения депрессии и невропатическая боль в августе 2004 г. Дулоксетин противопоказан пациентам с тяжелым употреблением алкоголя или хроническим заболеванием печени, так как дулоксетин может повышать уровни определенных ферментов печени, что может привести к острым заболеваниям печени. гепатит или другие заболевания у некоторых пациентов из группы риска. В настоящее время риск повреждения печени существует только для пациентов, уже находящихся в группе риска, в отличие от антидепрессантов. нефазодон, которые, хотя и редко, могут спонтанно вызывать печеночную недостаточность у здоровых пациентов.[13] Дулоксетин также одобрен для сильное депрессивное расстройство (MDD), генерализованное тревожное расстройство (ГТР), диабетическая нейропатия, хроническая скелетно-мышечная боль, в том числе хроническая остеоартроз боль и хроническая боль в пояснице.[11] Дулоксетин также подвергается метаболизму в печени и, как было показано, вызывает ингибирование фермента цитохрома P450 в печени. CYP 2D6.[14] С осторожностью следует принимать дулоксетин с другими лекарствами, которые метаболизируются CYP 2D6, поскольку это может спровоцировать потенциальное лекарственное взаимодействие.[14] |
| Левомилнаципран | Фетзима |
| 2013 | 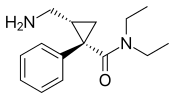 | В левовращающий изомер милнаципрана. Разрабатываемый для лечения депрессии в США и Канаде, он был одобрен FDA для лечения БДР в июле 2013 года. |
| Милнаципран | Иксель Савелла Импульсор |
| 1996 |  | Показано, чтобы быть значительно эффективен при лечении депрессии и фибромиалгии.[15] В Управление по контролю за продуктами и лекарствами (FDA) одобрило милнаципран для лечения фибромиалгии в Соединенных Штатах Америки в январе 2009 года, однако в настоящее время он не одобрен для лечения депрессии в этой стране. Милнаципран коммерчески доступен в Европе и Азии в течение нескольких лет. Впервые он был представлен во Франции в 1996 году. |
| Сибутрамин | Меридия | 1997 |  | SNRI, который вместо того, чтобы разрабатываться для лечения депрессии, широко продавался как подавитель аппетита для потеря веса целей. Сибутрамин был первым лекарством для лечения ожирения, одобренным за 30 лет.[17] Это было связано с учащением сердечно-сосудистых событий и инсультов, а также снято с рынка в нескольких странах и регионах, включая Соединенные Штаты в 2010.[18] | |
| Трамадол | Ультрам |
| 1977 | 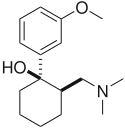 | Двойной слабый опиоид и ИОНИИ. Он был одобрен FDA в 1995 году, хотя продавался в Германия с 1977 г. Препарат применяется для лечения острой и хронической боли. Он показал эффективность при лечении фибромиалгии, хотя специально для этой цели не одобрен. Препарат также исследуется как антидепрессант и для лечения нейропатической боли. По химической структуре он связан с венлафаксином. Из-за того, что он является опиоидом, существует риск злоупотребления и зависимости, но он имеет меньший потенциал злоупотребления, угнетение дыхания и запор по сравнению с другими опиоидами (гидрокодон, оксикодон и т. Д.).[19] |
| Венлафаксин | Эффексор | 1994 |  | Первый и наиболее часто используемый SNRI. Он был представлен Wyeth в 1994 г. Эффекты обратного захвата венлафаксина зависят от дозы. В низких дозах (<150 мг / день) он действует только на серотонинергическую передачу. В умеренных дозах (> 150 мг / день) он действует на серотонинергическую и норадренергическую системы, тогда как в высоких дозах (> 300 мг / день) он также влияет на дофаминергическую нейротрансмиссию.[22] Венлафаксин в малых дозах также эффективен при лечении: вазомоторные симптомы (приливы и ночная потливость) менопаузы и могут быть столь же эффективны, как заместительная гормональная терапия (HRT).[21] |
История
В 1952 г. ипрониазид, антимикобактериальный агент, было обнаружено, что он психоактивный свойства при исследовании в качестве возможного лечения туберкулез. Исследователи отметили, что пациенты, получавшие ипрониазид, стали веселее, оптимистичнее и физически активнее. Вскоре после его разработки было показано, что ипрониазид и родственные ему вещества замедляют ферментативное расщепление серотонина, дофамин, и норэпинефрин через ингибирование фермента моноаминоксидаза. По этой причине этот класс препаратов получил название ингибиторы моноаминоксидазы, или MAOI. В это время также изучалась разработка совершенно разных антидепрессантов. Имипрамин стал первым клинически полезным трициклический антидепрессант (TCA). Было обнаружено, что имипрамин влияет на многочисленные системы нейротрансмиттеров и блокирует обратный захват норадреналина и серотонина из синапс, таким образом увеличивая уровни этих нейромедиаторов. Использование MAOI и TCA дало большие успехи в лечении депрессия но их использование ограничивалось неприятными побочные эффекты и значительная безопасность и токсичность проблемы.[23]
На протяжении 1960-х и 1970-х годов катехоламин Гипотеза эмоции и ее связь с депрессией вызвала большой интерес, и что пониженные уровни определенных нейротрансмиттеров, таких как норадреналин, серотонин и дофамин, могут играть роль в патогенез депрессии. Это привело к развитию флуоксетин, первый СИОЗС. Улучшенный профиль безопасности и переносимости СИОЗС у пациентов с БДР по сравнению с ТЦА и ИМАО представляет собой еще один важный шаг вперед в лечении депрессии.[23]
С конца 1980-х годов на рынке антидепрессантов доминируют СИОЗС. Сегодня наблюдается повышенный интерес к антидепрессантам с более широким механизмы действия это может предложить повышение эффективности и меньшее количество побочных эффектов. В 1993 году на рынке США был представлен новый препарат под названием венлафаксин, ингибитор обратного захвата серотонина-норэпинефрина.[20] Венлафаксин был первым соединением, описанным в новом классе антидепрессивных веществ, называемых фенилэтиламины. Эти вещества не связаны с ТЦА и другими СИОЗС. Венлафаксин блокирует обратный захват нейронами серотонина, норадреналина и, в меньшей степени, дофамин в Центральная нервная система. В отличие от некоторых других антидепрессантов, венлафаксин может вызывать быстрое начало действия, главным образом из-за последующего ингибирования обратного захвата норэпинефрина.[24] См. График на рисунке 1.

Механизм действия
Моноамины связаны с патофизиология депрессии. Симптомы могут возникать из-за недостаточной концентрации нейротрансмиттеров, таких как норэпинефрин и серотонин, что приводит к последующим изменениям.[10][25] Лекарства от депрессии влияют на передачу серотонина, норэпинефрина и дофамина.[10] Более старые и неселективные антидепрессанты, такие как ТЦА и ИМАО, ингибируют обратный захват или метаболизм норадреналина и серотонина в головном мозге, что приводит к более высоким концентрациям нейротрансмиттеров.[25] Антидепрессанты с двойным механизмом действия ингибируют обратный захват как серотонина, так и норадреналина, а в некоторых случаях подавляют обратный захват дофамина со слабым эффектом.[10]Антидепрессанты влияют на различные нейрональные рецепторы, такие как мускарино-холинергические, α1- и α2-адренергический и H1-гистаминергические рецепторы, и натриевые каналы в сердечная мышца, что приводит к снижению сердечной проводимости и кардиотоксичность {необходим источник}. Селективность антидепрессантов основана на нейротрансмиттерах, которые, как считается, влияют на симптомы депрессии.[26]Лекарства, избирательно блокирующие обратный захват серотонина и норэпинефрина, эффективно лечат депрессию и переносятся лучше, чем ТЦА. ТЦА оказывают комплексное воздействие на рецепторы различных нейротрансмиттеров, что приводит к непереносимости и повышенному риску токсичности.[27]
Трициклические антидепрессанты

ТЦА были первыми лекарствами с двойным механизмом действия. Механизм действия трициклических вторичных аминовых антидепрессантов изучен лишь частично. ТЦА оказывают двойное ингибирующее действие на переносчики обратного захвата норэпинефрина и переносчики обратного захвата серотонина. Повышенные концентрации норадреналина и серотонина достигаются путем ингибирования обоих этих белков-переносчиков. ТЦА имеют значительно большее сродство к белкам обратного захвата норэпинефрина, чем СИОЗС. Это происходит из-за образования метаболитов вторичных аминов TCA.[28][29]
Кроме того, ТЦА взаимодействуют с адренорецепторы. Это взаимодействие, по-видимому, является критическим для увеличения доступности норадреналина в синаптических щелях или рядом с ними. Трициклические антидепрессанты, подобные имипрамин-подобным, имеют сложную вторичную адаптацию к их первоначальному и устойчивому действию в качестве ингибиторов транспорта норэпинефрина и различной блокады транспорта серотонина.
Норэпинефрин взаимодействует с подтипами постсинаптических α- и β-адренорецепторов и пресинаптическими α-рецепторами.2 ауторецепторы. Α2 рецепторы включают пресинаптические ауторецепторы которые ограничивают нейрофизиологическую активность норадренергических нейронов в Центральная нервная система. Образование норадреналина снижается за счет ауторецепторы через фермент, ограничивающий скорость тирозингидроксилаза, эффект, опосредованный уменьшением циклический AMP -опосредованный фосфорилирование -активация фермент.[29] α2 рецепторы также вызывают снижение внутриклеточной экспрессии циклического АМФ, что приводит к гладкая мышца расслабление или снижение секреции.[30]
TCAs активируют негативный отзыв механизм через их влияние на пресинаптические рецепторы. Одно из вероятных объяснений влияния на снижение высвобождения нейротрансмиттеров заключается в том, что по мере активации рецепторов происходит ингибирование высвобождения нейромедиаторов (включая подавление потенциал-зависимого Ca2+ токи и активация G-белка, управляемого рецептором K+ токи). Повторное воздействие агентов с этим типом механизма приводит к ингибированию высвобождения нейротрансмиттеров, но повторное введение ТЦА в конечном итоге приводит к снижению ответов α2 рецепторы. десенсибилизация Эти ответы могут быть связаны с повышенным воздействием эндогенного норадреналина или с длительным использованием механизмов транспорта норадреналина (через аллостерический эффект). Адаптация позволяет пресинаптическому синтезу и секреции норэпинефрина возвращаться к нормальным уровням норадреналина в синаптических щелях или даже превышать их. В целом, ингибирование обратного захвата норэпинефрина, индуцированное ТЦА, приводит к снижению частоты возбуждения нейронов (опосредовано через α2 ауторецепторы), метаболическая активность и высвобождение нейротрансмиттеров.[29]
ТЦА не блокируют транспорт дофамина напрямую, но могут косвенно способствовать дофаминергическим эффектам, ингибируя транспорт дофамина в норадренергические терминалы кора головного мозга.[29] Поскольку они влияют на очень много различных рецепторов, ТЦА имеют побочные эффекты, плохую переносимость и повышенный риск токсичности.[27]
Селективные ингибиторы обратного захвата серотонина
Селективные ингибиторы обратного захвата серотонина (СИОЗС) селективно подавляют обратный захват серотонина и представляют собой широко используемую группу антидепрессантов.[31] Повышенная избирательность рецепторов по сравнению с ТЦА позволяет избежать нежелательных эффектов, таких как плохая переносимость.[29] Серотонин синтезируется из аминокислоты, называемой L-триптофан. Активный транспорт система регулирует потребление триптофан через гематоэнцефалический барьер. Серотонинергические пути в мозге подразделяются на два основных пути: восходящие проекции от медиального и дорсального шва и нисходящие проекции от медиального и дорсального шва. хвостовой шов в спинной мозг.
Селективные ингибиторы обратного захвата норэпинефрина
Норадренергические нейроны расположены в двух основных областях мозга. Эти регионы голубое пятно и латеральный тегментальный. При введении СИОЗСН нейрональная активность в области голубого пятна индуцируется из-за повышенной концентрации норэпинефрина в синаптической щели. Это приводит к активации α2 адренорецепторы,[25] как обсуждалось ранее.
Анализы показали, что ИОЗСН обладают незначительной склонностью к МАЧ, α1 и α2 адренергический, или ЧАС1 рецепторы.[26]
Двойные ингибиторы обратного захвата серотонина и норэпинефрина
Агенты с двойным ингибированием обратного захвата серотонина и норадреналина (СИОЗСН) иногда называют нетрициклическими ингибиторами обратного захвата серотонина и норэпинефрина. Клинические исследования показывают, что соединения, которые увеличивают концентрацию в синаптической щели как норэпинефрина, так и серотонина, более эффективны, чем препараты однократного действия при лечении депрессии, но данные не являются окончательными, являются ли СИОЗСН более эффективным вариантом лечения депрессии по сравнению с СИОЗС.[32][33][34] Ингибиторы двойного обратного захвата имеют низкое сродство к нейрональным рецепторам других нейротрансмиттеров, которые имеют низкие побочные эффекты по сравнению с ТЦА. Нетрициклические антидепрессанты обладают улучшенной эффективностью и ускорением начала действия при ответе на антидепрессанты, чем только СИОЗС, что создает впечатление, что синергизм является эффективным свойством в опосредовании антидепрессивной активности.
Нетрициклические ИОЗСН имеют несколько важных отличий, которые основаны на фармакокинетике, метаболизме до активных метаболитов, ингибировании CYP изоформы, эффект лекарственного взаимодействия и период полураспада нетрициклических ИОЗСН.[28][35]
Сочетание механизмов действия в одном активном веществе является важным достижением в психофармакология.[35]
Взаимосвязь структурной деятельности (SAR)
Арилоксипропанаминный каркас
Некоторые ингибиторы обратного захвата содержат арилоксипропанаминовый каркас. Этот структурный мотив имеет потенциал для связывания с высоким сродством с транспортом биогенных аминов.[35] Лекарства, содержащие арилоксипропанаминовый каркас, обладают профилем селективности в отношении переносчиков норэпинефрина и серотонина, который зависит от схемы замещения арилокси-кольца. Селективные NRI содержат заместитель в положении 2 'арилокси-кольца, но SSRI содержат заместитель в положении 4 'арилокси-кольца. Атомоксетин, низоксетин и ребоксетин все имеют группу замещения в положении 2 'и являются селективными NRI, в то время как соединения, которые имеют группу замещения в положении 4' (например, флуоксетин и пароксетин ) являются СИОЗС. Дулоксетин содержит фенильная группа слит в положениях 2 'и 3', поэтому он обладает двойным селективным ингибирующим действием на обратный захват норэпинефрина и серотонина и имеет схожую эффективность для обоих переносчиков.[36] Природа ароматный заместитель также оказывает значительное влияние на активность и селективность соединений в качестве ингибиторов переносчиков серотонина или норэпинефрина.[35]

Циклоалканол этиламин каркас
Венлафаксин и десвенлафаксин содержат циклоалканолэтиламиновый каркас. Повышение электроноакцепторного характера ароматическое кольцо обеспечивает более сильное ингибирующее действие на захват норадреналина и повышает селективность в отношении норадреналина по сравнению с переносчиком серотонина.[36] Были протестированы эффекты хлор-, метокси и трифторметильных заместителей в ароматическом кольце циклоалканолэтиламинового каркаса. Результаты показали, что самые сильные электроноакцепторные м-трифторметиловый аналог проявлял наиболее сильное ингибирующее действие норадреналина и наибольшую селективность в отношении поглощения серотонина.[36] WY-46824, производное, содержащее пиперазин, показало ингибирование обратного захвата норэпинефрина и дофамина. Дальнейший синтез и тестирование выявили WAY-256805, мощный ингибитор обратного захвата норэпинефрина, который проявлял превосходную селективность и был эффективен на животных моделях депрессии, боли и терморегуляторной дисфункции.[37]

Милнаципран

Милнаципран структурно отличается от других SNRI.[28] SAR производных милнаципрана на уровне переносчиков все еще в значительной степени неясен и основан на эффективности in vivo, о которой сообщалось в 1987 году. N-метилирование милнаципрана в группе заместителей R4 и R5 снижает активность норэпинефрина и серотонина.[38] Исследования различных вторичных амидов в группах замещения R6 и R7 показали, что π-электроны играют важную роль во взаимодействии между переносчиками и лигандами. Фенильная группа в заместителе R6 показали влияние на переносчики норадреналина. Группы заместителей в R6 и R7 с участием аллильный двойная связь показала значительно улучшенный эффект как на переносчики норэпинефрина, так и на переносчики серотонина.[38] Исследования показывают, что введение 2-метильной группы в заместитель R3эффективность переносчиков норэпинефрина и серотонина практически отсутствует. Метильные группы в группах заместителей R1 и R2 также отменяют активность переносчиков норадреналина и серотонина. Исследователи обнаружили, что замена одной из этильных групп милнаципрана на аллильную часть увеличивает активность норэпинефрина.[39] В фармакофор производных милнаципрана до сих пор остается неясным.[38]
Конформация милнаципрана является важной частью его фармакофора. Изменение SAR в милнаципране меняет стереохимия соединения и влияет на концентрацию норэпинефрина и серотонина. Милнаципран продается как рацемическая смесь. Действие милнаципрана проявляется в (1S,2р) -изомер и замещение фенильной группы в (1S,2р) -изомер отрицательно влияет на концентрацию норадреналина.[39] Милнаципран имеет низкий молекулярный вес и низкий липофильность. Благодаря этим свойствам милнаципран практически идеален. фармакокинетика у людей, таких как высокие биодоступность, низкая межпредметная вариабельность, ограниченная печень фермент взаимодействие, умеренное распределение тканей и достаточно длительный период полувыведения. Отсутствие межлекарственного взаимодействия милнаципрана через цитохром P450 Ферменты считаются привлекательной особенностью, поскольку многие препараты для центральной нервной системы обладают высокой липофильностью и в основном выводятся из организма ферментами печени.[39]
Будущее развитие SAR
Применение каркаса из арилоксипропанамина привело к появлению ряда сильнодействующих ИМАО.[40] До разработки дулоксетина изучение SAR арилоксипропанамина привело к идентификации флуоксетина и атомоксетина. Тот же мотив можно найти в ребоксетине, где он ограничен морфолин кольцевая система. Были проведены некоторые исследования, в которых кислород в ребоксетине заменен на сера дать арилтиометилморфолин. Некоторые производные арилтиометилморфолина поддерживают высокий уровень ингибирования обратного захвата серотонина и норэпинефрина. Двойное ингибирование обратного захвата серотонина и норэпинефрина находится в различных энантиомерах арилтиометилморфолинового каркаса.[41] Возможные лекарственные препараты-кандидаты с двойной ингибирующей активностью обратного захвата серотонина и норадреналина также были получены из матриц пиперазина, 3-аминопирролидина и бензиламина.[42]
Клинические испытания
Несколько исследований показали, что антидепрессанты, сочетающие серотонинергическую и норадренергическую активность, обычно более эффективны, чем СИОЗС, которые сами по себе действуют на обратный захват серотонина. Серотонинергические-норадренергические антидепрессанты могут иметь небольшое преимущество в эффективности по сравнению с СИОЗС при лечении большого депрессивного расстройства (БДР),[43] но переносятся немного хуже.[44] Необходимы дальнейшие исследования для изучения возможных различий в эффективности этих классов антидепрессантов в отдельных подгруппах пациентов с БДР или в отношении конкретных симптомов БДР.
Данные клинических испытаний показали, что СИОЗСН могут обладать обезболивающими свойствами. Хотя восприятие и передача болевых стимулов в центральной нервной системе полностью не выяснены, обширные данные подтверждают роль серотонина и норэпинефрина в модуляции боли. Результаты клинических испытаний на людях показали, что эти антидепрессанты могут уменьшать боль и снижать функциональные нарушения при центральных и невропатических болевых состояниях. Это свойство SNRIs можно использовать для снижения доз других обезболивающих и снижения частоты проблем с безопасностью, ограниченной эффективностью и переносимостью.[45]Данные клинических исследований показали у пациентов с ГТР, что дулоксетин SNRI значительно более эффективен, чем плацебо, в уменьшении болевых симптомов ГТР после краткосрочного и длительного лечения. Однако полученные данные свидетельствуют о том, что такие симптомы физической боли повторяются в ситуациях рецидива, что указывает на необходимость постоянного лечения пациентов с ГТР и сопутствующими болезненными физическими симптомами.[46]
Показания
ИОЗСН были протестированы для лечения следующих состояний:
- Сильное депрессивное расстройство (MDD)
- Пост-травматическое стрессовое растройство (ПТСР)
- Генерализованное тревожное расстройство (GAD)
- Социальное тревожное расстройство (ПЕЧАЛЬНЫЙ)
- Обсессивно-компульсивное расстройство[47][48][49]
- Паническое расстройство
- Невропатическая боль
- Фибромиалгия
- Хронический скелетно-мышечная боль
Фармакология
Путь введения
ИОЗСН доставляются перорально, обычно в форме капсул или таблеток. Рекомендуется принимать ИОЗСН утром во время завтрака, что не влияет на уровень препарата, но может помочь с некоторыми побочными эффектами.[50] Норэпинефрин оказывает активирующее действие на организм и, следовательно, может вызывать бессонницу у некоторых пациентов, если принимать его перед сном.[51] SNRIs также могут вызывать тошноту, которая обычно бывает легкой и проходит в течение нескольких недель после лечения, но прием лекарства во время еды может помочь облегчить это.[52] Сами лекарства обычно представляют собой мелкокристаллический порошок, который диффундирует в организм во время пищеварения.
Дозировка
Дозировки варьируются в зависимости от используемого ИОЗСН из-за разной активности рассматриваемого лекарства, а также из-за нескольких сильных сторон каждого лекарства.
Способ действия
Считается, что состояние, при котором в основном показаны СИОЗСН, большое депрессивное расстройство, в основном вызвано снижением уровня серотонина и норэпинефрин в синаптической щели, вызывая беспорядочную передачу сигналов. На основе гипотеза моноаминов депрессии, которая утверждает, что снижение концентрации моноаминовых нейромедиаторов приводит к депрессивным симптомам, были определены следующие отношения: «Норэпинефрин может быть связан с бдительностью и энергией, а также с тревогой, вниманием и интересом к жизни; [недостаток] серотонина вызывает беспокойство. , навязчивые идеи и компульсии, а также допамин для внимания, мотивации, удовольствия и вознаграждения, а также интереса к жизни ».[53] ИОНИИ работают подавление то обратный захват нейротрансмиттеров серотонина и норэпинефрина. Это приводит к увеличению внеклеточный концентрации серотонина и норэпинефрина и, как следствие, увеличение нейротрансмиссия. Большинство ИОЗСН, включая венлафаксин, десвенлафаксин и дулоксетин, в несколько раз более селективны в отношении серотонина по сравнению с норадреналином, тогда как милнаципран в три раза более селективен в отношении норадреналина, чем серотонин.Считается, что повышение уровня норэпинефрина необходимо для того, чтобы антидепрессант был эффективным против невропатическая боль, собственность, которую делят со старшими трициклические антидепрессанты (ТЦА), но не с СИОЗС.[54]
Недавние исследования показали, что депрессия может быть связана с усилением воспалительной реакции,[55] таким образом, были предприняты попытки найти дополнительный механизм для SNRI. Исследования показали, что СИОЗС, а также СИОЗС оказывают значительное противовоспалительное действие на микроглия[56] в дополнение к их влиянию на уровень серотонина и норэпинефрина. Таким образом, возможно, что существует дополнительный механизм этих лекарств, который действует в сочетании с ранее понятым механизмом. Смысл этих результатов предполагает использование SNRI в качестве потенциальных противовоспалительных средств после травмы головного мозга или любого другого заболевания, при котором отек мозга является проблемой. Однако, независимо от механизма, эффективность этих препаратов в лечении заболеваний, для которых они показаны, доказана как клинически, так и на практике.[неправильный синтез? ]
Фармакодинамика
Большинство ИОНИС работают вместе первичные метаболиты и вторичные метаболиты для подавления обратного захвата серотонина, норэпинеферина и предельных количеств дофамина. Например, венлафаксин работает вместе со своим основным метаболитом. О-десметилвенлафаксин сильно ингибирует обратный захват серотонина и норадреналина в головном мозге. Имеющиеся данные также предполагают, что дофамин и норадреналин ведут себя ко-транспортирующим образом из-за инактивации дофамина путем обратного захвата норадреналина в организме. лобная кора, область мозга, в которой в значительной степени отсутствуют переносчики дофамина. Этот эффект SNRIs приводит к усилению нейротрансмиссии дофамина в дополнение к увеличению активности серотонина и норадреналина.[57] Кроме того, поскольку SNRIs чрезвычайно избирательны, они не оказывают заметного воздействия на другие, непредусмотренные рецепторы, в отличие от моноаминоксидаза торможение.[58] Фармацевтические испытания показали, что использование как СИОЗС, так и СИОЗС может оказывать значительное противовоспалительное действие на микроглия, также.[56][16][59][60][11][61]
Профили активности
| Соединение | SERT | СЕТЬ | ~ Соотношение (5-HT : NE) | ||
|---|---|---|---|---|---|
| Kя | IC50 | Kя | IC50 | ||
| Венлафаксин | 7.8 | 145 | 1,920 | 1420 | 30:1 |
| Дез-венлафаксин | 40.2 | 47.3 | 558.4 | 531.3 | 14:1 |
| Дулоксетин | 0.07 | 3.7 | 1.17 | 20 | 10:1 |
| Атомоксетин | 87[63] | 5.4 [63] | 0.06:1 (1:16) | ||
| Милнаципран | 8.44 | 151 | 22 | 68 | 1.6:1 |
| Лево-милнаципран | 11.2 | 19.0 | 92.2 | 10.5 | 1:2 |
| Все Kя и IC50 ценности нМ. В 5-HT/NE соотношение на основе IC50 ценности для SERT и СЕТЬ.[62] | |||||
Фармакокинетика
Период полураспада венлафаксин составляет около 5 часов, а при дозировке один раз в день стабильная концентрация достигается примерно через 3 дня, хотя его активный метаболит десвенлафаксин действует дольше.[60] Период полураспада десвенлафаксин составляет около 11 часов, а стабильные концентрации достигаются через 4-5 дней.[59] Период полураспада дулоксетин составляет около 12 часов (диапазон: 8–17 часов), а стабильное состояние достигается примерно через 3 дня.[11] Милнаципран имеет период полураспада от 6 до 8 часов, а стабильный уровень достигается в течение 36-48 часов.[61]
Противопоказания
ИОЗСН противопоказаны пациентам, принимающим MAOI в течение последних двух недель из-за повышенного риска серотониновый синдром, что может быть опасно для жизни.[65] Другие препараты и вещества, которых следует избегать из-за повышенного риска серотонинового синдрома в сочетании с ИОЗСН, включают: антидепрессанты, противосудорожные средства, анальгетики, противорвотные средства, лекарства от мигрени, метиленовый синий, линезолид, Литий, Сусло Святого Иоанна, экстаз, и ЛСД.[65] Признаки и симптомы серотонинового синдрома включают: гипертермию, ригидность, миоклонус вегетативная нестабильность с колебаниями показателей жизненно важных функций и изменения психического статуса, которые включают крайнее возбуждение, переходящее в делирий и кому.[11]
За счет эффектов повышенного норэпинефрин уровни и, следовательно, более высокие норадренергический Активность, ранее существовавшая артериальная гипертензия должна контролироваться до начала лечения с помощью СИОЗСН и периодически контролироваться артериальное давление в течение всего лечения.[66] Дулоксетин также связан со случаями печеночной недостаточности, и его не следует назначать пациентам с хроническим употреблением алкоголя или заболеваниями печени. Исследования показали, что дулоксетин может увеличить функциональные пробы печени в три раза выше их верхнего нормального предела.[67] Пациенты, страдающие ишемическая болезнь сердца следует предостеречь от использования ИОЗСН.[68] Кроме того, из-за действия некоторых SNRIs по борьбе с ожирением пациенты с серьезными расстройствами пищевого поведения, такими как нервная анорексия или булимия не следует назначать ИОЗСН.[16] Дулоксетин и милнаципран также противопоказаны пациентам с неконтролируемой узкоугольной глаукомой, поскольку, как было показано, они увеличивают частоту мидриаз.[11][61]
Побочные эффекты
Поскольку СИОЗСН и СИОЗС действуют аналогичным образом, повышая уровень серотонина, они имеют много побочных эффектов, хотя и в разной степени. Наиболее частые побочные эффекты включают тошноту / рвоту, потоотделение, потерю аппетита, головокружение, головную боль, усиление суицидальных мыслей и сексуальную дисфункцию.[69] Повышение уровня норадреналина иногда может вызывать беспокойство, слегка учащенный пульс и повышенное кровяное давление. Однако селективные к норэпинефрину антидепрессанты, такие как ребоксетин и дезипрамин, успешно лечат тревожные расстройства.[70] Люди с риском гипертонии и сердечных заболеваний должны следить за своим кровяным давлением.[16][59][60][11][61] Побочные эффекты расстройства желудка можно уменьшить, если принимать СИОЗН с пищей.
Сексуальная дисфункция
СИОЗС, как и СИОЗС, могут вызывать несколько типов сексуальной дисфункции, такие как эректильная дисфункция, снижение либидо, половая дисфункция. ангедония, и аноргазмия.[71][72][73] Два общих сексуальных побочных эффекта - это снижение интереса к сексу (либидо) и трудности с достижением оргазма (аноргазмия ), которые обычно несколько мягче при использовании СИОЗС по сравнению с СИОЗС.[74] Исследования показали, что для управления сексуальной дисфункцией переход на бупропион или добавив Ингибитор PDE5 уменьшились симптомы сексуальной дисфункции.[75] Исследования показали, что ингибиторы PDE5, такие как силденафил (Виагра), тадалафил (Сиалис), варденафил (Левитра) и аванафил (Стендра), иногда были полезны для уменьшения сексуальной дисфункции, включая эректильную дисфункцию, хотя было показано, что они более эффективны у мужчин, чем у женщин.[75]
Серотониновый синдром
Серьезным, но редким побочным эффектом СИОЗСН является серотониновый синдром, который вызывается избытком серотонина в организме. Серотониновый синдром может быть вызван приемом нескольких серотонинергических препаратов, таких как СИОЗС или СИОЗСН. Другие препараты, которые способствуют развитию серотонинового синдрома, включают ингибиторы МАО, линезолид, тедизолид, метиленовый синий, прокарбазин, амфетамины, кломипрамин и другие.[76] Ранние симптомы серотонинового синдрома могут включать тошноту, рвоту, диарею, потоотделение, возбуждение, спутанность сознания, ригидность мышц, расширение зрачков, гипертермию, ригидность и мурашки по коже. Более серьезные симптомы включают лихорадку, судороги, нерегулярное сердцебиение, делирий и кому.[77][78][11] При появлении признаков или симптомов немедленно прекратите лечение серотонинергическими агентами.[77] Перед применением ингибитора МАО рекомендуется вымыть от 4 до 5 периодов полувыведения серотонинергического агента.[79]
Кровотечение
Некоторые исследования предполагают, что существует риск кровотечения из верхних отделов желудочно-кишечного тракта, особенно венлафаксина, из-за нарушения агрегации тромбоцитов и снижения уровня серотонина тромбоцитов.[80][81] Подобно СИОЗС, СИОЗС могут взаимодействовать с антикоагулянты, любить варфарин. В настоящее время существует больше доказательств того, что СИОЗС имеют более высокий риск кровотечения, чем СИОЗСН.[80] Исследования показали осторожность при использовании СИОЗСН или СИОЗС с высокими дозами нестероидные противовоспалительные препараты (НПВП), такие как ибупрофен или напроксен из-за повышенного риска кровотечения из верхних отделов ЖКТ.[34]
Меры предосторожности
Начало режима SNRI
Из-за резких изменений норадренергической активности, вызванной ингибированием обратного захвата норэпинефрина и серотонина, пациентам, которые только начинают принимать СИОЗСН, обычно назначают более низкие дозы, чем их ожидаемая конечная доза, чтобы позволить организму адаптироваться к действию препарата. По мере того как пациент продолжает прием низких доз без каких-либо побочных эффектов, дозу постепенно увеличивают до тех пор, пока пациент не увидит улучшение симптомов без вредных побочных эффектов.[82]
Синдром отмены
Как и в случае с СИОЗС, резкое прекращение приема ИОЗСН обычно приводит к вывод, или "синдром отмены ", который может включать состояния беспокойство и другие симптомы. Поэтому пользователям, желающим прекратить прием ИОЗСН, рекомендуется медленно снижать дозу под наблюдением профессионала. Сообщается, что синдром отмены значительно ухудшается при венлафаксин по сравнению с другими ИОНИС. Как, например трамадол относится к венлафаксину, применяются те же условия.[83] Вероятно, это связано с относительно коротким сроком действия венлафаксина. период полураспада и, следовательно, быстрое разрешение после прекращения приема. В некоторых случаях для уменьшения симптомов отмены может быть рекомендован переход с венлафаксина на флуоксетин, СИОЗС длительного действия, а затем постепенное снижение дозы флуоксетина.[84][85] Признаки и симптомы отмены при резком прекращении приема СИОЗСН включают головокружение, беспокойство, бессонницу, тошноту, потоотделение и гриппоподобные симптомы, такие как вялость и недомогание.[86]
Передозировка
Причины
Передозировка СИОЗСН может быть вызвана комбинацией лекарств или чрезмерным количеством самого препарата. Венлафаксин незначительно более токсичен при передозировке, чем дулоксетин или СИОЗС.[16][59][60][11][61][87] Риск передозировки увеличивается у пациентов, принимающих несколько серотонинергических агентов или взаимодействующих агентов.
Симптомы
Симптомы передозировки СИОЗСН, будь то смешанное лекарственное взаимодействие или одно лекарственное средство, различаются по интенсивности и частоте в зависимости от количества принимаемого лекарства и индивидуальной чувствительности к лечению СИОЗСН. Возможные симптомы могут включать:[11]
Управление
Передозировка обычно лечится симптоматически, особенно в случае серотонинового синдрома, который требует лечения ципрогептадином и контроля температуры в зависимости от прогрессирования токсичности серотонина.[88] Пациенты часто контролируются на предмет жизненно важных функций и очищения дыхательных путей, чтобы убедиться, что они получают достаточный уровень кислорода. Другой вариант - использовать активированный уголь в желудочно-кишечном тракте, чтобы поглотить избыток нейромедиатора.[11] При работе с пациентами с передозировкой важно учитывать лекарственные взаимодействия, поскольку могут возникать отдельные симптомы.
Сравнение с СИОЗС
Поскольку СИОЗС были разработаны позже, чем СИОЗС, их относительно немного. Однако сегодня ИОЗСН являются одними из наиболее широко используемых антидепрессантов. В 2009 году Цимбалта и Эффексор занимали 11-е и 12-е место по количеству назначаемых брендовых препаратов в США соответственно. Это означает 2-й и 3-й по популярности антидепрессанты после Lexapro (эсциталопрам ), СИОЗС.[89] В некоторых исследованиях СИОЗС продемонстрировали немного более высокую антидепрессивную эффективность, чем СИОЗС (частота ответа 63,6% против 59,3%).[43] Однако в одном исследовании эсциталопрам имел более высокий профиль эффективности по сравнению с венлафаксином.[90]
Особые группы населения
Беременность
В настоящее время антидепрессанты во время беременности не одобрены FDA. Все СИОЗС и ИОЗСН относятся к Категории C, за исключением пароксетина, который относится к Категории D, поскольку он показал связь с врожденными пороками сердца.[91] Использование антидепрессантов во время беременности может привести к аномалиям плода, влияющим на функциональное развитие мозга и поведение.[91] Нелеченная депрессия также может повлиять на исход родов, поэтому рекомендуется обсудить варианты с врачом, чтобы взвесить риски и преимущества.
Педиатрия
СИОЗС и СИОЗС показали свою эффективность при лечении большого депрессивного расстройства и тревоги в педиатрической популяции.[92] Однако существует риск повышенного суицидального поведения в педиатрической популяции при лечении большого депрессивного расстройства, особенно венлафаксином.[92] Флуоксетин - единственный антидепрессант, одобренный для лечения большого депрессивного расстройства у детей / подростков.[93]
Гериатрия
Большинство антидепрессантов, включая СИОЗСН, безопасны и эффективны для гериатрической популяции. Решения часто основываются на сопутствующих заболеваниях, лекарственном взаимодействии и терпимости пациента. Из-за различий в составе тела и обмене веществ начальная доза часто вдвое меньше рекомендованной дозы для молодых людей.[94]
Смотрите также
- Ингибитор обратного захвата моноаминов
- Список антидепрессантов
- Агент, высвобождающий серотонин
- Селективный ингибитор обратного захвата серотонина (СИОЗС)
- Отмена наркотиков
- Серотониновый синдром
- Сексуальная дисфункция
использованная литература
- ^ Кэшман Дж. Р., Гирмаи С. (октябрь 2009 г.). «Ингибирование обратного захвата серотонина и норэпинефрина и ингибирование фосфодиэстеразы с помощью многоцелевых ингибиторов как потенциальных агентов для депрессии». Биоорганическая и медицинская химия. 17 (19): 6890–7. Дои:10.1016 / j.bmc.2009.08.025. PMID 19740668.
- ^ Райт, Меган Э .; Риццоло, Дениз (март 2017). «Обновленная информация о фармакологическом управлении и лечении невропатической боли». Журнал Американской академии PA. 30 (3): 13–17. Дои:10.1097 / 01.JAA.0000512228.23432.f7. ISSN 1547-1896. PMID 28151738.
- ^ Спина Е., Санторо В., Д'Арриго С. (июль 2008 г.). «Клинически значимые фармакокинетические лекарственные взаимодействия с антидепрессантами второго поколения: обновление». Клиническая терапия. 30 (7): 1206–27. Дои:10.1016 / S0149-2918 (08) 80047-1. PMID 18691982.
- ^ а б Hillhouse TM, Портер JH (февраль 2015 г.). «Краткая история разработки антидепрессантов: от моноаминов до глутамата». Экспериментальная и клиническая психофармакология. 23 (1): 1–21. Дои:10.1037 / a0038550. ЧВК 4428540. PMID 25643025.
- ^ «Капсулы Strattera (атомоксетин) для перорального применения. Полная информация по назначению» (PDF). Lilly USA, LLC, Индианаполис, IN 46285, США. Получено 29 августа 2016.
- ^ Динг Ю.С., Наганава М., Галлезот Дж. Д., Набулси Н., Лин С.Ф., Ропчан Дж. И др. (Февраль 2014 года). «Клинические дозы атомоксетина значительно влияют на транспорт норэпинефрина и серотонина: влияние на лечение депрессии и СДВГ». NeuroImage. 86: 164–71. Дои:10.1016 / j.neuroimage.2013.08.001. PMID 23933039.
- ^ а б Дичер, округ Колумбия, Бейер С.Э., Джонстон Дж., Брей Дж., Шах С., Абу-Гарбия М., Андре Т.Х. (август 2006 г.). «Десвенлафаксина сукцинат: новый ингибитор обратного захвата серотонина и норэпинефрина». Журнал фармакологии и экспериментальной терапии. 318 (2): 657–65. Дои:10.1124 / jpet.106.103382. PMID 16675639.
- ^ а б Перри Р., Кассаньол М (июнь 2009 г.). «Десвенлафаксин: новый ингибитор обратного захвата серотонина и норэпинефрина для лечения взрослых с большим депрессивным расстройством». Клиническая терапия. 31 Pt 1 (1): 1374–404. Дои:10.1016 / j.clinthera.2009.07.012. PMID 19698900.
- ^ Айенгар С., Вебстер А.А., Хемрик-Люке С.К., Сюй Дж.Й., Симмонс Р.М. (ноябрь 2004 г.). «Эффективность дулоксетина, мощного и сбалансированного ингибитора обратного захвата серотонина-норэпинефрина в моделях стойкой боли у крыс». Журнал фармакологии и экспериментальной терапии. 311 (2): 576–84. Дои:10.1124 / jpet.104.070656. PMID 15254142.
- ^ а б c d Hunziker ME, Suehs BT, Bettinger TL, Crismon ML (август 2005 г.). «Дулоксетина гидрохлорид: новый препарат двойного действия для лечения большого депрессивного расстройства». Клиническая терапия. 27 (8): 1126–43. Дои:10.1016 / j.clinthera.2005.08.010. PMID 16199241.
- ^ а б c d е ж г час я j k «Цимбалта (дулоксетин с отсроченным высвобождением), капсулы для перорального применения. Полная информация по назначению» (PDF). Lilly USA, LLC, Индианаполис, IN 46285, США. Получено 29 августа 2016.
- ^ "Yentreve (гидрохлорид дулоксетина) Твердые гастрорезистентные капсулы. Краткое описание характеристик продукта" (PDF). Европейское агентство по лекарствам. Получено 29 августа 2016.
- ^ «Таблетки Нефазодона гидрохлорида. Полная информация по назначению». DailyMed. Teva Pharmaceuticals USA, Inc. Северный Уэльс, Пенсильвания 19454. Сентябрь 2015 г.. Получено 2 сентября 2016.
- ^ а б Фрэмптон Дж. Э., Плоскер Г. Л. (2007). «Дулоксетин: обзор его использования в лечении большого депрессивного расстройства». Препараты ЦНС. 21 (7): 581–609. Дои:10.2165/00023210-200721070-00004. PMID 17579500.
- ^ а б Моришита С., Арита С. (февраль 2003 г.). «Клиническое применение милнаципрана при депрессии». Европейская психиатрия. 18 (1): 34–5. Дои:10.1016 / S0924-9338 (02) 00003-2. PMID 12648895.
- ^ а б c d е «Меридиа (моногидрат гидрохлорида сибутрамина), капсулы C-IV. Полная информация по назначению (заархивированная этикетка)». Abbott Laboratories, Северный Чикаго, Иллинойс 60064, США. Получено 2 сентября 2016.
- ^ Luque CA, Rey JA (апрель 2002 г.). «Открытие и статус сибутрамина как лекарства от ожирения». Европейский журнал фармакологии. 440 (2–3): 119–28. Дои:10.1016 / S0014-2999 (02) 01423-1. PMID 12007530.
- ^ Rockoff JD, Dooren JC (8 октября 2010 г.). "Abbott убирает с полок в США диетические препараты Meridia". Журнал "Уолл Стрит. Получено 8 октября 2010.
- ^ Китинг GM (2006). «Капсулы с замедленным высвобождением трамадола». Наркотики. 66 (2): 223–30. Дои:10.2165/00003495-200666020-00006. PMID 16451094.
- ^ а б Gutierrez MA, Stimmel GL, Aiso JY (август 2003 г.). «Венлафаксин: обновление 2003 года». Клиническая терапия. 25 (8): 2138–54. Дои:10.1016 / s0149-2918 (03) 80210-2. PMID 14512125.
- ^ а б Джоффе Х., Гатри К.А., Лакруа А.З., Рид С.Д., Энсруд К.Э., Мэнсон Дж.Э. и др. (Июль 2014 г.). «Низкие дозы эстрадиола и венлафаксина, ингибитора обратного захвата серотонина и норэпинефрина при вазомоторных симптомах: рандомизированное клиническое испытание». JAMA Internal Medicine. 174 (7): 1058–66. Дои:10.1001 / jamainternmed.2014.1891. ЧВК 4179877. PMID 24861828.
- ^ Redrobe JP, Bourin M, Colombel MC, Baker GB (июль 1998 г.). «Дозозависимые норадренергические и серотонинергические свойства венлафаксина на животных моделях, указывающие на антидепрессивную активность». Психофармакология. 138 (1): 1–8. Дои:10.1007 / s002130050638. PMID 9694520.
- ^ а б Либерман Я.А. (2003). «История использования антидепрессантов в первичной медико-санитарной помощи» (PDF). Помощник по первичной медицинской помощи J Clin Psychiatry. 5 (S7): 6–10.
- ^ Руэлас Э.Г., Диас-Мартинес А., Руис Р.М., Study TV, Группа C (1997). «Открытая оценка приемлемости, эффективности и переносимости венлафаксина в обычных условиях лечения». Текущие терапевтические исследования. 58 (9): 609–630. Дои:10.1016 / S0011-393X (97) 80088-4.
- ^ а б c Грандосо Л., Пинеда Дж., Угедо Л. (май 2004 г.). «Сравнительное исследование эффектов дезипрамина и ребоксетина на нейроны голубого пятна в срезах мозга крысы». Нейрофармакология. 46 (6): 815–23. Дои:10.1016 / j.neuropharm.2003.11.033. PMID 15033341.
- ^ а б Брунелло Н., Мендлевич Дж., Каспер С., Леонард Б., Монтгомери С., Нельсон Дж. И др. (Октябрь 2002 г.). «Роль норадреналина и селективного ингибирования обратного захвата норадреналина при депрессии» (PDF). Европейская нейропсихофармакология. 12 (5): 461–75. Дои:10.1016 / s0924-977x (02) 00057-3. PMID 12208564.
- ^ а б Шталь С.М., Грейди М.М., Морет С., Брайли М. (сентябрь 2005 г.). «ИОЗСН: их фармакология, клиническая эффективность и переносимость по сравнению с другими классами антидепрессантов». Спектры ЦНС. 10 (9): 732–47. Дои:10.1017 / S1092852900019726. PMID 16142213.
- ^ а б c Лемке Т.Л., Уильямс Д.А., Рош В.Ф., Зито С.В. (2008). Принципы медицинской химии Фуа (6-е изд.). США: Липпинкотт Уильямс и Уилкинс. С. 547–67, 581–582.
- ^ а б c d е Brunton, L.L .; Lazo, J.S .; Паркер, К.Л., ред. (2006). Goodman & Gilman's: Фармакологическая основа терапии (11-е изд.). Нью-Йорк: Макгроу-Хилл.
- ^ Сильверторн, Д.У., изд. (2007). Физиология человека (4-е изд.). Сан-Франциско: Пирсон. С. 383–384.
- ^ Nutt DJ, Forshall S, Bell C, Rich A, Sandford J, Nash J, Argyropoulos S (июль 1999 г.). «Механизмы действия селективных ингибиторов обратного захвата серотонина в лечении психических расстройств». Европейская нейропсихофармакология. 9 Дополнение 3: S81-6. Дои:10.1016 / S0924-977X (99) 00030-9. PMID 10523062.
- ^ Сантарсиери, Даниэль; Шварц, Томас Л. (2015-10-08). «Эффективность антидепрессантов и бремя побочных эффектов: краткое руководство для врачей». Наркотики в контексте. 4: 212290. Дои:10.7573 / dic.212290. ISSN 1745-1981. ЧВК 4630974. PMID 26576188.
- ^ Клевенджер, Стивен С .; Мальхотра, Девврат; Данг, Джонатан; Ванле, Бриджит; Исхак, Вагих Уильям (2018). «Роль селективных ингибиторов обратного захвата серотонина в предотвращении рецидива большого депрессивного расстройства». Терапевтические достижения в психофармакологии. 8 (1): 49–58. Дои:10.1177/2045125317737264. ISSN 2045-1253. ЧВК 5761909. PMID 29344343.
- ^ а б Зейнд, Кэролайн; Карвалью (2018). Прикладная терапия: клиническое использование лекарств, 11e. Wolters Kluwer. С. 1813–1833. ISBN 9781496318299.
- ^ а б c d Boot J, Cases M, Clark BP, Findlay J, Gallagher PT, Hayhurst L, et al. (Февраль 2005 г.). «Открытие и взаимосвязь между структурой и активностью нового селективного норадреналина и двойных ингибиторов обратного захвата серотонина / норэпинефрина». Письма по биоорганической и медицинской химии. 15 (3): 699–703. Дои:10.1016 / j.bmcl.2004.11.025. PMID 15664840.
- ^ а б c Махани П.Е., Ву А.Т., МакКомас С.К., Чжан П., Ногле Л.М., Уоттс В.Л. и др. (Декабрь 2006 г.). «Синтез и активность нового класса ингибиторов обратного захвата норэпинефрина и серотонина двойного действия: 3- (1H-индол-1-ил) -3-арилпропан-1-аминов». Биоорганическая и медицинская химия. 14 (24): 8455–66. Дои:10.1016 / j.bmc.2006.08.039. PMID 16973367.
- ^ Махани П.Е., Гаврин Л.К., Трибульски Э.Дж., Стек Г.П., Ву Т.А., Кон С.Т. и др. (Июль 2008 г.). «Взаимосвязь между структурой и активностью циклоалканолэтиламинового каркаса: открытие селективных ингибиторов обратного захвата норэпинефрина». Журнал медицинской химии. 51 (13): 4038–49. Дои:10.1021 / jm8002262. PMID 18557608.
- ^ а б c Чен С., Дайк Б., Флек Б.А., Фостер А.С., Грей Дж., Йович Ф. и др. (Февраль 2008 г.). «Исследования SAR и фармакофора производных милнаципрана в качестве ингибиторов переносчиков моноаминов». Письма по биоорганической и медицинской химии. 18 (4): 1346–9. Дои:10.1016 / j.bmcl.2008.01.011. PMID 18207394.
- ^ а б c Тамия Дж., Дайк Б., Чжан М., Фан К., Флек Б.А., Апарисио А. и др. (Июнь 2008 г.). «Идентификация аналогов 1S, 2R-милнаципрана как сильнодействующих ингибиторов переносчиков норэпинефрина и серотонина». Письма по биоорганической и медицинской химии. 18 (11): 3328–32. Дои:10.1016 / j.bmcl.2008.04.025. PMID 18445525.
- ^ Ву А.Т., Кон С.Т., Терефенко Е.А., Мур В.Дж., Чжан П., Махани П.Е. и др. (Май 2009 г.). «3- (Ариламино) -3-фенилпропан-2-оламины как новая серия двойных ингибиторов обратного захвата норэпинефрина и серотонина». Письма по биоорганической и медицинской химии. 19 (9): 2464–7. Дои:10.1016 / j.bmcl.2009.03.054. PMID 19329313.
- ^ Boot JR, Brace G, Delatour CL, Dezutter N, Fairhurst J, Findlay J и др. (Ноябрь 2004 г.). «Бензотиенилоксифенилпропанамины, новые двойные ингибиторы обратного захвата серотонина и норэпинефрина». Письма по биоорганической и медицинской химии. 14 (21): 5395–9. Дои:10.1016 / j.bmcl.2004.08.005. PMID 15454233.
- ^ Fish PV, Deur C, Gan X, Greene K, Hoople D, Mackenny M и др. (Апрель 2008 г.). «Дизайн и синтез производных морфолина. SAR для двойного ингибирования обратного захвата серотонина и норадреналина». Письма по биоорганической и медицинской химии. 18 (8): 2562–6. Дои:10.1016 / j.bmcl.2008.03.050. PMID 18387300.
- ^ а б Папакостас Г.И., Тасе М.Э., Фава М., Нельсон Дж. К., Шелтон Р. К. (декабрь 2007 г.). «Являются ли антидепрессанты, сочетающие серотонинергический и норадренергический механизмы действия, более эффективными, чем селективные ингибиторы обратного захвата серотонина, при лечении большого депрессивного расстройства? Метаанализ исследований новых агентов». Биологическая психиатрия. 62 (11): 1217–27. Дои:10.1016 / j.biopsych.2007.03.027. PMID 17588546.
- ^ Nemeroff CB, Thase ME (2007). «Двойное слепое плацебо-контролируемое сравнение лечения венлафаксином и флуоксетином у амбулаторных пациентов с депрессией». Журнал психиатрических исследований. 41 (3–4): 351–9. Дои:10.1016 / j.jpsychires.2005.07.009. PMID 16165158.
- ^ Marks DM, Shah MJ, Patkar AA, Masand PS, Park GY, Pae CU (декабрь 2009 г.). «Ингибиторы обратного захвата серотонина и норэпинефрина для контроля боли: предпосылка и обещание». Современная нейрофармакология. 7 (4): 331–6. Дои:10.2174/157015909790031201. ЧВК 2811866. PMID 20514212.
- ^ Бисдо К., Хартфорд Дж., Рассел Дж., Спанн М., Болл С., Витчен Х.У. (декабрь 2009 г.). «Краткосрочное и долгосрочное влияние дулоксетина на болезненные физические симптомы у пациентов с генерализованным тревожным расстройством: результаты трех клинических испытаний». Журнал тревожных расстройств. 23 (8): 1064–71. Дои:10.1016 / j.janxdis.2009.07.008. PMID 19643572.
- ^ «Международный фонд ОКР | Лекарства от ОКР». Международный фонд ОКР. Получено 2020-04-18.
- ^ Издательство, Harvard Health. «Спросите доктора Роба об ОКР». Гарвардское Здоровье. Получено 2020-04-18.
- ^ Sansone, Randy A .; Сансоне, Лори А. (2011). "Фармакологические альтернативы SNRI для лечения обсессивно-компульсивного расстройства?". Инновации в клинической неврологии. 8 (6): 10–14. ISSN 2158-8333. ЧВК 3140892. PMID 21779536.
- ^ Troy, S.M .; Паркер, В. П .; Hicks, D. R .; Pollack, G.M .; Чан, С. Т. (октябрь 1997 г.). «Фармакокинетика и влияние пищи на биодоступность перорального венлафаксина». Журнал клинической фармакологии. 37 (10): 954–961. Дои:10.1002 / j.1552-4604.1997.tb04270.x. ISSN 0091-2700. PMID 9505987.
- ^ Wichniak A, Wierzbicka A, Walęcka M, Jernajczyk W (август 2017 г.). «Влияние антидепрессантов на сон». Текущие отчеты психиатрии. 19 (9): 63. Дои:10.1007 / s11920-017-0816-4. ЧВК 5548844. PMID 28791566.
- ^ «Полезен при хронической боли в дополнение к депрессии». Клиника Майо. Получено 2019-10-24.
- ^ Натт DJ (2008). «Связь нейромедиаторов с симптомами большого депрессивного расстройства». Журнал клинической психиатрии. 69 Дополнение E1: 4–7. PMID 18494537.
- ^ Синдруп С.Х., Отто М., Финнеруп Н.Б., Йенсен Т.С. (июнь 2005 г.). «Антидепрессанты в лечении невропатической боли». Фундаментальная и клиническая фармакология и токсикология. 96 (6): 399–409. Дои:10.1111 / j.1742-7843.2005.pto_96696601.x. PMID 15910402.
- ^ Шелтон Р.К., Миллер А.Х. (2011). «Воспаление при депрессии: является ли причиной ожирения?». Диалоги в клинической неврологии. 13 (1): 41–53. ЧВК 3181969. PMID 21485745.
- ^ а б Тайнан Р.Дж., Вайденхофер Дж., Хинвуд М., Кэрнс М.Дж., Day TA, Walker FR (март 2012 г.). «Сравнительное исследование противовоспалительного действия антидепрессантов СИОЗС и СИОЗСН на микроглию, стимулированную ЛПС». Мозг, поведение и иммунитет. 26 (3): 469–79. Дои:10.1016 / j.bbi.2011.12.011. PMID 22251606.
- ^ http://stahlonline.cambridge.org/prescribers_drug.jsf?page=9781107675025c127.html.therapeutics&name=Venlafaxine&title=Therapeutics
- ^ Ламберт О., Бурин М. (ноябрь 2002 г.). «ИОЗСН: механизм действия и клинические особенности». Экспертный обзор нейротерапии. 2 (6): 849–58. Дои:10.1586/14737175.2.6.849. PMID 19810918.
- ^ а б c d «Таблетки с расширенной высвобождением Pristiq (десвенлафаксин) для перорального применения. Полная информация по назначению». Wyeth Pharmaceuticals, Inc. Дочерняя компания Pfizer, Inc. Филадельфия, Пенсильвания, 19101. Июль 2016 г.. Получено 2 сентября 2016.
- ^ а б c d «Эффексор XR (венлафаксин) капсулы с расширенным высвобождением. Полная информация по назначению». Wyeth Pharmaceuticals, Inc. Дочерняя компания Pfizer, Inc. Филадельфия, Пенсильвания, 19101. Август 2015 г.. Получено 2 сентября 2016.
- ^ а б c d е «Таблетки Savella (милнаципран HCl). Полная информация по назначению». Allergan USA, Inc. Ирвин, Калифорния 92612. Август 2016 г.. Получено 2 сентября 2016.
- ^ а б Рауф М., Глоговски А.Дж., Беттингер Дж. Дж., Фудин Дж. (Август 2017 г.). «Ингибиторы обратного захвата серотонина-норэпинефрина и влияние аффинности связывания (Ki) на обезболивание». Журнал клинической фармации и терапии. 42 (4): 513–517. Дои:10.1111 / jcpt.12534. PMID 28503727.
- ^ а б c Упадхьяя HP, Desaiah D, Schuh KJ, Bymaster FP, Kallman MJ, Clarke DO и др. (Март 2013 г.). «Обзор оценки потенциала злоупотребления атомоксетином: нестимулирующим препаратом для лечения синдрома дефицита внимания / гиперактивности». Психофармакология. Springer Nature. 226 (2): 189–200. Дои:10.1007 / s00213-013-2986-z. ЧВК 3579642. PMID 23397050.
- ^ Рот Б.Л., Дрискол Дж. (Декабрь 2012 г.). «ПДСП Кя База данных". Программа скрининга психоактивных веществ (PDSP). Университет Северной Каролины в Чапел-Хилл и Национальный институт психического здоровья США. Получено 7 июля 2018.
- ^ а б Бойер Э.В., Шеннон М. (март 2005 г.). «Серотониновый синдром». Медицинский журнал Новой Англии. 352 (11): 1112–20. Дои:10.1056 / NEJMra041867. PMID 15784664.
- ^ Чжун, Чжуоюань; Ван, Лимин; Вэнь Сяоцзюнь; Лю, Юньюнь; Фан, Яфэй; Лю, Чжунлинь (2017-11-07). «Мета-анализ эффектов селективных ингибиторов обратного захвата серотонина на артериальное давление при лечении депрессии: результаты контролируемых испытаний плацебо и ингибиторов обратного захвата серотонина и норадреналина». Психоневрологические заболевания и лечение. 13: 2781–2796. Дои:10.2147 / NDT.S141832. ISSN 1176-6328. ЧВК 5683798. PMID 29158677.
- ^ McIntyre RS et al. Профиль безопасности дулоксетина для печени: обзор. Мнение эксперта Drug Metab Toxicol. 2008;4(3):281–285.
- ^ Младенка, Пршемысл; Апплова, Ленка; Паточка, Иржи; Коста, Вера Мариса; Ремиао, Фернандо; Пурова, Яна; Младенка, Алеш; Карличкова, Яна; Ягодарж, Лудек; Вопршалова, Мария; Варнер, Курт Дж. (Июль 2018 г.). «Комплексный обзор сердечно-сосудистой токсичности лекарств и родственных агентов». Обзоры медицинских исследований. 38 (4): 1332–1403. Дои:10.1002 / med.21476. ISSN 0198-6325. ЧВК 6033155. PMID 29315692.
- ^ «Антидепрессанты СИНИИ». яд.org. Получено 2019-10-21.
- ^ Версиани М., Кассано Дж., Перуджи Дж., Бенедетти А., Масталли Л., Нарди А., Савино М. (январь 2002 г.). «Ребоксетин, селективный ингибитор обратного захвата норэпинефрина, является эффективным и хорошо переносимым препаратом для лечения панического расстройства». Журнал клинической психиатрии. 63 (1): 31–7. Дои:10.4088 / jcp.v63n0107. PMID 11838623.
- ^ "Пакетный вкладыш Cymbalta" (PDF).
- ^ «Информация о назначении Effexor XR».
- ^ Оливье Дж. Д., Оливье Б. (01.09.2019). «Антидепрессанты и сексуальные дисфункции: трансляционная перспектива». Текущие отчеты о сексуальном здоровье. 11 (3): 156–166. Дои:10.1007 / s11930-019-00205-у. ISSN 1548-3592.
- ^ Клейтон А.Х., Монтехо А.Л. (2006). «Большое депрессивное расстройство, антидепрессанты и сексуальная дисфункция». Журнал клинической психиатрии. 67 Дополнение 6: 33–7. PMID 16848675.
- ^ а б Цзин Э., Стро-Уилсон К. (июль 2016 г.). «Сексуальная дисфункция в селективных ингибиторах обратного захвата серотонина (СИОЗС) и возможные решения: обзор повествовательной литературы». Психиатр. 6 (4): 191–196. Дои:10.9740 / mhc.2016.07.191. ЧВК 6007725. PMID 29955469.
- ^ «Серотониновый синдром: профилактика, распознавание и лечение». www.mdedge.com. Получено 2019-11-21.
- ^ а б Фрэнк С. (июль 2008 г.). «Распознавание и лечение серотонинового синдрома». Канадский семейный врач. 54 (7): 988–92. ЧВК 2464814. PMID 18625822.
- ^ «Антидепрессанты СИНИИ». яд.org. Получено 2019-10-23.
- ^ Тинт, Аунг; Хаддад, Питер М; Андерсон, Ян М. (2008-05-01). «Влияние скорости снижения дозы антидепрессантов на частоту симптомов отмены: рандомизированное исследование». Журнал психофармакологии. 22 (3): 330–332. Дои:10.1177/0269881107081550. ISSN 0269-8811. PMID 18515448.
- ^ а б Кокран К.А., Каваллари Л.Х., Шапиро Н.Л., Епископ-младший (август 2011 г.). «Частота кровотечений при одновременном приеме антидепрессантов и варфарина». Терапевтический мониторинг лекарственных средств. 33 (4): 433–8. Дои:10.1097 / FTD.0b013e318224996e. ЧВК 3212440. PMID 21743381.
- ^ Cheng YL, Hu HY, Lin XH, Luo JC, Peng YL, Hou MC и др. (Ноябрь 2015 г.). «Использование SSRI, но не SNRI, усиление кровотечений из верхних и нижних отделов желудочно-кишечного тракта: общенациональное популяционное когортное исследование на Тайване». Лекарство. 94 (46): e2022. Дои:10.1097 / MD.0000000000002022. ЧВК 4652818. PMID 26579809.
- ^ «Дулоксетин: информация о лекарстве». Своевременно. Получено 28 июн 2012.
- ^ Perahia DG, Pritchett YL, Kajdasz DK, Bauer M, Jain R, Russell JM и др. (Январь 2008 г.). «Рандомизированное двойное слепое сравнение дулоксетина и венлафаксина в лечении пациентов с большим депрессивным расстройством». Журнал психиатрических исследований. 42 (1): 22–34. Дои:10.1016 / j.jpsychires.2007.01.008. PMID 17445831.
- ^ Уилсон Э, Ладер М (декабрь 2015 г.). «Обзор лечения симптомов отмены антидепрессантов». Терапевтические достижения в психофармакологии. 5 (6): 357–68. Дои:10.1177/2045125315612334. ЧВК 4722507. PMID 26834969.
- ^ Фава Г.А., Бенаси Дж., Лусенте М., Оффидани Е., Коши Ф., Гуиди Дж. (2018). «Симптомы отмены после прекращения приема ингибиторов обратного захвата серотонина-норадреналина: систематический обзор» (PDF). Психотерапия и психосоматика. 87 (4): 195–203. Дои:10.1159/000491524. PMID 30016772.
- ^ Fava, Giovanni A .; Бенаси, Гиада; Люсенте, Марселла; Оффидани, Эмануэла; Cosci, Fiammetta; Гуиди, Дженни (2018). «Симптомы отмены после отмены ингибитора обратного захвата серотонина-норадреналина: систематический обзор». Психотерапия и психосоматика. 87 (4): 195–203. Дои:10.1159/000491524. HDL:2158/1132671. ISSN 0033-3190. PMID 30016772.
- ^ Тейлор Д., Ленокс-Смит А., Брэдли А. (июнь 2013 г.). «Обзор пригодности дулоксетина и венлафаксина для использования у пациентов с депрессией в системе первичной медико-санитарной помощи с особым вниманием к сердечно-сосудистой безопасности, суицидам и смертности из-за передозировки антидепрессантами». Терапевтические достижения в психофармакологии. 3 (3): 151–61. Дои:10.1177/2045125312472890. ЧВК 3805457. PMID 24167687.
- ^ Саймон, Лесли В .; Хашми, Мухаммад Ф .; Кинэган, Майкл (2019), «Серотониновый синдром», StatPearls, StatPearls Publishing, PMID 29493999, получено 2019-11-21
- ^ «200 лучших брендовых препаратов по общему количеству выписанных в 2009 г.» (PDF). SDI / Verispan, VONA, полный 2009 г.. www.drugtopics.com. Архивировано из оригинал (PDF) 14 июля 2011 г.. Получено 6 апреля 2011.
- ^ Льорка П.М., Фернандес Дж. Л. (апрель 2007 г.). «Эсциталопрам в лечении большого депрессивного расстройства: клиническая эффективность, переносимость и экономическая эффективность по сравнению с препаратом с пролонгированным высвобождением венлафаксина». Международный журнал клинической практики. 61 (4): 702–10. Дои:10.1111 / j.1742-1241.2007.01335.x. PMID 17394446.
- ^ а б Дубовицкий, Михал; Беловикова, Кристина; Чатлосова, Кристина; Боги, Эстер (сентябрь 2017 г.). «Риски использования антидепрессантов СИОЗС / СИОЗСН во время беременности и кормления грудью». Междисциплинарная токсикология. 10 (1): 30–34. Дои:10.1515 / Intx-2017-0004. ISSN 1337-6853. ЧВК 6096863. PMID 30123033.
- ^ а б Strawn, Джеффри Р .; Миллс, Джеффри А .; Sauley, Beau A .; Велдж, Джеффри А. (апрель 2018 г.). «Влияние дозы и класса антидепрессантов на ответ на лечение при детских тревожных расстройствах: метаанализ». Журнал Американской академии детской и подростковой психиатрии. 57 (4): 235–244.e2. Дои:10.1016 / j.jaac.2018.01.015. ISSN 0890-8567. ЧВК 5877120. PMID 29588049.
- ^ Эмсли, Грэм Дж .; Heiligenstein, John H .; Вагнер, Карен Динин; Hoog, Sharon L .; Ernest, Daniel E .; Браун, Эйлин; Нильссон, Мэри; Джейкобсон, Дженни Г. (октябрь 2002 г.). «Флуоксетин для лечения острой депрессии у детей и подростков: плацебо-контролируемое рандомизированное клиническое исследование». Журнал Американской академии детской и подростковой психиатрии. 41 (10): 1205–1215. Дои:10.1097/00004583-200210000-00010. ISSN 0890-8567. PMID 12364842.
- ^ Mulsant, Benoit H .; Blumberger, Daniel M .; Исмаил, Захинор; Раберу, Киран; Рапопорт, Марк Дж. (Август 2014 г.). «Системный подход к фармакотерапии большой гериатрической депрессии». Клиники гериатрической медицины. 30 (3): 517–534. Дои:10.1016 / j.cger.2014.05.002. ISSN 0749-0690. ЧВК 4122285. PMID 25037293.
