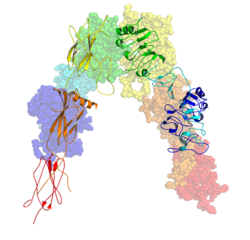
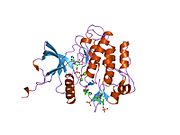
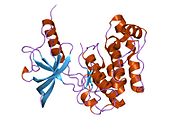
Рецептор инсулина - Insulin receptor
В рецептор инсулина (ИК) это трансмембранный рецептор что активируется инсулин, IGF-I, IGF-II и принадлежит к большому классу рецепторы тирозинкиназы.[5] Метаболически рецептор инсулина играет ключевую роль в регуляции гомеостаз глюкозы, функциональный процесс, который в условиях дегенерации может привести к ряду клинических проявлений, включая сахарный диабет и рак.[6][7] Передача сигналов инсулина контролирует доступ к глюкозе крови в клетках организма. Когда инсулин падает, особенно у людей с высокой чувствительностью к инсулину, клетки тела начинают получать доступ только к липидам, которые не требуют транспорта через мембрану. Таким образом, инсулин также является ключевым регулятором метаболизма жиров. Биохимически рецептор инсулина кодируется одним ген INSR, откуда альтернативное сращивание во время транскрипции приводит к IR-A или IR-B изоформы.[8] Последующие посттрансляционные события любой изоформы приводят к образованию протеолитически расщепленной α- и β-субъединицы, которые при комбинации в конечном итоге способны к гомо- или гетеродимеризации с образованием трансмембранного инсулинового рецептора с дисульфидной связью ≈320 кДа.[8]
Структура
Первоначально, транскрипция альтернативных вариантов сплайсинга, полученных из гена INSR, являются переведено с образованием одного из двух мономерных изомеров; IR-A, в котором экзон 11 исключен, и IR-B, в который включен экзон 11. Включение экзона 11 приводит к добавлению 12 аминокислот выше собственного фурин сайт протеолитического расщепления.

При димеризации рецепторов, после протеолитическое расщепление в α- и β-цепи, дополнительные 12 аминокислот остаются в C-конец α-цепи (обозначенной αCT), где, как предполагается, они влияют на рецептор–лиганд взаимодействие.[9]
Каждый изометрический мономер структурно организован в 8 различных доменов, состоит из; богатый лейцином повторяющийся домен (L1, остатки 1-157), богатый цистеином участок (CR, остатки 158-310), дополнительный богатый лейцином повторяющийся домен (L2, остатки 311-470), три домены фибронектина III типа; FnIII-1 (остатки 471-595), FnIII-2 (остатки 596-808) и FnIII-3 (остатки 809-906). Кроме того, домен вставки (ID, остатки 638-756) находится внутри FnIII-2, содержащий сайт расщепления α / β фурином, из которого протеолиз приводит к доменам IDα и IDβ. Внутри β-цепи ниже домена FnIII-3 находится область трансмембранной спирали (TH) и внутриклеточной прилегающей мембраны (JM), непосредственно перед каталитическим доменом внутриклеточной тирозинкиназы (TK), отвечающим за последующие внутриклеточные пути передачи сигналов.[10]
После расщепления мономера на его соответствующие α- и β-цепи, рецепторная гетеро- или гомодимеризация поддерживается ковалентно между цепями с помощью одной дисульфидной связи и между мономерами в димере с помощью двух дисульфидных связей, отходящих от каждой α-цепи. Общий 3D эктодомен структура, имеющая четыре сайта связывания лиганда, напоминает перевернутую «V», при этом каждый мономер повернут примерно в 2 раза вокруг оси, параллельной перевернутым «V» и L2 и FnIII-1 доменам от каждого мономера, образуя перевернутые «V». вершина.[10][11]
Связывание лиганда


Эндогенные лиганды рецептора инсулина включают: инсулин, IGF-I и IGF-II. Используя крио-ЭМ, было предоставлено структурное понимание конформационных изменений при связывании инсулина. Связывание лиганда с α-цепями димерного эктодомена IR смещает его от перевернутой U-формы к T-образной конформации, и это изменение структурно распространяется на трансмембранные домены, которые сближаются, что в конечном итоге приводит к аутофосфорилированию различных тирозинов. остатки внутриклеточного ТК-домена β-цепи.[12] Эти изменения облегчают набор конкретных адаптерные белки такие как белки субстрата инсулинового рецептора (IRS) в дополнение к SH2-B (Src Гомологии 2 - B), APS и протеинфосфатазы, такие как PTP1B, в конечном итоге способствуя последующим процессам, связанным с гомеостазом глюкозы в крови.[14]
Строго говоря, связь между IR и лигандом проявляет сложные аллостерические свойства. Это было указано с помощью Сюжеты Скэтчарда которые определили, что измерение отношения связанного IR лиганда к несвязанному лиганду не следует линейной зависимости по отношению к изменениям концентрации IR связанного лиганда, предполагая, что IR и его соответствующий лиганд разделяют отношения совместная привязка.[15] Более того, наблюдение того, что скорость диссоциации IR-лиганда увеличивается при добавлении несвязанного лиганда, подразумевает, что природа этого взаимодействия является отрицательной; по-другому говорят, что первоначальное связывание лиганда с IR ингибирует дальнейшее связывание со вторым его активным сайтом - проявление аллостерического ингибирования.[15]
Эти модели утверждают, что каждый IR-мономер имеет 2 сайта связывания инсулина; сайт 1, который связывается с «классической» связывающей поверхностью инсулин: состоящий из L1 плюс αCT доменов и сайта 2, состоящего из петель на стыке FnIII-1 и FnIII-2, которые, как предполагается, связываются с «новым» сайтом связывания лицевой стороны гексамера инсулина.[5] Поскольку каждый мономер, вносящий вклад в IR-эктодомен, демонстрирует трехмерную `` зеркальную '' комплементарность, N-концевой сайт 1 одного мономера в конечном итоге сталкивается с C-концевым сайтом 2 второго мономера, где это также верно для каждого зеркального комплемента мономера (противоположная сторона структура эктодомена). В современной литературе сайты связывания комплемента различаются путем обозначения номенклатуры сайта 1 и сайта 2 второго мономера либо как сайт 3 и сайт 4, либо как сайт 1 'и сайт 2' соответственно.[5][14]Таким образом, эти модели утверждают, что каждый IR может связываться с молекулой инсулина (которая имеет две поверхности связывания) через 4 местоположения, являясь сайтом 1, 2, (3/1 ') или (4/2'). Поскольку каждый сайт 1 проксимально обращен к сайту 2, при связывании инсулина с конкретным сайтом, 'сшивание' через лиганд между мономерами (т.е. как [мономер 1, сайт 1 - инсулин - мономер 2, сайт (4/2 ')] или как [мономер 1, сайт 2 - инсулин - сайт мономера 2 (3/1')]) . В соответствии с текущим математическим моделированием кинетики IR-инсулина, есть два важных последствия для событий перекрестного связывания инсулина; 1. что в результате вышеупомянутого наблюдения отрицательного взаимодействия между IR и его лигандом последующее связывание лиганда с IR уменьшается, и 2. что физическое действие поперечного сшивания приводит эктодомен в такое конформация который необходим для возникновения событий внутриклеточного фосфорилирования тирозина (т.е. эти события служат в качестве требований для активации рецепторов и возможного поддержания гомеостаза глюкозы в крови).[14]
Применение крио-ЭМ и молекулярная динамика моделирование рецептора, восстановленного в нанодиски была визуализирована структура всего димерного эктодомена инсулинового рецептора с четырьмя связанными молекулами инсулина, что подтвердило и прямо показало биохимически предсказанные 4 места связывания.[13]
Агонисты
Путь передачи сигнала
Рецептор инсулина - это тип рецептор тирозинкиназы, при котором связывание агонистического лиганда запускает аутофосфорилирование остатков тирозина, причем каждая субъединица фосфорилирует своего партнера. Добавление фосфатных групп создает сайт связывания для субстрат рецептора инсулина (IRS-1), который впоследствии активируется посредством фосфорилирования. Активированный IRS-1 инициирует путь передачи сигнала и связывается с фосфоинозитид-3-киназа (PI3K), что в свою очередь вызывает его активацию. Затем это катализирует превращение Фосфатидилинозитол 4,5-бисфосфат в Фосфатидилинозитол 3,4,5-трифосфат (PIP3). PIP3 действует как вторичный мессенджер и вызывает активацию фосфатидилинозитол-зависимой протеинкиназы, которая затем активирует несколько других киназ, в первую очередь протеинкиназа B, (PKB, также известный как Akt). PKB запускает транслокацию переносчика глюкозы (GLUT4 ), содержащих везикулы, на клеточную мембрану за счет активации SNARE белки, чтобы облегчить диффузию глюкозы в клетку. PKB также фосфорилирует и ингибирует киназа гликогенсинтазы, который является ферментом, ингибирующим гликогенсинтаза. Таким образом, PKB запускает процесс гликогенеза, который в конечном итоге снижает концентрацию глюкозы в крови.[16]
- Сигнальная трансдукция инсулина

Влияние инсулина на усвоение глюкозы и метаболизм. Инсулин связывается со своим рецептором (1), который, в свою очередь, запускает множество каскадов активации белков (2). К ним относятся: транслокация транспортера Glut-4 к плазматической мембране и приток глюкозы (3), синтез гликогена (4), гликолиз (5) и синтез жирных кислот (6).

Сигнальная трансдукция инсулина: В конце процесса трансдукции активированный белок связывается с PIP2 белки, встроенные в мембрану.
Функция
Регулирование экспрессии генов
Активированный IRS-1 действует как вторичный мессенджер внутри клетки, чтобы стимулировать транскрипцию регулируемых инсулином генов. Во-первых, белок Grb2 связывает остаток P-Tyr IRS-1 в своем SH2 домен. Grb2 затем может связывать SOS, что, в свою очередь, катализирует замену связанного GDP на GTP на Ras, a G протеин. Затем этот белок начинает каскад фосфорилирования, завершающийся активацией митоген-активируемой протеинкиназы (MAPK ), который проникает в ядро и фосфорилирует различные факторы ядерной транскрипции (например, Elk1).
Стимуляция синтеза гликогена
Синтез гликогена также стимулируется рецептором инсулина через IRS-1. В данном случае это SH2 домен из PI-3 киназа (PI-3K), который связывает P-Tyr IRS-1. Теперь активированный PI-3K может преобразовывать липид мембраны. фосфатидилинозитол-4,5-бисфосфат (PIP2) к фосфатидилинозитол 3,4,5-трифосфат (PIP3). Это косвенно активирует протеинкиназу PKB (Акт ) через фосфорилирование. Затем PKB фосфорилирует несколько белков-мишеней, включая киназа гликогенсинтазы 3 (ГСК-3). GSK-3 отвечает за фосфорилирование (и, таким образом, дезактивацию) гликогенсинтазы. Когда GSK-3 фосфорилируется, он деактивируется и предотвращается деактивация гликогенсинтазы. Таким окольным путем инсулин увеличивает синтез гликогена.
Деградация инсулина
Как только молекула инсулина закрепилась на рецепторе и осуществила свое действие, она может высвободиться обратно во внеклеточную среду или может быть разложена клеткой. Деградация обычно включает эндоцитоз комплекса инсулин-рецептор с последующим действием фермент, разрушающий инсулин. Большинство молекул инсулина разлагаются печень клетки. Было подсчитано, что типичная молекула инсулина окончательно разлагается примерно через 71 минуту после ее первоначального выброса в кровоток.[17]
Иммунная система
Помимо метаболической функции, рецепторы инсулина также экспрессируются на иммунных клетках, таких как макрофаги, В-клетки и Т-клетки. На Т-клетках экспрессия рецепторов инсулина не определяется в состоянии покоя, но повышается при Рецептор Т-клеток (TCR) активация. В самом деле, инсулин было показано, что при экзогенном введении способствует in vitro Пролиферация Т-клеток на животных моделях. Передача сигналов рецептора инсулина важна для максимального увеличения потенциального эффекта Т-клеток во время острой инфекции и воспаления.[18][19]
Патология
Основная активность активации рецептора инсулина - стимулирование поглощения глюкозы. По этой причине «нечувствительность к инсулину» или снижение передачи сигналов рецептора инсулина приводит к сахарный диабет 2 типа - клетки не могут усваивать глюкозу, и в результате гипергликемия (увеличение циркулирующей глюкозы) и все последствия диабета.
Пациенты с резистентность к инсулину может отображать черный акантоз.
Несколько пациентов с гомозиготными мутациями в INSR были описаны гены, вызывающие Синдром Донохью или лепреконизм. Этот аутосомно-рецессивный нарушение приводит к полностью нефункциональному рецептору инсулина. У этих пациентов низко посаженные, часто выпуклые уши, расширенные ноздри, утолщенные губы и серьезная задержка роста. В большинстве случаев прогноз для этих пациентов крайне плохой, и смерть наступает в течение первого года жизни. Другие мутации того же гена вызывают менее серьезные Синдром Рабсона-Менденхолла, у пациентов с характерными аномальными зубами, гипертрофическими десна (десны) и увеличение шишковидная железа. Оба заболевания проявляются колебаниями глюкоза уровень: после еды уровень глюкозы вначале очень высок, а затем быстро падает до аномально низкого уровня.[20] Другие генетические мутации гена рецептора инсулина могут вызвать тяжелую резистентность к инсулину.[21]
Взаимодействия
Было показано, что рецептор инсулина взаимодействовать с
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000171105 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск ансамбля 89: ENSMUSG00000005534 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ а б c Уорд CW, Лоуренс MC (апрель 2009 г.). «Лиганд-индуцированная активация рецептора инсулина: многоступенчатый процесс, включающий структурные изменения как лиганда, так и рецептора». BioEssays. 31 (4): 422–34. Дои:10.1002 / bies.200800210. PMID 19274663. S2CID 27645596.
- ^ Эбина Ю., Эллис Л., Ярнагин К., Эдери М., Граф Л., Клаузер Е., Оу Дж. Х., Масиарц Ф., Кан Ю. В., Goldfine ID (апрель 1985 г.). «КДНК человеческого инсулинового рецептора: структурная основа гормонально-активированной трансмембранной передачи сигналов». Клетка. 40 (4): 747–58. Дои:10.1016/0092-8674(85)90334-4. PMID 2859121. S2CID 23230348.
- ^ Malaguarnera R, Sacco A, Voci C, Pandini G, Vigneri R, Belfiore A (май 2012 г.). «Проинсулин с высокой аффинностью связывает изоформу А рецептора инсулина и преимущественно активирует митогенный путь». Эндокринология. 153 (5): 2152–63. Дои:10.1210 / en.2011-1843. PMID 22355074.
- ^ а б Бельфиоре А., Фраска Ф., Пандини Дж., Шакка Л., Виньери Р. (октябрь 2009 г.). «Изоформы рецептора инсулина и гибриды рецептора инсулина / рецептора инсулиноподобного фактора роста в физиологии и болезнях». Эндокринные обзоры. 30 (6): 586–623. Дои:10.1210 / эр.2008-0047. PMID 19752219.
- ^ Кнудсен Л., Де Мейтс П., Киселев В.В. (декабрь 2011 г.). «Понимание молекулярной основы кинетических различий между двумя изоформами рецептора инсулина» (PDF). Биохимический журнал. 440 (3): 397–403. Дои:10.1042 / BJ20110550. PMID 21838706.
- ^ а б Смит Б.Дж., Хуанг К., Конг Джи, Чан С.Дж., Накагава С., Ментинг Дж.Г., Ху С.К., Уиттакер Дж., Штайнер Д.Ф., Кацояннис П.Г., Уорд К.В., Вайс М.А., Лоуренс М.С. (апрель 2010 г.). «Структурное разрешение тандемного гормон-связывающего элемента в рецепторе инсулина и его значение для разработки пептидных агонистов». Труды Национальной академии наук Соединенных Штатов Америки. 107 (15): 6771–6. Bibcode:2010PNAS..107.6771S. Дои:10.1073 / pnas.1001813107. ЧВК 2872410. PMID 20348418.
- ^ МакКерн Н.М., Лоуренс М.К., Стрельцов В.А., Лу М.З., Адамс Т.Э., Ловреч Г.О., Эллеман Т.С., Ричардс К.М., Бентли Д.Д., Пиллинг П.А., Хойн П.А., Картледж К.А., Фам Т.М., Льюис Дж.Л., Санкович С.Е., Стойчевская В., Да Силва E, Робинсон CP, Френкель MJ, Sparrow LG, Fernley RT, Epa VC, Ward CW (сентябрь 2006 г.). «Структура эктодомена рецептора инсулина имеет складчатую конформацию». Природа. 443 (7108): 218–21. Bibcode:2006Натура.443..218М. Дои:10.1038 / природа05106. PMID 16957736. S2CID 4381431.
- ^ а б Гутманн Т., Ким К.Х., Гжибек М., Вальц Т., Джошкун Ю. (май 2018 г.). «Визуализация лиганд-индуцированной трансмембранной передачи сигналов в полноразмерном рецепторе инсулина человека». Журнал клеточной биологии. 217 (5): 1643–1649. Дои:10.1083 / jcb.201711047. ЧВК 5940312. PMID 29453311.
- ^ а б Гутманн, Т; Шефер, И.Б .; Пуджари, C; Бранкачк, Б; Ваттулайнен, I; Штраус, М; Coskun, Ü (6 января 2020 г.). «Крио-ЭМ структура полного эктодомена инсулинового рецептора, насыщенного лигандами». Журнал клеточной биологии. 219 (1). Дои:10.1083 / jcb.201907210. ЧВК 7039211. PMID 31727777.
- ^ а б c Киселев В.В., Верстейхе С., Гоген Л., Де Мейтс П. (февраль 2009 г.). "Модель гармонического осциллятора аллостерического связывания и активации рецепторов инсулина и IGF1". Молекулярная системная биология. 5 (5): 243. Дои:10.1038 / msb.2008.78. ЧВК 2657531. PMID 19225456.
- ^ а б де Мейтс П., Рот Дж., Невилл Д.М., Гэвин Дж. Р., Лесняк М.А. (ноябрь 1973 г.). «Взаимодействие инсулина с его рецепторами: экспериментальные доказательства отрицательной кооперативности». Сообщения о биохимических и биофизических исследованиях. 55 (1): 154–61. Дои:10.1016 / S0006-291X (73) 80072-5. PMID 4361269.
- ^ Берг Дж. М., Тимочко Дж. Л., Страйер Л., Берг Дж. М., Тимочко Дж. Л., Страйер Л. (2002). Биохимия (5-е изд.). W H Freeman. ISBN 0716730510.
- ^ Дакворт В.К., Беннетт Р.Г., Хэмел Ф.Г. (октябрь 1998 г.). «Деградация инсулина: прогресс и потенциал». Эндокринные обзоры. 19 (5): 608–24. Дои:10.1210 / edrv.19.5.0349. PMID 9793760.
- ^ Tsai S, Clemente-Casares X, Zhou AC, Lei H, Ahn JJ, Chan YT, et al. (Август 2018 г.). «Стимуляция, опосредованная рецепторами инсулина, повышает иммунитет Т-клеток во время воспаления и инфекции». Клеточный метаболизм. 28 (6): 922–934.e4. Дои:10.1016 / j.cmet.2018.08.003. PMID 30174303.
- ^ Fischer HJ, Sie C, Schumann E, Witte AK, Dressel R, van den Brandt J, Reichardt HM (март 2017 г.). «Рецептор инсулина играет решающую роль в функции Т-клеток и адаптивном иммунитете». Журнал иммунологии. 198 (5): 1910–1920. Дои:10.4049 / jimmunol.1601011. PMID 28115529.
- ^ Лонго Н., Ван Й., Смит С.А., Лэнгли С.Д., Димелио Л.А., Джаннелла-Нето Д. (июнь 2002 г.). «Генотип-фенотипическая корреляция в наследственной тяжелой инсулинорезистентности». Молекулярная генетика человека. 11 (12): 1465–75. Дои:10.1093 / hmg / 11.12.1465. PMID 12023989. S2CID 15924838.
- ^ Мелвин, Одри; Стирс, Анна. «Тяжелая инсулинорезистентность: патологии». Практический диабет. Получено 31 октября 2020.
- ^ Maddux BA, Goldfine ID (январь 2000 г.). «Мембранный гликопротеин PC-1 ингибирует функцию рецептора инсулина посредством прямого взаимодействия с альфа-субъединицей рецептора». Сахарный диабет. 49 (1): 13–9. Дои:10.2337 / диабет.49.1.13. PMID 10615944.
- ^ Langlais P, Dong LQ, Hu D, Liu F (июнь 2000 г.). «Идентификация Grb10 как прямого субстрата для членов семейства тирозинкиназ Src». Онкоген. 19 (25): 2895–903. Дои:10.1038 / sj.onc.1203616. PMID 10871840.
- ^ Хансен Х., Свенссон Ю., Чжу Дж., Лавиола Л., Джорджино Ф., Вольф Г., Смит Р. Дж., Ридель Х (апрель 1996 г.). «Взаимодействие между SH2-доменом Grb10 и карбоксильным концом инсулинового рецептора». Журнал биологической химии. 271 (15): 8882–6. Дои:10.1074 / jbc.271.15.8882. PMID 8621530.
- ^ Лю Ф., Рот Р.А. (октябрь 1995 г.). «Grb-IR: белок, содержащий SH2-домен, который связывается с рецептором инсулина и ингибирует его функцию». Труды Национальной академии наук Соединенных Штатов Америки. 92 (22): 10287–91. Bibcode:1995PNAS ... 9210287L. Дои:10.1073 / пнас.92.22.10287. ЧВК 40781. PMID 7479769.
- ^ He W., Rose DW, Olefsky JM, Gustafson TA (март 1998 г.). «Grb10 по-разному взаимодействует с рецептором инсулина, рецептором инсулиноподобного фактора роста I и рецептором эпидермального фактора роста через домен гомологии 2 Grb10 Src (SH2) и второй новый домен, расположенный между доменами гомологии плекстрина и SH2». Журнал биологической химии. 273 (12): 6860–7. Дои:10.1074 / jbc.273.12.6860. PMID 9506989.
- ^ Франц Дж. Д., Джорджетти-Перальди С., Оттингер Э. А., Шелсон С. Е. (январь 1997 г.). "Человеческий GRB-IRbeta / GRB10. Варианты сплайсинга белка, связывающего рецептор инсулина и фактора роста, с доменами PH и SH2". Журнал биологической химии. 272 (5): 2659–67. Дои:10.1074 / jbc.272.5.2659. PMID 9006901.
- ^ Kasus-Jacobi A, Béréziat V, Perdereau D, Girard J, Burnol AF (апрель 2000 г.). «Доказательства взаимодействия между рецептором инсулина и Grb7. Роль двух из его связывающих доменов, PIR и SH2». Онкоген. 19 (16): 2052–9. Дои:10.1038 / sj.onc.1203469. PMID 10803466.
- ^ Агирре В., Вернер Э.Д., Жиро Дж., Ли Ю.Х., Шоелсон С.Е., Белый М.Ф. (январь 2002 г.). «Фосфорилирование Ser307 в субстрате-1 рецептора инсулина блокирует взаимодействия с рецептором инсулина и подавляет действие инсулина». Журнал биологической химии. 277 (2): 1531–7. Дои:10.1074 / jbc.M101521200. PMID 11606564.
- ^ Sawka-Verhelle D, Tartare-Deckert S, White MF, Van Obberghen E (март 1996). «Субстрат-2 рецептора инсулина связывается с рецептором инсулина через свой фосфотирозин-связывающий домен и через недавно идентифицированный домен, содержащий аминокислоты 591-786». Журнал биологической химии. 271 (11): 5980–3. Дои:10.1074 / jbc.271.11.5980. PMID 8626379.
- ^ О'Нил Т.Дж., Чжу Ю., Густафсон Т.А. (апрель 1997 г.). «Взаимодействие MAD2 с карбоксильным концом рецептора инсулина, но не с IGFIR. Доказательства высвобождения из рецептора инсулина после активации». Журнал биологической химии. 272 (15): 10035–40. Дои:10.1074 / jbc.272.15.10035. PMID 9092546.
- ^ Брейман Л., Альт А., Куроки Т., Охба М., Бак А., Тенненбаум Т., Сэмпсон С.Р. (апрель 2001 г.). «Инсулин индуцирует специфическое взаимодействие между рецептором инсулина и дельта протеинкиназы C в первичных культивируемых скелетных мышцах». Молекулярная эндокринология. 15 (4): 565–74. Дои:10.1210 / исправление.15.4.0612. PMID 11266508.
- ^ Розенцвейг Т., Брайман Л., Бак А., Альт А., Куроки Т., Сэмпсон С.Р. (июнь 2002 г.). «Дифференциальные эффекты фактора некроза опухоли альфа на изоформы протеинкиназы С альфа и дельта опосредуют ингибирование передачи сигналов рецептора инсулина». Сахарный диабет. 51 (6): 1921–30. Дои:10.2337 / диабет. 51.6.1921. PMID 12031982.
- ^ Маэгава Х, Уги С., Адачи М., Хинода Й, Киккава Р., Ячи А., Сигета Й, Касиваги А. (март 1994 г.). «Киназа инсулинового рецептора фосфорилирует протеинтирозинфосфатазу, содержащую области 2 гомологии Src, и модулирует ее активность PTPase in vitro». Сообщения о биохимических и биофизических исследованиях. 199 (2): 780–5. Дои:10.1006 / bbrc.1994.1297. PMID 8135823.
- ^ Харитоненков А., Шнекенбургер Дж., Чен З., Князев П., Али С., Цвик Э., Уайт М., Ульрих А. (декабрь 1995 г.). «Адаптерная функция протеин-тирозинфосфатазы 1D во взаимодействии рецептора инсулина / субстрата-1 рецептора инсулина». Журнал биологической химии. 270 (49): 29189–93. Дои:10.1074 / jbc.270.49.29189. PMID 7493946.
- ^ Котани К., Уилден П., Пиллэй Т.С. (октябрь 1998 г.). «SH2-Balpha представляет собой адаптерный белок инсулинового рецептора и субстрат, который взаимодействует с петлей активации киназы инсулинового рецептора». Биохимический журнал. 335 (Pt 1) (1): 103–9. Дои:10.1042 / bj3350103. ЧВК 1219757. PMID 9742218.
- ^ Нелмс К., О'Нил Т.Дж., Ли С., Хаббард С.Р., Густафсон Т.А., Пол В.Е. (декабрь 1999 г.). «Альтернативный сплайсинг, локализация гена и связывание SH2-B с киназным доменом рецептора инсулина». Геном млекопитающих. 10 (12): 1160–7. Дои:10.1007 / s003359901183. PMID 10594240. S2CID 21060861.
дальнейшее чтение
- Пирсон РБ, Кемп Б.Э. (1991). «Последовательности сайта фосфорилирования протеинкиназы и мотивы консенсусной специфичности: таблицы». Методы в энзимологии. 200: 62–81. Дои:10.1016 / 0076-6879 (91) 00127-И. ISBN 9780121821012. PMID 1956339.
- Joost HG (февраль 1995 г.). «Структурно-функциональная неоднородность рецепторов инсулина». Сотовая связь. 7 (2): 85–91. Дои:10.1016 / 0898-6568 (94) 00071-I. PMID 7794689.
- О'Делл С.Д., День IN (июль 1998 г.). «Инсулиноподобный фактор роста II (IGF-II)». Международный журнал биохимии и клеточной биологии. 30 (7): 767–71. Дои:10.1016 / S1357-2725 (98) 00048-X. PMID 9722981.
- Лопачинский В. (1999). «Дифференциальная регуляция сигнальных путей для инсулина и инсулиноподобного фактора роста I». Acta Biochimica Polonica. 46 (1): 51–60. Дои:10.18388 / abp.1999_4183. PMID 10453981.
- Сасаока Т., Кобаяши М. (август 2000 г.). «Функциональное значение Shc в передаче сигналов инсулина в качестве субстрата рецептора инсулина». Эндокринный журнал. 47 (4): 373–81. Дои:10.1507 / endocrj.47.373. PMID 11075717.
- Перц М., Торлинская Т. (2001). «Рецептор инсулина - структурные и функциональные характеристики». Монитор медицинских наук. 7 (1): 169–77. PMID 11208515.
- Бенаим Дж., Вильялобо А. (август 2002 г.). «Фосфорилирование кальмодулина. Функциональные последствия». Европейский журнал биохимии / FEBS. 269 (15): 3619–31. Дои:10.1046 / j.1432-1033.2002.03038.x. HDL:10261/79981. PMID 12153558.
внешняя ссылка
- Инсулин + рецептор в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- Обзор всей структурной информации, доступной в PDB за UniProt: P06213 (Рецептор инсулина) на PDBe-KB.