C-июн - C-jun
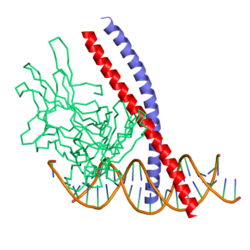
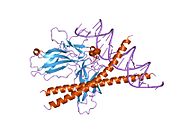
с-июн это белок что у людей кодируется ИЮНЬ ген. c-Jun, в сочетании с c-Fos, формирует АП-1 ранний ответ фактор транскрипции. Впервые он был идентифицирован как Fos-связывающий белок. стр39 и только позже был переоткрыт как продукт гена JUN. c-jun был первым онкогенный открыт фактор транскрипции.[5] Протоонкоген c-Jun является клеточным гомологом вирусного онкопротеин в-июн (P05411).[6] Вирусный гомолог v-jun был обнаружен в вирусе саркомы птиц 17 и назван в честь Джу-нана, то Японский слово для 17.[7] JUN человека кодирует белок, который очень похож на вирусный белок, который непосредственно взаимодействует со специфическими последовательностями ДНК-мишени для регулирования экспрессия гена. Этот ген не имеет интрона и картирован на 1p32-p31, хромосомную область, участвующую как в транслокациях, так и в делециях при злокачественных новообразованиях человека.[8]
Функция
Регулирование
И Jun, и его партнеры по димеризации в образовании AP-1 регулируются различными внеклеточными стимулами, которые включают факторы роста пептидов, провоспалительные цитокины, окислительные и другие формы клеточного стресса, и УФ-облучение. Например, УФ-облучение является мощным индуктором повышенной экспрессии c-jun.[6]
Транскрипция c-jun автоматически регулируется его собственным продуктом, Jun. Связывание Jun (AP-1) с высокоаффинным сайтом связывания AP-1 в промоторной области jun индуцирует транскрипцию jun. Эта положительная ауторегуляция за счет стимуляции собственной транскрипции может быть механизмом продления сигналов от внеклеточных стимулов. Этот механизм может иметь биологическое значение для активности c-jun при раке.[9][10]
Кроме того, активность c-jun может регулироваться путем ERK. Обнаружено, что конститутивно активная ERK увеличивает транскрипцию и стабильность c-jun через CREB и GSK3. Это приводит к активации c-jun и его последующих мишеней, таких как RACK1 и циклин D1. RACK1 может усиливать активность JNK, а активированная передача сигналов JNK впоследствии регулирует активность c-jun.[11]
Активируется путем двойного фосфорилирования JNK пути, но также имеет независимую от фосфорилирования функцию. с-июн нокаутировать смертельно, но трансгенные животные с мутировавшим c-jun, который не может быть фосфорилированный (названный c-junAA) может выжить.
Фосфорилирование Jun по серинам 63 и 73 и треонину 91 и 93 увеличивает транскрипцию генов-мишеней c-jun.[12] Следовательно, регуляция активности c-jun может быть достигнута посредством N-концевого фосфорилирования N-концевыми киназами Jun (JNK). Показано, что активность Jun (AP-1) в индуцированном стрессом апоптозе и клеточной пролиферации регулируется его N-концевым фосфорилированием.[13] Другое исследование показало, что онкогенная трансформация с помощью ras и fos также требует N-концевого фосфорилирования Jun по Serine 63 и 73.[14]
Развитие клеточного цикла
Исследования показали, что c-jun необходим для прогресса Фаза G1 из клеточный цикл, а нулевые клетки c-jun обнаруживают усиленный арест G1. C-jun регулирует уровень транскрипции циклин D1, что является основным Rb киназа. Rb является супрессором роста, и он инактивируется фосфорилированием. Следовательно, c-jun необходим для поддержания достаточной активности киназы циклин D1 и обеспечения развития клеточного цикла.[6]
В клетках, в которых отсутствует c-jun, экспрессия p53 (индуктор остановки клеточного цикла) и стр.21 (Ингибитор CDK и ген-мишень p53) увеличивается, и эти клетки демонстрируют дефект клеточного цикла. Сверхэкспрессия c-jun в клетках приводит к снижению уровня p53 и p21 и ускоряет пролиферацию клеток. C-jun подавляет транскрипцию p53 путем связывания с вариантом сайта AP-1 в промоторе p53. Эти результаты показывают, что c-jun подавляет p53, чтобы контролировать развитие клеточного цикла.[15]
Антиапоптотическая активность
УФ-облучение может активировать экспрессию c-jun и сигнальный путь JNK. C-jun защищает клетки от УФ-излучения. апоптоз, и он сотрудничает с NF-κB для предотвращения апоптоза, вызванного TNFα. Для защиты от апоптоза с помощью c-jun необходимы серины 63/73 (участвующие в фосфорилировании Jun), что не требуется для опосредованного c-jun прогрессирования G1. Это предполагает, что c-jun регулирует развитие клеточного цикла и апоптоз посредством двух отдельных механизмов.[6]
В исследовании использовалась специфическая для печени инактивация c-jun при гепатоцеллюлярной карциноме, которая показала, что нарушение развития опухоли коррелирует с повышенным уровнем белка p53 и уровнем мРНК целевого гена p53. Нокса. Также c-jun может защитить гепатоциты от апоптоза, так как гепатоциты отсутствие c-jun показало повышенную чувствительность к апоптозу, индуцированному TNFα. В гепатоцитах, лишенных c-jun, делеция p53 может восстановить устойчивость к TNFα. Эти результаты показывают, что c-jun противодействует проапоптотической активности p53 в опухоли печени.[16]
Клиническое значение
Известно, что c-jun играет роль в клеточная пролиферация и апоптоз эндометрий на протяжении менструальный цикл. Циклическое изменение уровней белка c-jun имеет важное значение для пролиферации и апоптоза железистых эпителиальных клеток. Устойчивая стромальная экспрессия белка c-jun может предотвратить стромальные клетки от вступления в апоптоз во время поздней секреторной фазы.[17]
Рак
В исследовании с использованием немелкоклеточный рак легких (NSCLC) было обнаружено, что c-jun сверхэкспрессируется в 31% случаев в первичных и метастатических опухолях легких, тогда как нормальные проводящие дыхательные пути и альвеолярный эпителий в целом не экспрессируют c-jun.[18]
Исследование с группой, состоящей из 103 случаев инвазивного рака груди I / II фазы, показало, что активированный c-jun экспрессируется преимущественно на инвазивном фронте рака груди и связан с пролиферацией и ангиогенез.[19]
Инициация опухоли
Было проведено исследование специфической для печени инактивации c-jun на разных стадиях развития опухоли у мышей с химически индуцированными гепатоцеллюлярными карциномами. Результат указывает на то, что c-jun необходим на ранней стадии развития опухоли, а удаление c-jun может в значительной степени подавить образование опухоли. Кроме того, c-jun необходим для выживания опухолевых клеток между стадиями инициации и прогрессирования. В отличие от этого, инактивация c-jun в запущенных опухолях не влияет на прогрессирование опухоли.[16]
Рак молочной железы
Сверхэкспрессия c-jun в клетках MCF-7 может привести к общей повышенной агрессивности, о чем свидетельствует повышенная клеточная подвижность, повышенная экспрессия фермента, разрушающего матрикс. ММП-9, увеличение химиоинвазии in vitro и образование опухолей у голых мышей в отсутствие экзогенных эстрогены. В MCF-7 клетки со сверхэкспрессией c-jun стали нечувствительными к эстрогену и тамоксифену, поэтому предполагается, что избыточная экспрессия c-jun приводит к эстроген-независимому фенотипу в клетках рака молочной железы. Наблюдаемый фенотип для клеток MCF-7 со сверхэкспрессией c-jun подобен фенотипу, наблюдаемому клинически при распространенном раке молочной железы, который стал невосприимчивым к гормонам.[20]
Инвазивный фенотип, обусловленный сверхэкспрессией c-jun, подтвержден в другом исследовании. Кроме того, это исследование показало увеличение in vivo метастазов в печень при раке груди со сверхэкспрессией c-jun. Это открытие предполагает, что c-jun играет решающую роль в метастазировании рака груди.[21]
В опухолях молочной железы эндогенный c-jun играет ключевую роль в ErbB2 -индуцированная миграция и инвазия эпителиальных клеток молочной железы. Jun транскрипционно активирует промоторы SCF (фактор стволовых клеток ) и CCL5. Индуцированная экспрессия SCF и CCL5 способствует самообновлению эпителиальной популяции молочных желез. Это предполагает, что c-jun опосредует распространение стволовых клеток рака молочной железы для повышения инвазивности опухоли.[22]
Рак вульвы
C-jun наблюдается сверхэкспрессия в Плоскоклеточный рак вульвы образцов в сочетании с индуцированной гиперметилированием инактивацией RARB ген-супрессор опухоли.[9] Действительно, уровни мРНК c-Jun были выше в Рак вульвы по сравнению с образцами нормальной кожи и предопухолевых поражений вульвы, что подчеркивает перекрестную связь между геном RARB и онкогеном c-Jun.[9]
Клеточная дифференциация
Десять недифференцированных и очень агрессивных сарком показали амплификацию гена jun и избыточную экспрессию JUN как на уровне РНК, так и на уровне белка. Сверхэкспрессия c-jun в клетках 3T3-L1 (линия преадипоцитарных неопухолевых клеток, напоминающая человеческие липосаркома ) может блокировать или задерживать адипоцитарную дифференцировку этих клеток.[23]
Регенерация нервов и спинного мозга
Повреждение периферических нервов у грызунов быстро активирует передачу сигналов JNK, которая, в свою очередь, активирует c-Jun. Напротив, повреждение нервов в центральной нервной системе - нет. c-Jun достаточно для ускорения регенерации аксонов как в периферической, так и в центральной нервной системе, поскольку избыточная экспрессия как в нейронах ганглиев задних корешков, так и в нейронах коры приводит к усилению регенерации.[24]
В качестве мишени противоракового лекарства
Поскольку при раке наблюдается чрезмерная экспрессия c-jun,[9] несколько исследований выдвинули на первый план гипотезу о том, что этот ген может быть мишенью для лечения рака. Исследование показало, что онкогенная трансформация с помощью ras и fos требует N-концевого фосфорилирования Jun в серинах 63 и 73 с помощью N-концевых киназ Jun (JNK). В этом исследовании индуцированная опухоль кожи и остеосаркома показали нарушение развития у мышей с мутантом Jun, неспособным к N-концевому фосфорилированию.[14] Кроме того, в модели рака кишечника у мышей генетическая отмена N-концевого фосфорилирования Jun или кишечная инактивация c-jun ослабляли развитие рака и увеличивали продолжительность жизни.[12] Следовательно, нацеливание на N-концевое фосфорилирование Jun (или путь передачи сигналов JNK) может быть потенциальной стратегией ингибирования роста опухоли.
В раковых клетках B16-F10, полученных из меланомы, инактивация c-jun фармакологическим ингибитором JNK / jun SP в сочетании с нокдауном JunB может привести к цитотоксическому эффекту, ведущему к остановке клеток и апоптозу. Эта стратегия против JunB / Jun может увеличить выживаемость мышей, инокулированных опухолевыми клетками, что предполагает потенциальную противоопухолевую стратегию за счет ингибирования Jun и JunB.[25]
Противораковые свойства c-jun
Большинство результатов исследований показывают, что c-jun способствует возникновению опухоли и увеличению инвазивности. Тем не менее, несколько исследований обнаружили некоторые альтернативные действия c-jun, предполагающие, что c-jun на самом деле может быть обоюдоострым мечом при раке.
p16
p16INK4a является супрессором опухолей и ингибитором клеточного цикла, и исследование показывает, что c-jun действует как «телохранитель» для p16INK4a предотвращая метилирование p16INK4a промоутер. Следовательно, c-jun может предотвратить молчание гена p16.INK4a.[нужна цитата ]
Тилофорин
Тилофорин - это тип алкалоида растительного происхождения с противораковой активностью, вызывающий остановку клеточного цикла. Исследование показало, что лечение тилофорином увеличивает накопление белка c-jun. Затем экспрессия c-jun в сочетании с тилофорином способствует остановке G1 в клетках карциномы за счет подавления циклина A2. Таким образом, результат указывает на то, что противораковый механизм тилофорина опосредуется через c-jun.[26]
Взаимодействия
C-jun был показан взаимодействовать с:
- ATF2[27][28][29]
- AR[30]
- ASCC3[31]
- ATF3[29][32][33]
- BCL3[34]
- BCL6[35]
- BRCA1[36]
- C-Fos[37][38][39][40][41][42][43]
- CSNK2A1[44]
- COPS5[45]
- CREBBP[46]
- CSNK2A2[44]
- DDX21,[47]
- DDIT3[48]
- ЭРГ[49]
- ETS2,[50]
- FOSL1[38]
- GTF2B[51]
- MAPK8[52][53][54][55][56][57][58][59]
- MyoD[60]
- NACA[61]
- NELFB[62]
- NFE2L1[43]
- NFE2L2[43]
- NCOR2[63]
- NCOA1[64][65][66]
- PIN1[67]
- RBM39[68]
- РЕЛА[40]
- RB1[69]
- RFWD2[70][71]
- RUNX1[72][73]
- RUNX2[72][73]
- SMAD3[74][75][76]
- STAT1[77]
- STAT3[77]
- TBP[51]
- TGIF1[78]
Смотрите также
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000177606 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000052684 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ Фогт П.К. (июнь 2002 г.). «Случайные совпадения: начало ИЮНЯ». Обзоры природы. Рак. 2 (6): 465–9. Дои:10.1038 / nrc818. PMID 12189388.
- ^ а б c d Мудрость Р., Джонсон Р., Мур С. (январь 1999 г.). «c-Jun регулирует развитие клеточного цикла и апоптоз с помощью различных механизмов». Журнал EMBO. 18 (1): 188–97. Дои:10.1093 / emboj / 18.1.188. ЧВК 1171114. PMID 9878062.
- ^ Маки Ю., Бос Т.Дж., Дэвис К., Старбак М., Фогт П.К. (май 1987 г.). «Вирус саркомы птиц 17 несет онкоген jun». Труды Национальной академии наук Соединенных Штатов Америки. 84 (9): 2848–52. Дои:10.1073 / пнас.84.9.2848. ЧВК 304757. PMID 3033666.
- ^ "Entrez Gene: JUN jun онкоген".
- ^ а б c d Rotondo JC, Borghi A, Selvatici R, Mazzoni E, Bononi I, Corazza M, Kussini J, Montinari E, Gafà R, Tognon M, Martini F (июль 2018 г.). «Ассоциация гена рецептора ретиноевой кислоты β с началом и прогрессированием плоскоклеточной карциномы вульвы, связанной со склеротическим лишаем». JAMA Дерматология. 154 (7): 819–823. Дои:10.1001 / jamadermatol.2018.1373. ЧВК 6128494. PMID 29898214.
- ^ Ангел П., Хаттори К., Смил Т., Карин М. (декабрь 1988 г.). «Протоонкоген jun положительно саморегулируется его продуктом, Jun / AP-1». Клетка. 55 (5): 875–85. Дои:10.1016/0092-8674(88)90143-2. PMID 3142689.
- ^ Лопес-Бергами П., Хуанг С., Гойдос Дж. С., Ип Д., Бар-Эли М., Херлин М., Смолли К. С., Махале А., Ерошкин А., Ааронсон С., Ронаи З. (май 2007 г.). «Перепроектированные сигнальные пути ERK-JNK при меланоме». Раковая клетка. 11 (5): 447–60. Дои:10.1016 / j.ccr.2007.03.009. ЧВК 1978100. PMID 17482134.
- ^ а б Натери А.С., Спенсер-Дене Б., Беренс А. (сентябрь 2005 г.). «Взаимодействие фосфорилированного c-Jun с TCF4 регулирует развитие рака кишечника». Природа. 437 (7056): 281–5. Bibcode:2005Натура.437..281Н. Дои:10.1038 / природа03914. PMID 16007074.
- ^ Беренс А., Сибилия М., Вагнер Э. Ф. (март 1999 г.). «Амино-терминальное фосфорилирование c-Jun регулирует индуцированный стрессом апоптоз и клеточную пролиферацию». Природа Генетика. 21 (3): 326–9. Дои:10.1038/6854. PMID 10080190.
- ^ а б Беренс А., Йохум В., Сибилия М., Вагнер Е. Ф. (май 2000 г.). «Онкогенная трансформация с помощью ras и fos опосредована фосфорилированием N-конца c-Jun». Онкоген. 19 (22): 2657–63. Дои:10.1038 / sj.onc.1203603. PMID 10851065.
- ^ Schreiber M, Kolbus A, Piu F, Szabowski A, Möhle-Steinlein U, Tian J, Karin M, Angel P, Wagner EF (март 1999 г.). «Контроль прохождения клеточного цикла с помощью c-Jun зависит от p53». Гены и развитие. 13 (5): 607–19. Дои:10.1101 / gad.13.5.607. ЧВК 316508. PMID 10072388.
- ^ а б Эферл Р., Риччи Р., Кеннер Л., Зенц Р., Дэвид Дж. П., Рат М., Вагнер Е. Ф. (январь 2003 г.). «Развитие опухоли печени. C-Jun противодействует проапоптотической активности p53». Клетка. 112 (2): 181–92. Дои:10.1016 / S0092-8674 (03) 00042-4. PMID 12553907.
- ^ Удоу Т., Хатисуга Т., Цудзиока Х., Каварабаяси Т. (2004). «Роль белка c-jun в пролиферации и апоптозе эндометрия на протяжении менструального цикла». Гинекологическое и акушерское обследование. 57 (3): 121–6. Дои:10.1159/000075701. PMID 14691341.
- ^ Сабо Э., Рифф М.Э., Штейнберг С.М., Биррер М.Дж., Линнойла Р.И. (январь 1996 г.). «Измененная экспрессия cJUN: раннее событие в канцерогенезе легких у человека». Исследования рака. 56 (2): 305–15. PMID 8542585.
- ^ Vleugel MM, Greijer AE, Bos R, van der Wall E, van Diest PJ (июнь 2006 г.). «Активация c-Jun связана с пролиферацией и ангиогенезом при инвазивном раке груди». Патология человека. 37 (6): 668–74. Дои:10.1016 / j.humpath.2006.01.022. PMID 16733206.
- ^ Смит Л.М., Вайз С.К., Хендрикс Д.Т., Сабичи А.Л., Бос Т., Редди П., Браун П.Х., Биррер М.Дж. (октябрь 1999 г.). «Сверхэкспрессия cJun в клетках рака молочной железы MCF-7 вызывает онкогенный, инвазивный и устойчивый к гормонам фенотип». Онкоген. 18 (44): 6063–70. Дои:10.1038 / sj.onc.1202989. PMID 10557095.
- ^ Чжан И, Пу Икс, Ши М, Чен Л., Сун Й, Цянь Л., Юань Г, Чжан Х, Ю М, Ху М, Шен Б., Го Н. (август 2007 г.). «Критическая роль сверхэкспрессии c-Jun в метастазах печени на модели ксенотрансплантата рака груди человека». BMC Рак. 7: 145. Дои:10.1186/1471-2407-7-145. ЧВК 1959235. PMID 17672916.
- ^ Цзяо X, Катияр С., Уиллмарт NE, Лю М., Ма Х, Фломенберг Н., Лисанти М.П., Пестелл Р.Г. (март 2010 г.). «c-Jun вызывает инвазию эпителиальных клеток молочной железы и рост стволовых клеток рака груди». Журнал биологической химии. 285 (11): 8218–26. Дои:10.1074 / jbc.M110.100792. ЧВК 2832973. PMID 20053993.
- ^ Мариани О., Бреннето К., Коиндре Дж. М., Груэль Н., Ганем С., Делатре О., Стерн М. Х., Ауриас А. (апрель 2007 г.). «Амплификация онкогена JUN и сверхэкспрессия блокируют дифференцировку адипоцитов в высокоагрессивных саркомах». Раковая клетка. 11 (4): 361–74. Дои:10.1016 / j.ccr.2007.02.007. PMID 17418412.
- ^ Махар М., Кавалли В. (июнь 2018 г.). «Внутренние механизмы регенерации аксонов нейронов». Обзоры природы. Неврология. 19 (6): 323–337. Дои:10.1038 / с41583-018-0001-8. ЧВК 5987780. PMID 29666508.
- ^ Гурзов Е.Н., Бакири Л., Альфаро Дж. М., Вагнер Е. Ф., Искьердо М. (январь 2008 г.). «Нацеливание на белки c-Jun и JunB в качестве потенциальной противораковой клеточной терапии». Онкоген. 27 (5): 641–52. Дои:10.1038 / sj.onc.1210690. PMID 17667939.
- ^ Ян CW, Ли YZ, Hsu HY, Wu CM, Чанг ХЙ, Чао Ю.С., Ли SJ (июнь 2013 г.). «c-Jun-опосредованные противораковые механизмы тилофорина». Канцерогенез. 34 (6): 1304–14. Дои:10.1093 / carcin / bgt039. PMID 23385061.
- ^ Newell CL, Deisseroth AB, Lopez-Berestein G (июль 1994 г.). «Взаимодействие ядерных белков с AP-1 / CRE-подобной промоторной последовательностью в гене TNF-альфа человека». Журнал биологии лейкоцитов. 56 (1): 27–35. Дои:10.1002 / jlb.56.1.27. PMID 8027667.
- ^ Кара CJ, Liou HC, Ивашкив LB, Glimcher LH (апрель 1990). «КДНК человеческого белка, связывающего элемент ответа на циклический АМФ, который отличается от CREB и экспрессируется преимущественно в головном мозге». Молекулярная и клеточная биология. 10 (4): 1347–57. Дои:10.1128 / MCB.10.4.1347. ЧВК 362236. PMID 2320002.
- ^ а б Хай Т., Курран Т. (май 1991 г.). «Межсемейная димеризация факторов транскрипции Fos / Jun и ATF / CREB изменяет специфичность связывания ДНК». Труды Национальной академии наук Соединенных Штатов Америки. 88 (9): 3720–4. Bibcode:1991PNAS ... 88.3720H. Дои:10.1073 / pnas.88.9.3720. ЧВК 51524. PMID 1827203.
- ^ Sato N, Sadar MD, Bruchovsky N, Saatcioglu F, Rennie PS, Sato S, Lange PH, Gleave ME (июль 1997 г.). «Андрогенная индукция гена простатоспецифического антигена подавляется белок-белковым взаимодействием между рецептором андрогена и AP-1 / c-Jun в клеточной линии рака простаты человека LNCaP». Журнал биологической химии. 272 (28): 17485–94. Дои:10.1074 / jbc.272.28.17485. PMID 9211894.
- ^ Jung DJ, Sung HS, Goo YW, Lee HM, Park OK, Jung SY, Lim J, Kim HJ, Lee SK, Kim TS, Lee JW, Lee YC (июль 2002 г.). «Новый комплекс коактиватора транскрипции, содержащий коинтегратор активирующего сигнала 1». Молекулярная и клеточная биология. 22 (14): 5203–11. Дои:10.1128 / MCB.22.14.5203-5211.2002. ЧВК 139772. PMID 12077347.
- ^ Пирсон А.Г., Грей CW, Пирсон Дж. Ф., Гринвуд Дж. М., Во время MJ, Драгунов М. (декабрь 2003 г.). «ATF3 усиливает c-Jun-опосредованное прорастание нейритов». Исследование мозга. Молекулярные исследования мозга. 120 (1): 38–45. Дои:10.1016 / j.molbrainres.2003.09.014. PMID 14667575.
- ^ Чен Б.П., Вольфганг С.Д., Хай Т. (март 1996 г.). «Анализ ATF3, фактора транскрипции, индуцируемого физиологическими стрессами и модулируемого gadd153 / Chop10». Молекулярная и клеточная биология. 16 (3): 1157–68. Дои:10.1128 / MCB.16.3.1157. ЧВК 231098. PMID 8622660.
- ^ На СИ, Чой Дж. Э., Ким Х. Дж., Чжун Б. Х., Ли Ю. Си, Ли Дж. У. (октябрь 1999 г.). «Bcl3, белок IkappaB, стимулирует активирующую трансактивацию белка-1 и клеточную пролиферацию». Журнал биологической химии. 274 (40): 28491–6. Дои:10.1074 / jbc.274.40.28491. PMID 10497212.
- ^ Васанвала Ф. Х., Кусам С., Тони Л. М., Дент А. Л. (август 2002 г.). «Подавление функции AP-1: механизм регуляции экспрессии Blimp-1 и дифференцировки В-лимфоцитов протоонкогеном В-клеточной лимфомы-6». Журнал иммунологии. 169 (4): 1922–9. Дои:10.4049 / jimmunol.169.4.1922. PMID 12165517.
- ^ Ху Ю.Ф., Ли Р. (июнь 2002 г.). «JunB усиливает функцию домена 1 активации BRCA1 (AD1) посредством взаимодействия, опосредованного спиральной спиралью». Гены и развитие. 16 (12): 1509–17. Дои:10.1101 / gad.995502. ЧВК 186344. PMID 12080089.
- ^ Ито Т., Ямаути М., Нишина М., Ямамичи Н., Мизутани Т., Уи М., Мураками М., Иба Х. (январь 2001 г.). «Идентификация субъединицы BAF60a комплекса SWI.SNF как детерминанта трансактивационного потенциала димеров Fos / Jun». Журнал биологической химии. 276 (4): 2852–7. Дои:10.1074 / jbc.M009633200. PMID 11053448.
- ^ а б Pognonec P, Boulukos KE, Aperlo C, Fujimoto M, Ariga H, Nomoto A, Kato H (май 1997 г.). «Межсемейное взаимодействие между белками bHLHZip USF и bZip Fra1 приводит к подавлению активности AP1». Онкоген. 14 (17): 2091–8. Дои:10.1038 / sj.onc.1201046. PMID 9160889.
- ^ Гловер Дж. Н., Харрисон СК (январь 1995 г.). «Кристаллическая структура гетеродимерного фактора транскрипции bZIP c-Fos-c-Jun, связанного с ДНК». Природа. 373 (6511): 257–61. Bibcode:1995Натура 373..257Г. Дои:10.1038 / 373257a0. PMID 7816143.
- ^ а б Ян Х, Чен Й, Габузда Д. (сентябрь 1999 г.). «Киназа ERK MAP связывает сигналы цитокинов с активацией латентной инфекции ВИЧ-1, стимулируя кооперативное взаимодействие AP-1 и NF-kappaB». Журнал биологической химии. 274 (39): 27981–8. Дои:10.1074 / jbc.274.39.27981. PMID 10488148.
- ^ Номура Н., Зу Ю.Л., Маэкава Т., Табата С., Акияма Т., Исии С. (февраль 1993 г.). «Выделение и характеристика нового члена семейства генов, кодирующего белок, связывающий элемент ответа цАМФ CRE-BP1». Журнал биологической химии. 268 (6): 4259–66. PMID 8440710.
- ^ Финкель Т., Дык Дж., Ферон ER, Данг CV, Томаселли Г.Ф. (январь 1993 г.). «Обнаружение и модуляция in vivo белок-белковых взаимодействий спираль-петля-спираль». Журнал биологической химии. 268 (1): 5–8. PMID 8380166.
- ^ а б c Венугопал Р., Джайсвал А.К. (декабрь 1998 г.). «Nrf2 и Nrf1 в сочетании с белками Jun регулируют экспрессию, опосредованную элементами антиоксидантного ответа, и скоординированную индукцию генов, кодирующих детоксифицирующие ферменты». Онкоген. 17 (24): 3145–56. Дои:10.1038 / sj.onc.1202237. PMID 9872330.
- ^ а б Ямагути Ю., Вада Т., Судзуки Ф, Такаги Т., Хасэгава Дж., Ханда Х (август 1998 г.). «Казеинкиназа II взаимодействует с доменами bZIP нескольких факторов транскрипции». Исследования нуклеиновых кислот. 26 (16): 3854–61. Дои:10.1093 / nar / 26.16.3854. ЧВК 147779. PMID 9685505.
- ^ Claret FX, Hibi M, Dhut S, Toda T, Karin M (октябрь 1996 г.). «Новая группа консервативных коактиваторов, повышающих специфичность факторов транскрипции AP-1». Природа. 383 (6599): 453–7. Bibcode:1996Натура.383..453C. Дои:10.1038 / 383453a0. PMID 8837781.
- ^ Сано Й, Токиту Ф., Дай П., Маэкава Т., Ямамото Т., Исии С. (октябрь 1998 г.). «CBP снижает внутримолекулярное ингибирование функции ATF-2». Журнал биологической химии. 273 (44): 29098–105. Дои:10.1074 / jbc.273.44.29098. PMID 9786917.
- ^ Вестермарк Дж., Вайс С., Саффрих Р., Каст Дж., Мусти А.М., Уэссели М., Ансорге В., Серафин Б., Вильм М., Вальдес Б.К., Боман Д. (февраль 2002 г.). «DEXD / H-бокс РНК-геликаза RHII / Gu является кофактором для транскрипции, активируемой c-Jun». Журнал EMBO. 21 (3): 451–60. Дои:10.1093 / emboj / 21.3.451. ЧВК 125820. PMID 11823437.
- ^ Убеда М., Вальехо М., Хабенер Дж. Ф. (ноябрь 1999 г.). «Усиление транскрипции генов CHOP за счет взаимодействия с комплексными белками Jun / Fos AP-1». Молекулярная и клеточная биология. 19 (11): 7589–99. Дои:10.1128 / MCB.19.11.7589. ЧВК 84780. PMID 10523647.
- ^ Verger A, Buisine E, Carrère S, Wintjens R, Flourens A, Coll J, Stéhelin D, Duterque-Coquillaud M (май 2001 г.). «Идентификация аминокислотных остатков фактора транскрипции ETS Erg, которые опосредуют образование тройного комплекса Erg-Jun / Fos-ДНК» (PDF). Журнал биологической химии. 276 (20): 17181–9. Дои:10.1074 / jbc.M010208200. PMID 11278640.
- ^ Basuyaux JP, Ferreira E, Stéhelin D, Butticè G (октябрь 1997 г.). «Факторы транскрипции Ets взаимодействуют друг с другом и с комплексом c-Fos / c-Jun через отдельные белковые домены ДНК-зависимым и независимым образом». Журнал биологической химии. 272 (42): 26188–95. Дои:10.1074 / jbc.272.42.26188. PMID 9334186.
- ^ а б Франклин СС, Маккалок А.В., Крафт А.С. (февраль 1995 г.). «Связь in vitro между семейством белков Jun и общими факторами транскрипции, TBP и TFIIB». Биохимический журнал. 305 (Pt 3): 967–74. Дои:10.1042 / bj3050967. ЧВК 1136352. PMID 7848298.
- ^ Иситани Т., Такаэсу Г., Ниномия-Цудзи Дж., Сибуя Х., Гейнор Р. Б., Мацумото К. (декабрь 2003 г.). «Роль TAB2-родственного белка TAB3 в передаче сигналов IL-1 и TNF». Журнал EMBO. 22 (23): 6277–88. Дои:10.1093 / emboj / cdg605. ЧВК 291846. PMID 14633987.
- ^ Нишито Х., Сайто М., Мочида Й., Такеда К., Накано Х., Роте М., Миядзоно К., Итиджо Х. (сентябрь 1998 г.). «ASK1 необходим для активации JNK / SAPK с помощью TRAF2». Молекулярная клетка. 2 (3): 389–95. Дои:10.1016 / S1097-2765 (00) 80283-X. PMID 9774977.
- ^ Дерихард Б., Хиби М., Ву И. Х., Баррет Т., Су Б., Дэн Т., Карин М., Дэвис Р. Дж. (Март 1994 г.). «JNK1: протеинкиназа, стимулируемая УФ-светом и Ha-Ras, которая связывает и фосфорилирует домен активации c-Jun». Клетка. 76 (6): 1025–37. Дои:10.1016/0092-8674(94)90380-8. PMID 8137421.
- ^ Язган О., Пфарр С.М. (август 2002 г.). «Регулирование двух изоформ JunD с помощью N-концевых киназ Jun». Журнал биологической химии. 277 (33): 29710–8. Дои:10.1074 / jbc.M204552200. PMID 12052834.
- ^ Тада К., Окадзаки Т., Сакон С., Кобараи Т., Куросава К., Ямаока С., Хашимото Х., Мак Т.В., Ягита Х., Окумура К., Йе В.К., Накано Х. (сентябрь 2001 г.). «Важнейшие роли TRAF2 и TRAF5 в индуцированной фактором некроза опухоли активации NF-каппа B и защите от гибели клеток». Журнал биологической химии. 276 (39): 36530–4. Дои:10.1074 / jbc.M104837200. PMID 11479302.
- ^ Мейер К.Ф., Ван X, Чанг С., Темплтон Д., Тан Т.Х. (апрель 1996 г.). «Взаимодействие между c-Rel и митоген-активируемым сигнальным каскадом киназы 1 протеинкиназы в опосредовании активации энхансера kappaB». Журнал биологической химии. 271 (15): 8971–6. Дои:10.1074 / jbc.271.15.8971. PMID 8621542.
- ^ Кано Э., Хаззалин К.А., Кардалину Э., Пряжка Р.С., Махадеван Л.С. (ноябрь 1995 г.). «Ни ERK, ни подтипы JNK / SAPK MAP киназы не являются существенными для фосфорилирования гистона H3 / HMG-14 или индукции c-fos и c-jun». Журнал клеточной науки. 108 (Pt 11): 3599–609. PMID 8586671.
- ^ Tournier C, Whitmarsh AJ, Cavanagh J, Barrett T, Davis RJ (июль 1997 г.). «Митоген-активированная протеинкиназа киназа 7 является активатором c-Jun NH2-концевой киназы». Труды Национальной академии наук Соединенных Штатов Америки. 94 (14): 7337–42. Bibcode:1997PNAS ... 94.7337T. Дои:10.1073 / пнас.94.14.7337. ЧВК 23822. PMID 9207092.
- ^ Бенгал Э., Рансоне Л., Шарфманн Р., Дварки В.Дж., Тапскотт С.Дж., Вайнтрауб Х., Верма И.М. (февраль 1992 г.). «Функциональный антагонизм между белками c-Jun и MyoD: прямая физическая ассоциация». Клетка. 68 (3): 507–19. Дои:10.1016 / 0092-8674 (92) 90187-Н. PMID 1310896.
- ^ Моро А., Йотов В. В., Глорье Ф. Х., Сен-Арно Р. (март 1998 г.). «Костно-специфическая экспрессия альфа-цепи растущего полипептид-ассоциированного комплекса, коактиватора, усиливающего транскрипцию, опосредованную c-Jun». Молекулярная и клеточная биология. 18 (3): 1312–21. Дои:10.1128 / MCB.18.3.1312. ЧВК 108844. PMID 9488446.
- ^ Чжун Х., Чжу Дж., Чжан Х., Дин Л., Сунь И, Хуан С., Е Цюй (декабрь 2004 г.). «COBRA1 ингибирует транскрипционную активность AP-1 в трансфицированных клетках». Сообщения о биохимических и биофизических исследованиях. 325 (2): 568–73. Дои:10.1016 / j.bbrc.2004.10.079. PMID 15530430.
- ^ Ли СК, Ким Дж. Х., Ли Ю. Си, Чеонг Дж., Ли Дж. У. (апрель 2000 г.). «Медиатор подавления рецепторов ретиноевой кислоты и гормонов щитовидной железы, как новая транскрипционная молекула-корепрессор, активирующая белок-1, ядерный фактор-каппаВ и фактор сывороточного ответа». Журнал биологической химии. 275 (17): 12470–4. Дои:10.1074 / jbc.275.17.12470. PMID 10777532.
- ^ Ли С.К., Анзик С.Л., Чой Дж.Э., Бубендорф Л., Гуан XY, Юнг Ю.К., Каллиониеми О.П., Кононен Дж., Трент Дж. М., Азорса Д., Джун Б. Х., Чеонг Дж. Х., Ли Ю. К., Мельцер П. С., Ли Дж. В. (ноябрь 1999 г.). «Ядерный фактор, ASC-2, как транскрипционный коактиватор, усиленный раком, необходимый для лиганд-зависимой трансактивации ядерными рецепторами in vivo». Журнал биологической химии. 274 (48): 34283–93. Дои:10.1074 / jbc.274.48.34283. PMID 10567404.
- ^ Ли СК, На Си, Юнг Си, Чой Дж. Э., Чжун Б. Х., Чеонг Дж., Мельцер П. С., Ли Ю. К., Ли Дж. В. (июнь 2000 г.). «Активация белка-1, ядерного фактора-каппаВ и фактора ответа сыворотки в качестве новых молекул-мишеней коактиватора транскрипции, усиленного раком, ASC-2». Молекулярная эндокринология. 14 (6): 915–25. Дои:10.1210 / исправление.14.6.0471. PMID 10847592.
- ^ Ли С.К., Ким Х.Дж., На СЫ, Ким Т.С., Чой Х.С., Им С.Ю., Ли Дж.В. (июль 1998 г.). «Коактиватор-1 стероидного рецептора коактивирует активирующую трансактивацию, опосредованную белком-1, посредством взаимодействия с субъединицами c-Jun и c-Fos». Журнал биологической химии. 273 (27): 16651–4. Дои:10.1074 / jbc.273.27.16651. PMID 9642216.
- ^ Wulf GM, Ryo A, Wulf GG, Lee SW, Niu T, Petkova V, Lu KP (июль 2001 г.). «Pin1 сверхэкспрессируется при раке молочной железы и взаимодействует с передачей сигналов Ras, увеличивая транскрипционную активность c-Jun по отношению к циклину D1». Журнал EMBO. 20 (13): 3459–72. Дои:10.1093 / emboj / 20.13.3459. ЧВК 125530. PMID 11432833.
- ^ Юнг DJ, Na SY, Na DS, Ли JW (январь 2002 г.). «Молекулярное клонирование и характеристика CAPER, нового коактиватора активации рецепторов белка-1 и эстрогена». Журнал биологической химии. 277 (2): 1229–34. Дои:10.1074 / jbc.M110417200. PMID 11704680.
- ^ Nishitani J, Nishinaka T., Cheng CH, Rong W, Yokoyama KK, Chiu R (февраль 1999 г.). «Привлечение белка ретинобластомы к c-Jun усиливает активность транскрипции, опосредованную сайтом связывания AP-1». Журнал биологической химии. 274 (9): 5454–61. Дои:10.1074 / jbc.274.9.5454. PMID 10026157.
- ^ Wertz IE, O'Rourke KM, Zhang Z, Dornan D, Arnott D, Deshaies RJ, Dixit VM (февраль 2004 г.). «Деэтиолированный-1 человека регулирует c-Jun путем сборки убиквитинлигазы CUL4A» (PDF). Наука. 303 (5662): 1371–4. Bibcode:2004Наука ... 303.1371W. Дои:10.1126 / science.1093549. PMID 14739464.
- ^ Бьянки Е., Денти С., Катена Р., Россетти Дж., Поло С., Гаспарян С., Путиньяно С., Рогге Л., Парди Р. (май 2003 г.). «Характеристика человеческого конститутивного белка 1 фотоморфогенеза, убиквитинлигазы пальца RING, которая взаимодействует с факторами транскрипции Jun и модулирует их транскрипционную активность». Журнал биологической химии. 278 (22): 19682–90. Дои:10.1074 / jbc.M212681200. PMID 12615916.
- ^ а б Хесс Дж, Порт Д, Мунц С., Ангел П. (июнь 2001 г.). «AP-1 и Cbfa / runt физически взаимодействуют и регулируют зависимую от паратироидного гормона экспрессию MMP13 в остеобластах через новый составной элемент 2 / AP-1, специфичный для остеобластов». Журнал биологической химии. 276 (23): 20029–38. Дои:10.1074 / jbc.M010601200. PMID 11274169.
- ^ а б Д'Алонсо Р.К., Селвамуруган Н., Карсенти Г., Партридж, Северная Каролина (январь 2002 г.). «Физическое взаимодействие факторов активатора белка-1 c-Fos и c-Jun с Cbfa1 для активации промотора коллагеназы-3». Журнал биологической химии. 277 (1): 816–22. Дои:10.1074 / jbc.M107082200. PMID 11641401.
- ^ Чжан Ю., Фэн XH, Деринк Р. (август 1998 г.). «Smad3 и Smad4 взаимодействуют с c-Jun / c-Fos, чтобы опосредовать транскрипцию, индуцированную TGF-бета». Природа. 394 (6696): 909–13. Bibcode:1998Натура.394..909Z. Дои:10.1038/29814. PMID 9732876.
- ^ Verrecchia F, Pessah M, Atfi A, Mauviel A (сентябрь 2000 г.). «Фактор некроза опухоли-альфа ингибирует передачу сигналов трансформирующего фактора роста-бета / Smad в дермальных фибробластах человека посредством активации AP-1». Журнал биологической химии. 275 (39): 30226–31. Дои:10.1074 / jbc.M005310200. PMID 10903323.
- ^ Либерати Н.Т., Датто М.Б., Фредерик Дж. П., Шен X, Вонг С., Ружье-Чепмен Е.М., Ван XF (апрель 1999 г.). «Smads связываются непосредственно с семейством Jun факторов транскрипции AP-1». Труды Национальной академии наук Соединенных Штатов Америки. 96 (9): 4844–9. Bibcode:1999PNAS ... 96.4844L. Дои:10.1073 / пнас.96.9.4844. ЧВК 21779. PMID 10220381.
- ^ а б Zhang X, Wrzeszczynska MH, Horvath CM, Darnell JE (октябрь 1999 г.). «Взаимодействующие области в Stat3 и c-Jun, которые участвуют в совместной активации транскрипции». Молекулярная и клеточная биология. 19 (10): 7138–46. Дои:10.1128 / MCB.19.10.7138. ЧВК 84707. PMID 10490649.
- ^ Pessah M, Prunier C, Marais J, Ferrand N, Mazars A, Lallemand F, Gauthier JM, Atfi A (май 2001 г.). «c-Jun взаимодействует с корепрессорным TG-взаимодействующим фактором (TGIF), подавляя транскрипционную активность Smad2». Труды Национальной академии наук Соединенных Штатов Америки. 98 (11): 6198–203. Bibcode:2001ПНАС ... 98.6198П. Дои:10.1073 / pnas.101579798. ЧВК 33445. PMID 11371641.
дальнейшее чтение
- Боманн Д., Бос Т.Дж., Адмон А., Нишимура Т., Фогт П.К., Тьянь Р. (декабрь 1987 г.). «Человеческий протоонкоген c-jun кодирует ДНК-связывающий белок со структурными и функциональными свойствами фактора транскрипции AP-1». Наука. 238 (4832): 1386–92. Bibcode:1987Научный ... 238.1386Б. Дои:10.1126 / science.2825349. PMID 2825349.
- Рамсдорф HJ (декабрь 1996 г.). «Джун: фактор транскрипции и онкопротеин». Журнал молекулярной медицины. 74 (12): 725–47. Дои:10.1007 / s001090050077. PMID 8974016.
- Лю Дж. Л., Кунг Х. Дж. (2001). «Белок MEQ, трансформирующий герпесвирус болезни Марека: аналог c-Jun с альтернативным образом жизни». Гены вирусов. 21 (1–2): 51–64. Дои:10.1023 / А: 1008132313289. PMID 11022789.
- Веласкес Торрес А., Гариглио Видаль П. (2002). «[Возможная роль транскрипционного фактора AP1 в тканеспецифической регуляции вируса папилломы человека]». Revista de Investigacion Clinica. 54 (3): 231–42. PMID 12183893.
- Карамузис М.В., Константинопулос П.А., Папавассилиу А.Г. (февраль 2007 г.). «Активатор фактора транскрипции протеина-1 в канцерогенезе респираторного эпителия». Молекулярные исследования рака. 5 (2): 109–20. Дои:10.1158 / 1541-7786.MCR-06-0311. PMID 17314269.
внешняя ссылка
- c-jun + белки в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- c-jun + Гены в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- Дрозофила Jun-родственный антиген - Интерактивная муха
- FactorBook C-июн
- Человек ИЮНЬ расположение генома и ИЮНЬ страница сведений о генах в Браузер генома UCSC.