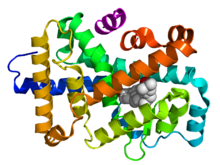
Ядерный рецептор - Nuclear receptor

В области молекулярная биология, ядерные рецепторы являются классом белки находится внутри клеток, которые отвечают за восприятие стероидный препарат и щитовидная железа гормоны и некоторые другие молекулы. В ответ эти рецепторы работают с другими белками, чтобы регулировать выражение конкретных гены, тем самым контролируя разработка, гомеостаз, и метаболизм организма.
Ядерные рецепторы обладают способностью напрямую связываться с ДНК и регулируют экспрессию соседних генов, поэтому эти рецепторы классифицируются как факторы транскрипции.[2][3] Регуляция экспрессии генов ядерными рецепторами обычно происходит только тогда, когда лиганд - молекула, влияющая на поведение рецептора - присутствует. Более конкретно, связывание лиганда с ядерным рецептором приводит к конформационный изменение рецептора, которое, в свою очередь, активирует рецептор, в результате чего повышающее или понижающее регулирование экспрессии генов.
Уникальное свойство ядерных рецепторов, которое отличает их от других классов рецепторы их способность напрямую взаимодействовать и контролировать выражение геномный ДНК. Как следствие, ядерные рецепторы играют ключевую роль как в эмбриональном развитии, так и в гомеостазе взрослых. Как обсуждается ниже, ядерные рецепторы можно классифицировать в соответствии с механизм[4][5] или же гомология.[6][7]
Распространение видов
Ядерные рецепторы специфичны для многоклеточные животные (животные) и не встречаются в протисты, водоросли, грибы, или растения.[8] Среди ранних ветвящихся линий животных с секвенированными геномами сообщалось о двух из губка Амфимедон королевский, два из гребневик Mnemiopsis leidyi[9] четыре из плакозой Trichoplax adhaerens и 17 из книдариец Nematostella vectensis.[10] Всего в организме 270 ядерных рецепторов. нематода C. elegans один,[11] 21 дюйм D. melanogaster и другие насекомые,[12] 73 дюйм данио.[13] У людей, мышей и крыс соответственно 48, 49 и 47 ядерных рецепторов.[14]
Лиганды

Лиганды, которые связываются с ядерными рецепторами и активируют их, включают: липофильный такие вещества как эндогенный гормоны, витамины А и D, и ксенобиотик эндокринные разрушители. Поскольку экспрессия большого количества генов регулируется ядерными рецепторами, лиганды, активирующие эти рецепторы, могут оказывать сильное воздействие на организм. Многие из этих регулируемых генов связаны с различными заболеваниями, что объясняет, почему молекулярные мишени примерно 13% Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) одобренные препараты нацелены на ядерные рецепторы.[15]
Ряд ядерных рецепторов, называемых сиротские рецепторы,[16] не имеют известных (или, по крайней мере, общепризнанных) эндогенных лигандов. Некоторые из этих рецепторов, такие как FXR, LXR, и PPAR связывают ряд промежуточных продуктов метаболизма, таких как жирные кислоты, желчные кислоты и / или стерины, с относительно низким сродством. Следовательно, эти рецепторы могут функционировать как метаболические сенсоры. Другие ядерные рецепторы, такие как МАШИНА и PXR по-видимому, функционируют как сенсоры ксенобиотиков, регулируя экспрессию цитохром P450 ферменты, метаболизирующие эти ксенобиотики.[17]
Структура
Большинство ядерных рецепторов имеют молекулярные массы от 50 000 до 100 000 дальтон.
Ядерные рецепторы имеют модульную структуру и содержат следующие домены:[18][19]
- (А-В) N-концевой регуляторный домен: содержит функцию активации 1 (AF-1), действие которого не зависит от наличия лиганда.[20] Активация транскрипции AF-1 обычно очень слабая, но она действительно действует синергетически с AF-2 в E-домене (см. Ниже), обеспечивая более устойчивую активацию экспрессии гена. Последовательность домена A-B сильно варьируется между различными ядерными рецепторами.
- (С) ДНК-связывающий домен (DBD): Высококонсервативный домен, содержащий два цинковые пальцы связывается с определенными последовательностями ДНК, называемыми элементы гормонального ответа (ОПЧ).
- (D) Шарнирная область: Предполагается, что это гибкий домен, который соединяет DBD с LBD. Влияет на внутриклеточный трафик и субклеточное распределение с целевой пептид последовательность.
- (E) Лиганд-связывающий домен (LBD): Умеренно консервативная последовательность и высококонсервативная структура между различными ядерными рецепторами. В структура LBD называется альфа спиральный бутерброд складывать в котором три антипараллельных альфа-спирали («начинка для сэндвичей») фланкированы двумя альфа-спиралями с одной стороны и тремя - с другой («хлеб»). Полость для связывания лиганда находится внутри LBD и чуть ниже трех антипараллельных альфа-спиральных сэндвич-«наполнителей». Наряду с DBD, LBD вносит вклад в интерфейс димеризации рецептора и, кроме того, связывает коактиватор и корепрессор белки. LBD также содержит функцию активации 2 (AF-2), действие которого зависит от наличия связанного лиганда, контролируемого конформацией спирали 12 (H12).[20]
- (F) C-терминал домен: Высоко вариабельная последовательность между различными ядерными рецепторами.
N-концевой (A / B), ДНК-связывающий (C) и лиганд-связывающий (E) домены являются независимо хорошо сложенными и структурно стабильными, в то время как шарнирная область (D) и необязательные C-концевые (F) домены могут быть конформационными. гибкий и беспорядочный.[21] Относительные ориентации доменов сильно различаются при сравнении трех известных многодоменных кристаллических структур, две из которых связываются с DR1 (DBD, разделенные 1 п.н.),[1][22] одно связывание с DR4 (по 4 п.н.).[23]
 Структурная организация ядерных рецепторов. Вершина - Схема 1D аминокислотная последовательность ядерного рецептора. Нижний - 3D-структуры областей DBD (связанных с ДНК) и LBD (связанных с гормоном) ядерного рецептора. Показанные конструкции относятся к рецептор эстрогена. Экспериментальные структуры N-концевого домена (A / B), шарнирной области (D) и C-концевого домена (F) не определены, поэтому они представлены красными, пурпурными и оранжевыми пунктирными линиями соответственно. |
|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Механизм действия
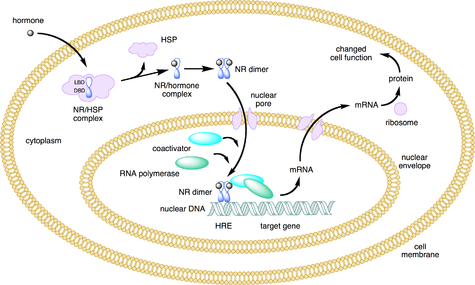

Ядерные рецепторы - это многофункциональные белки, которые преобразовывать сигналы их родственных лиганды. Ядерные рецепторы (NR) можно разделить на два широких класса в соответствии с их механизмом действия и субклеточным распределением в отсутствие лиганда.
Небольшие липофильные вещества, такие как природные гормоны, диффундируют через клеточную мембрану и связываются с ядерными рецепторами, расположенными в цитозоле (NR типа I) или ядре (NR типа II) клетки. Связывание вызывает конформационное изменение рецептора, которое, в зависимости от класса рецептора, запускает каскад последующих событий, которые направляют NR в сайты регуляции транскрипции ДНК, что приводит к усилению или понижению регуляции экспрессии генов. Обычно они действуют как гомо / гетеродимеры.[26] Кроме того, также были идентифицированы два дополнительных класса: тип III, который является вариантом типа I, и тип IV, которые связывают ДНК в виде мономеров.[4]
Соответственно, ядерные рецепторы можно подразделить на следующие четыре механистических класса:[4][5]
Тип I
Связывание лиганда с ядерными рецепторами типа I в цитозоле приводит к диссоциация из белки теплового шока, гомо-димеризация, транслокация (т.е., активный транспорт ) от цитоплазма в ядро клетки, и связывание с конкретными последовательностями ДНК известный как элементы гормонального ответа (ОПЧ). Ядерные рецепторы типа I связываются с HRE, состоящими из двух полусайтов, разделенных ДНК переменной длины, и второй полусайт имеет последовательность, инвертированную по сравнению с первым (инвертированный повтор). Ядерные рецепторы типа I включают членов подсемейства 3, таких как рецептор андрогенов, рецепторы эстрогена, рецептор глюкокортикоидов, и рецептор прогестерона.[27]
Было отмечено, что некоторые из ядерных рецепторов подсемейства 2 NR могут связываться с прямым повторением вместо перевернутый повтор ОПЧ. Кроме того, некоторые ядерные рецепторы связываются либо в виде мономеров, либо в виде димеров, при этом только один ДНК-связывающий домен рецептора присоединяется к одному полусайту HRE. Эти ядерные рецепторы считаются сиротские рецепторы, так как их эндогенные лиганды до сих пор неизвестны.
Ядерный рецептор / ДНК сложный затем привлекает другие белки, которые расшифровывать ДНК ниже по течению от ОПЧ в информационная РНК и в конце концов белок, что вызывает изменение функции клеток.
Тип II
Рецепторы типа II, в отличие от типа I, сохраняются в ядре независимо от статуса связывания лиганда и, кроме того, связываются как гетеро-димеры (обычно с RXR ) к ДНК.[26] В отсутствие лиганда ядерные рецепторы типа II часто образуют комплексы с корепрессор белки. Связывание лиганда с ядерным рецептором вызывает диссоциацию корепрессора и рекрутирование коактиватор белки. Дополнительные белки, включая РНК-полимераза затем рекрутируются в комплекс NR / ДНК, который транскрибирует ДНК в информационную РНК.
Ядерные рецепторы типа II включают в основном подсемейство 1, например рецептор ретиноевой кислоты, рецептор ретиноида X и рецептор гормона щитовидной железы.[28]
Тип III
Ядерные рецепторы типа III (в основном NR подсемейства 2) подобны рецепторам типа I в том, что оба класса связываются с ДНК как гомодимеры. Однако ядерные рецепторы типа III, в отличие от типа I, связываются с прямым повторением вместо перевернутый повтор ОПЧ.
Тип IV
Ядерные рецепторы типа IV связываются как мономеры или димеры, но только один ДНК-связывающий домен рецептора связывается с одним полусайтом HRE. Примеры рецепторов типа IV встречаются в большинстве подсемейств NR.
Корегуляторные белки
Ядерные рецепторы, связанные с элементами гормонального ответа, привлекают значительное количество других белков (называемых корегуляторы транскрипции ), которые облегчают или ингибируют транскрипцию связанного гена-мишени в мРНК.[29][30] Функции этих корегуляторов разнообразны и включают: хроматин ремоделирование (делая целевой ген более или менее доступным для транскрипции) или мостиковую функцию для стабилизации связывания других белков-регуляторов. Ядерные рецепторы могут специфически связываться с рядом белков-корегуляторов и тем самым влиять на клеточные механизмы передачи сигнала как напрямую, так и косвенно.[31]
Коактиваторы
Связывание агонистических лигандов (см. Раздел ниже) с ядерными рецепторами индуцирует конформацию рецептора, которая предпочтительно связывает коактиватор белки. Эти белки часто обладают внутренним гистонацетилтрансфераза (HAT) активность, которая ослабляет ассоциацию гистоны к ДНК и, следовательно, способствует транскрипции генов.
Corepressors
Связывание антагонистических лигандов с ядерными рецепторами, напротив, индуцирует конформацию рецептора, которая предпочтительно связывает корепрессор белки. Эти белки, в свою очередь, привлекают гистоновые деацетилазы (HDAC), что усиливает ассоциацию гистонов с ДНК и, следовательно, подавляет транскрипцию генов.
Агонизм против антагонизма
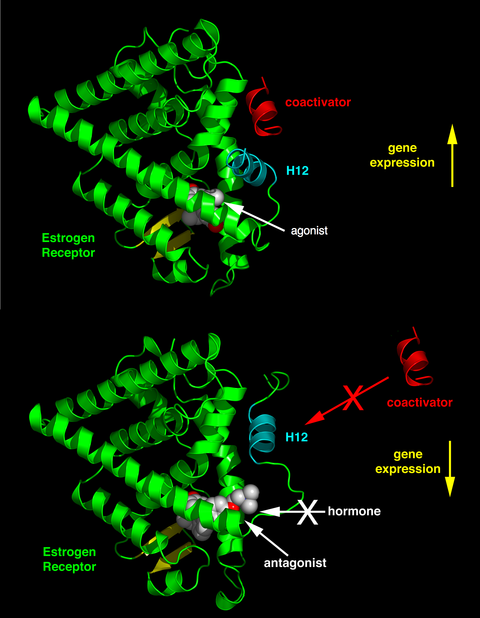
В зависимости от задействованного рецептора, химической структуры лиганда и ткани, которая подвергается воздействию, лиганды ядерного рецептора могут проявлять резко разнообразные эффекты в диапазоне от агонизма до антагонизма и до обратного агонизма.[34]
Агонисты
Активность эндогенных лигандов (например, гормонов эстрадиол и тестостерон ), когда они связаны со своими родственными ядерными рецепторами, обычно стимулируют экспрессию генов. Эта стимуляция экспрессии гена лигандом называется агонист отклик. Агонистические эффекты эндогенных гормонов также могут имитироваться некоторыми синтетическими лигандами, например, рецептор глюкокортикоидов противовоспалительный препарат дексаметазон. Лиганды-агонисты работают, индуцируя конформацию рецептора, которая способствует связыванию коактиватора (см. Верхнюю половину рисунка справа).
Антагонисты
Другие синтетические лиганды ядерных рецепторов не оказывают заметного влияния на транскрипцию генов в отсутствие эндогенного лиганда. Однако они блокируют действие агониста за счет конкурентного связывания с тем же сайтом связывания в ядерном рецепторе. Эти лиганды называют антагонистами. Примером лекарственного средства антагонистического действия ядерных рецепторов является мифепристон который привязан к глюкокортикоид и прогестерон рецепторы и, следовательно, блокирует активность эндогенных гормонов кортизол и прогестерон соответственно. Лиганды-антагонисты работают, индуцируя конформацию рецептора, которая предотвращает коактиватор и способствует связыванию корепрессора (см. Нижнюю половину рисунка справа).
Обратные агонисты
Наконец, некоторые ядерные рецепторы способствуют низкому уровню транскрипции генов в отсутствие агонистов (также называемой базальной или конститутивной активностью). Синтетические лиганды, которые снижают этот базальный уровень активности ядерных рецепторов, известны как обратные агонисты.[35]
Селективные модуляторы рецепторов
Ряд лекарств, которые действуют через ядерные рецепторы, проявляют агонистический ответ в одних тканях и антагонистический ответ в других тканях. Такое поведение может иметь существенные преимущества, поскольку оно может позволить сохранить желаемые полезные терапевтические эффекты лекарственного средства при минимизации нежелательных побочных эффектов. Лекарства с таким смешанным профилем действия агонистов / антагонистов называются селективными модуляторами рецепторов (SRM). Примеры включают селективные модуляторы рецепторов андрогенов (SARM ), Селективные модуляторы эстрогеновых рецепторов (SERM ) и селективные модуляторы рецепторов прогестерона (SPRM ). Механизм действия SRM может варьироваться в зависимости от химической структуры лиганда и задействованного рецептора, однако считается, что многие SRM работают, способствуя конформации рецептора, которая тесно сбалансирована между агонизмом и антагонизмом. В тканях, где концентрация коактиватор белков выше, чем корепрессоры, равновесие смещается в сторону агонистов. И наоборот, в тканях, где корепрессоры доминируют, лиганд ведет себя как антагонист.[36]
Альтернативные механизмы

Трансрепрессия
Наиболее распространенный механизм действия ядерного рецептора включает прямое связывание ядерного рецептора с элементом ответа гормона ДНК. Этот механизм упоминается как трансактивация. Однако некоторые ядерные рецепторы обладают способностью не только напрямую связываться с ДНК, но и с другими факторами транскрипции. Это связывание часто приводит к дезактивации второго фактора транскрипции в процессе, известном как трансрепрессия.[37] Одним из примеров ядерного рецептора, который способен трансрепрессировать, является рецептор глюкокортикоидов (GR). Кроме того, некоторые лиганды GR, известные как селективные агонисты рецепторов глюкокортикоидов (SEGRA ) способны активировать GR таким образом, что GR сильнее трансрепрессирует, чем трансактивирует. Эта селективность увеличивает разделение между желаемыми противовоспалительное средство эффекты и нежелательные метаболические побочные эффекты этих селективных глюкокортикоиды.
Негеномный
Классические прямые эффекты ядерных рецепторов на регуляцию генов обычно занимают несколько часов, прежде чем функциональный эффект проявляется в клетках из-за большого количества промежуточных этапов между активацией ядерных рецепторов и изменениями уровней экспрессии белка. Однако было замечено, что многие эффекты применения ядерных гормонов, такие как изменения активности ионных каналов, происходят в течение нескольких минут, что несовместимо с классическим механизмом действия ядерных рецепторов. Хотя молекулярная мишень для этих негеномных эффектов ядерных рецепторов окончательно не продемонстрирована, была выдвинута гипотеза, что существуют варианты ядерных рецепторов, которые связаны с мембраной, а не локализуются в цитозоле или ядре. Кроме того, эти ассоциированные с мембраной рецепторы функционируют альтернативно. преобразование сигнала механизмы, не включающие генную регуляцию.[38][39]
Хотя была выдвинута гипотеза, что существует несколько мембранно-ассоциированных рецепторов ядерных гормонов, было показано, что для многих быстрых эффектов требуются канонические ядерные рецепторы.[40][41] Однако проверка относительной важности геномных и негеномных механизмов in vivo была предотвращена из-за отсутствия специфических молекулярных механизмов негеномных эффектов, которые могли бы быть заблокированы мутацией рецептора без нарушения его прямого воздействия на экспрессию генов.
Молекулярный механизм негеномной передачи сигналов через ядерный рецептор гормона щитовидной железы. TRβ включает фосфатидилинозитол-3-киназу (PI3K ).[42] Эту сигнализацию можно заблокировать одним тирозин к фенилаланин замена TRβ без нарушения прямой регуляции гена.[43] Когда мыши были созданы с этой единственной консервативной аминокислотной заменой в TRβ,[43] синаптический созревание и пластичность в гиппокамп был нарушен почти так же эффективно, как и полное блокирование синтеза гормонов щитовидной железы.[44] Этот механизм, по-видимому, сохраняется у всех млекопитающих, но не у TRα или любые другие ядерные рецепторы. Таким образом, фосфотирозин-зависимая ассоциация TRβ с PI3K обеспечивает потенциальный механизм для интеграции регуляции развития и метаболизма тироидным гормоном и рецепторными тирозинкиназами. Кроме того, передача сигналов гормона щитовидной железы через PI3K может изменять экспрессию генов.[45]
Члены семьи
Ниже приводится список 48 известных ядерных рецепторов человека (и их ортологи у других видов)[14][46] классифицированы в соответствии с гомология последовательностей.[6][7] В список также входят избранные члены семьи, у которых отсутствуют человеческие ортологи (символ NRNC выделен желтым цветом).
| Подсемейство | Группа | Член | ||||||
|---|---|---|---|---|---|---|---|---|
| Символ NRNC[6] | Сокращение | Имя | Ген | Лиганд (ы) | ||||
| 1 | Рецептор гормона щитовидной железы | А | Рецептор гормона щитовидной железы | NR1A1 | TRα | Рецептор гормона щитовидной железы-α | THRA | гормон щитовидной железы |
| NR1A2 | TRβ | Рецептор гормона щитовидной железы-β | THRB | |||||
| B | Рецептор ретиноевой кислоты | NR1B1 | RARα | Рецептор ретиноевой кислоты-α | RARA | витамин А и родственные соединения | ||
| NR1B2 | RARβ | Рецептор ретиноевой кислоты-β | RARB | |||||
| NR1B3 | RARγ | Рецептор ретиноевой кислоты-γ | RARG | |||||
| C | Рецептор, активируемый пролифератором пероксисом | NR1C1 | PPARα | Рецептор-α, активируемый пролифератором пероксисом | PPARA | жирные кислоты, простагландины | ||
| NR1C2 | PPAR-β / δ | Рецептор-β / δ, активируемый пролифератором пероксисом | PPARD | |||||
| NR1C3 | PPARγ | Рецептор-γ, активируемый пролифератором пероксисом | PPARG | |||||
| D | Rev-ErbA | NR1D1 | Rev-ErbAα | Rev-ErbAα | NR1D1 | гем | ||
| NR1D2 | Rev-ErbAβ | Rev-ErbAα | NR1D2 | |||||
| E | E78C-подобный (членистоногие, трематоды, мультики, нематоды)[46][47] | NR1E1 | Eip78C | Белок 78C, индуцированный экдизоном | Eip78C | |||
| F | RAR-родственный орфанный рецептор | NR1F1 | RORα | RAR-родственный орфанный рецептор-α | RORA | холестерин, ATRA | ||
| NR1F2 | RORβ | RAR-связанный орфанный рецептор-β | RORB | |||||
| NR1F3 | RORγ | RAR-родственный орфанный рецептор-γ | RORC | |||||
| грамм | CNR14-подобный (нематода)[46] | NR1G1 | секс-1 | Рецептор стероидного гормона cnr14[48] | секс-1 | |||
| ЧАС | Х-рецептор печени -подобно | NR1H1 | EcR | Рецептор экдизона, EcR (членистоногие) | EcR | экдистероиды | ||
| NR1H2 | LXRβ | Х-рецептор-β печени | NR1H2 | оксистерины | ||||
| NR1H3 | LXRα | Х-рецептор-α печени | NR1H3 | |||||
| NR1H4 | FXR | Рецептор фарнезоида X | NR1H4 | |||||
| NR1H5[49] | FXR-β | Фарнезоидный X рецептор-β (псевдоген у человека) | NR1H5P | |||||
| я | Подобный рецептору витамина D | NR1I1 | VDR | Рецептор витамина D | VDR | Витамин Д | ||
| NR1I2 | PXR | Рецептор прегнана X | NR1I2 | ксенобиотики | ||||
| NR1I3 | МАШИНА | Конститутивный рецептор андростана | NR1I3 | андростан | ||||
| J | Hr96-подобный[46] | NR1J1 | 96 грн. /Даф-12 | Рецептор ядерного гормона HR96 | 96 грн. | холестрол /дафахроновая кислота[50] | ||
| NR1J2 | ||||||||
| NR1J3 | ||||||||
| K | Hr1-подобный[46] | NR1K1 | Hr1 | Рецептор ядерного гормона HR1 | ||||
| 2 | Ретиноид X рецептороподобный | А | Ядерный фактор гепатоцитов-4 | NR2A1 | HNF4α | Ядерный фактор гепатоцитов-4-α | HNF4A | жирные кислоты |
| NR2A2 | HNF4γ | Ядерный фактор гепатоцитов-4-γ | HNF4G | |||||
| B | Ретиноидный рецептор X | NR2B1 | RXRα | Ретиноидный рецептор X-α | RXRA | ретиноиды | ||
| NR2B2 | RXRβ | Ретиноидный рецептор X-β | RXRB | |||||
| NR2B3 | RXRγ | Ретиноидный рецептор X-γ | RXRG | |||||
| NR2B4 | USP | Белок Ultraspiracle (членистоногие) | usp | фосфолипиды[51] | ||||
| C | Рецептор яичка | NR2C1 | TR2 | Рецептор яичка 2 | NR2C1 | |||
| NR2C2 | TR4 | Рецептор яичек 4 | NR2C2 | |||||
| E | TLX / PNR | NR2E1 | TLX | Гомолог бесхвостого гена дрозофилы | NR2E1 | |||
| NR2E3 | PNR | Фоторецепторный клеточно-специфический ядерный рецептор | NR2E3 | |||||
| F | КУПЕ /УХО | NR2F1 | КУП-TFI | Куриный овальбумин перед промотором транскрипционного фактора I | NR2F1 | |||
| NR2F2 | COUP-TFII | Куриный овальбумин перед промотором фактора транскрипции II | NR2F2 | ретиноевая кислота (слабый)[52] | ||||
| NR2F6 | EAR-2 | Связанный с V-erbA | NR2F6 | |||||
| 3 | Рецептор эстрогена | А | Рецептор эстрогена | NR3A1 | ERα | Рецептор эстрогена-α | ESR1 | эстрогены |
| NR3A2 | ERβ | Рецептор эстрогена-β | ESR2 | |||||
| B | Рецептор, связанный с эстрогеном | NR3B1 | ERRα | Связанный с эстрогеном рецептор-α | ESRRA | |||
| NR3B2 | ERRβ | Связанный с эстрогеном рецептор-β | ESRRB | |||||
| NR3B3 | ERRγ | Эстроген-связанный рецептор-γ | ESRRG | |||||
| C | 3-кетостероидные рецепторы | NR3C1 | GR | Рецептор глюкокортикоидов | NR3C1 | кортизол | ||
| NR3C2 | МИСТЕР | Минералокортикоидный рецептор | NR3C2 | альдостерон | ||||
| NR3C3 | PR | Рецептор прогестерона | PGR | прогестерон | ||||
| NR3C4 | AR | Рецептор андрогенов | AR | тестостерон | ||||
| D | Рецептор эстрогена (в лофотрохозоа )[53] | NR3D | ||||||
| E | Рецептор эстрогена (в книдария )[54] | NR3E | ||||||
| F | Рецептор эстрогена (в плакозоа )[54] | NR3F | ||||||
| 4 | Фактор роста нервов IB-подобный | А | NGFIB / NURR1 / NOR1 | NR4A1 | NGFIB | Фактор роста нервов IB | NR4A1 | |
| NR4A2 | NURR1 | Связанные с ядерным рецептором 1 | NR4A2 | |||||
| NR4A3 | NOR1 | Орфанный рецептор 1, происходящий из нейронов | NR4A3 | |||||
| 5 | Стероидогенный Фактороподобный | А | SF1 / LRH1 | NR5A1 | SF1 | Стероидогенный фактор 1 | NR5A1 | фосфатидилинозиты |
| NR5A2 | LRH-1 | Гомолог-1 рецепторов печени | NR5A2 | фосфатидилинозиты | ||||
| B | Hr39-подобный | NR5B1[46] | HR39 /FTZ-F1 | Рецептор ядерного гормона фуши таразу фактор I бета | 39 грн. | |||
| 6 | Ядерный фактор зародышевой клетки | А | GCNF | NR6A1 | GCNF | Ядерный фактор зародышевой клетки | NR6A1 | |
| 7 | NR с двумя ДНК-связывающими доменами[46][55] (плоские черви, моллюски, членистоногие) | А | 2DBD-NRα | NR7A1 | ||||
| B | 2DBD-NRβ | NR7B1 | ||||||
| C | 2DBD-NRγ | NR7C1 | членистоногие "α / β" | |||||
| 8 | NR8[56] (Eumetazoa ) | А | NR8A | NR8A1 | CgNR8A1 | Ядерный рецептор 8 | AKG49571 | |
| 0 | Разное (отсутствует LBD или DBD) | А | knr / knrl / egon[46] (членистоногие) | NR0A1 | KNI | Зиготические белковые ножки | knl | |
| B | DAX / SHP | NR0B1 | DAX1 | Изменение пола в зависимости от дозировки, критическая область гипоплазии надпочечников, на хромосоме X, ген 1 | NR0B1 | |||
| NR0B2 | SHP | Малый гетеродимерный партнер | NR0B2 | |||||
Из двух 0-семейств 0A имеет DBD, подобную семейству 1, а 0B имеет очень уникальный LBD. Второй DBD семейства 7, вероятно, относится к DBD семейства 1. Три NR, вероятно, семьи-1 от Биомфалария глабрата обладают DBD вместе с семейством 0B-подобных LBD.[46] Размещение C. elegans нчр-1 (Q21878) оспаривается: хотя большинство источников называют его NR1K1,[46] ручная аннотация на WormBase считает его членом NR2A.[57] Раньше была группа 2D, в которой единственным членом был Дрозофилия HR78 / NR1D1 (Q24142) и ортологов, но позже из-за большого сходства она была объединена в группу 2C, образуя «группу 2C / D».[46] Исследования нокаута на мышах и плодовых мушках подтверждают наличие такой объединенной группы.[58]
Эволюция
Темой дебатов была идентичность предкового ядерного рецептора как связывающего лиганд или сиротский рецептор. Эта дискуссия началась более двадцати пяти лет назад, когда первыми лигандами были идентифицированы стероиды млекопитающих и гормоны щитовидной железы.[59] Вскоре после этого идентификация рецептора экдизона у дрозофилы привела к представлению о том, что ядерные рецепторы являются гормональными рецепторами, которые связывают лиганды с наномолярным сродством. В то время тремя известными лигандами ядерных рецепторов были стероиды, ретиноиды и гормон щитовидной железы, и из этих трех как стероиды, так и ретиноиды были продуктами метаболизма терпеноидов. Таким образом, было постулировано, что предковый рецептор был связан с молекулой терпеноида.[60]
В 1992 году сравнение ДНК-связывающего домена всех известных ядерных рецепторов привело к построению филогенного дерева ядерных рецепторов, которое показало, что все ядерные рецепторы имели общего предка.[61] В результате были увеличены усилия по раскрытию состояния первого ядерного рецептора, и к 1997 году была предложена альтернативная гипотеза: предковый ядерный рецептор был сиротским рецептором, и со временем он приобрел способность связываться с лигандом.[7] Эта гипотеза была предложена на основании следующих аргументов:
- Последовательности ядерных рецепторов, которые были идентифицированы у самых ранних многоклеточных животных (книдарий и Шистосома) все были членами групп рецепторов COUP-TF, RXR и FTZ-F1. И COUP-TF, и FTZ-F1 являются рецепторами-сиротами, а RXR, как обнаружено, связывает лиганд только у позвоночных.[62]
- В то время как рецепторы-сироты имели известные гомологи членистоногих, ортологи рецепторов лигандированных позвоночных не были идентифицированы за пределами позвоночных, что позволяет предположить, что рецепторы-сироты старше лиганд-рецепторов.[63]
- Рецепторы-сироты встречаются среди всех шести подсемейств ядерных рецепторов, а лиганд-зависимые рецепторы - среди трех.[7] Таким образом, поскольку лиганд-зависимые рецепторы считались преимущественно членами недавних подсемейств, казалось логичным, что они приобрели способность связывать лиганды независимо.
- Филогенетическое положение данного ядерного рецептора в дереве коррелирует с его ДНК-связывающим доменом и способностью к димеризации, но не выявлено никакой связи между лиганд-зависимым ядерным рецептором и химической природой его лиганда. В дополнение к этому, эволюционные взаимоотношения между лиганд-зависимыми рецепторами не имели большого смысла, поскольку близкородственные рецепторы подсемейств связывали лиганды, происходящие из совершенно разных биосинтетических путей (например, TR и RAR). С другой стороны, подсемейства, которые не являются эволюционно связанными, связывают сходные лиганды (RAR и RXR оба связывают полностью транс- и 9-цис-ретиноевую кислоту соответственно).[63]
- В 1997 году было обнаружено, что ядерные рецепторы не существуют в статических конформациях вне и во времени, но что лиганд может изменять равновесие между двумя состояниями. Более того, было обнаружено, что ядерные рецепторы могут регулироваться лиганд-независимым образом посредством фосфорилирования или других посттрансляционных модификаций. Таким образом, это предоставило механизм того, как предковый сиротский рецептор регулируется лиганд-независимым образом, и объяснил, почему лиганд-связывающий домен был консервативным.[63]
В течение следующих 10 лет были проведены эксперименты, чтобы проверить эту гипотезу, и вскоре появились контраргументы:
- Ядерные рецепторы были идентифицированы во вновь секвенированном геноме демоспуба. Амфимедон королевский, член древнейшего многоклеточного типа Porifera. В A. queenslandica геном содержит два ядерных рецептора, известных как AqNR1 и AqNR2, и оба были охарактеризованы как связывающиеся и регулируемые лигандами.[64]
- Гомологи лиганд-зависимых рецепторов позвоночных были обнаружены вне позвоночных у моллюсков и платихельминтов. Кроме того, было обнаружено, что ядерные рецепторы, обнаруженные у книдарий, имеют структурные лиганды у млекопитающих, что может отражать наследственную ситуацию.
- Два предполагаемых сиротские рецепторы, HNF4 и USP с помощью структурного и масс-спектрометрического анализа было обнаружено, что они связывают жирные кислоты и фосфолипиды соответственно.[51]
- Ядерные рецепторы и лиганды оказались гораздо менее специфичными, чем считалось ранее. Ретиноиды могут связывать рецепторы млекопитающих, отличные от RAR и RXR, такие как PPAR, RORb или COUP-TFII. Кроме того, RXR чувствителен к широкому спектру молекул, включая ретиноиды, жирные кислоты и фосфолипиды.[65]
- Изучение эволюции стероидных рецепторов показало, что предковые стероидные рецепторы могли связывать лиганд, эстрадиол. И наоборот, рецептор эстрогена, обнаруженный у моллюсков, конститутивно активен и не связывает гормоны, связанные с эстрогеном. Таким образом, это предоставило пример того, как предковый лиганд-зависимый рецептор мог потерять свою способность связывать лиганды.[66]
Комбинация этих недавних доказательств, а также глубокого исследования физической структуры лиганд-связывающего домена ядерного рецептора привело к появлению новой гипотезы относительно предкового состояния ядерного рецептора. Эта гипотеза предполагает, что предковый рецептор может действовать как липидный сенсор со способностью связывать, хотя и довольно слабо, несколько различных гидрофобных молекул, таких как ретиноиды, стероиды, гемы и жирные кислоты. Обладая способностью взаимодействовать с множеством соединений, этот рецептор из-за дупликаций либо утратит свою способность к лиганд-зависимой активности, либо специализируется на высокоспецифическом рецепторе для конкретной молекулы.[65]
История
Ниже приводится краткая подборка ключевых событий в истории исследований ядерных рецепторов.[67]
- 1905 – Эрнест Старлинг придумал слово гормон
- 1926 – Эдвард Кэлвин Кендалл и Тадеус Райхштейн изолировали и определили структуры кортизон и тироксин
- 1929 – Адольф Бутенандт и Эдвард Адельберт Дуази - самостоятельно выделил и определил структуру эстроген
- 1958 – Элвуд Дженсен - изолировал рецептор эстрогена
- 1980-е годы - клонирование рецепторов эстрогенов, глюкокортикоидов и гормонов щитовидной железы Пьер Шамбон, Рональд Эванс, и Бьорн Веннстрём соответственно
- 2004 - Пьер Шамбон, Рональд Эванс и Элвуд Дженсен были награждены Премия Альберта Ласкера за фундаментальные медицинские исследования, награда, которая часто предшествует Нобелевская премия по медицине
Смотрите также
Рекомендации
- ^ а б PDB: 3E00; Чандра В., Хуанг П., Хамуро Ю., Рагурам С., Ван Ю., Беррис Т. П., Растинежад Ф. (ноябрь 2008 г.). «Структура интактного комплекса PPAR-гамма-RXR-ядерный рецептор на ДНК». Природа. 456 (7220): 350–6. Дои:10.1038 / природа07413. ЧВК 2743566. PMID 19043829.
- ^ Эванс Р.М. (май 1988 г.). «Суперсемейство рецепторов стероидов и гормонов щитовидной железы». Наука. 240 (4854): 889–95. Bibcode:1988Научный ... 240..889E. Дои:10.1126 / science.3283939. ЧВК 6159881. PMID 3283939.
- ^ Олефский Ю.М. (октябрь 2001 г.). "Серия мини-обзоров ядерных рецепторов". Журнал биологической химии. 276 (40): 36863–4. Дои:10.1074 / jbc.R100047200. PMID 11459855. S2CID 5497175.
- ^ а б c Mangelsdorf DJ, Thummel C, Beato M, Herrlich P, Schütz G, Umesono K, Blumberg B, Kastner P, Mark M, Chambon P, Evans RM (декабрь 1995 г.). «Надсемейство ядерных рецепторов: второе десятилетие». Клетка. 83 (6): 835–9. Дои:10.1016 / 0092-8674 (95) 90199-Х. ЧВК 6159888. PMID 8521507.
- ^ а б Новац Н., Хайнцель Т. (декабрь 2004 г.). «Ядерные рецепторы: обзор и классификация». Текущие целевые показатели по лекарствам. Воспаление и аллергия. 3 (4): 335–46. Дои:10.2174/1568010042634541. PMID 15584884.
- ^ а б c Комитет по номенклатуре ядерных рецепторов (апрель 1999 г.). «Единая номенклатурная система надсемейства ядерных рецепторов». Клетка. 97 (2): 161–3. Дои:10.1016 / S0092-8674 (00) 80726-6. PMID 10219237. S2CID 36659104.
- ^ а б c d Лауде V (декабрь 1997 г.). «Эволюция надсемейства ядерных рецепторов: ранняя диверсификация от предкового сиротского рецептора». Журнал молекулярной эндокринологии. 19 (3): 207–26. Дои:10.1677 / jme.0.0190207. PMID 9460643. S2CID 16419929.
- ^ Escriva H, Langlois MC, Mendonça RL, Pierce R, Laudet V (май 1998 г.). «Эволюция и диверсификация надсемейства ядерных рецепторов». Летопись Нью-Йоркской академии наук. 839 (1): 143–6. Bibcode:1998НЯСА.839..143Е. Дои:10.1111 / j.1749-6632.1998.tb10747.x. PMID 9629140. S2CID 11164838.
- ^ Райцель А.М., Панг К., Райан Дж. Ф., Малликин Дж. К., Мартиндейл М. К., Баксеванис А. Д., Таррант А. М. (февраль 2011 г.). «Ядерные рецепторы гребневика Mnemiopsis leidyi лишены ДНК-связывающего домена с цинковыми пальцами: клон-специфическая потеря или наследственное состояние при появлении надсемейства ядерных рецепторов?». EvoDevo. 2 (1): 3. Дои:10.1186/2041-9139-2-3. ЧВК 3038971. PMID 21291545.
- ^ Бриджем Дж. Т., Эйк Г. Н., Ларру С., Дешпанде К., Хармс М. Дж., Готье М. Е., Ортлунд Е. А., Дегнан Б. М., Торнтон Дж. В. (октябрь 2010 г.). «Эволюция белка путем молекулярной обработки: диверсификация суперсемейства ядерных рецепторов от лиганд-зависимого предка». PLOS Биология. 8 (10): e1000497. Дои:10.1371 / journal.pbio.1000497. ЧВК 2950128. PMID 20957188.
- ^ Слудер А.Е., Майна CV (апрель 2001 г.). «Ядерные рецепторы нематод: темы и вариации». Тенденции в генетике. 17 (4): 206–13. Дои:10.1016 / S0168-9525 (01) 02242-9. PMID 11275326.
- ^ Читл Джарвела AM, Pick L (2017). «Функция и эволюция ядерных рецепторов в эмбриональном развитии насекомых». Актуальные темы биологии развития. 125: 39–70. Дои:10.1016 / bs.ctdb.2017.01.003. ISBN 9780128021729. PMID 28527580.
- ^ Шааф MJ (2017). «Исследование ядерных рецепторов у рыбок данио». Журнал молекулярной эндокринологии. 59 (1): R65 – R76. Дои:10.1530 / JME-17-0031. PMID 28438785.
- ^ а б Zhang Z, Burch PE, Cooney AJ, Lanz RB, Pereira FA, Wu J, Gibbs RA, Weinstock G, Wheeler DA (апрель 2004 г.). «Геномный анализ семейства ядерных рецепторов: новое понимание структуры, регуляции и эволюции генома крысы». Геномные исследования. 14 (4): 580–90. Дои:10.1101 / гр.2160004. ЧВК 383302. PMID 15059999.
- ^ Overington JP, Аль-Лазикани Б., Хопкинс А.Л. (декабрь 2006 г.). «Сколько существует мишеней для наркотиков?». Обзоры природы. Открытие наркотиков. 5 (12): 993–6. Дои:10.1038 / nrd2199. PMID 17139284. S2CID 11979420.
- ^ Бенуа Дж., Куни А., Жигер В., Ингрэм Х., Лазар М., Мускат Дж., Перлманн Т., Рено Дж. П., Швабе Дж., Сладек Ф., Цай М. Дж., Лауде В. (декабрь 2006 г.). "Международный союз фармакологии. LXVI. Орфанные ядерные рецепторы". Фармакологические обзоры. 58 (4): 798–836. Дои:10.1124 / пр.58.4.10. PMID 17132856. S2CID 2619263.
- ^ Мохан Р., Хейман Р.А. (2003). «Модуляторы орфанных ядерных рецепторов». Актуальные темы медицинской химии. 3 (14): 1637–47. Дои:10.2174/1568026033451709. PMID 14683519.
- ^ Кумар Р., Томпсон Э.Б. (май 1999 г.). «Строение рецепторов ядерных гормонов». Стероиды. 64 (5): 310–9. Дои:10.1016 / S0039-128X (99) 00014-8. PMID 10406480. S2CID 18333397.
- ^ Klinge CM (май 2000 г.). «Взаимодействие рецептора эстрогена с коактиваторами и корепрессорами». Стероиды. 65 (5): 227–51. Дои:10.1016 / S0039-128X (99) 00107-5. PMID 10751636. S2CID 41160722.
- ^ а б Варнмарк А., Тройтер Е., Райт А. П., Густафссон Дж. А. (октябрь 2003 г.). «Активационные функции 1 и 2 ядерных рецепторов: молекулярные стратегии транскрипционной активации». Молекулярная эндокринология. 17 (10): 1901–9. Дои:10.1210 / me.2002-0384. PMID 12893880.
- ^ Уэтерман Р.В., Флеттерик Р.Дж., Сканлан Т.С. (1999). «Лиганды ядерного рецептора и лиганд-связывающие домены». Ежегодный обзор биохимии. 68: 559–81. Дои:10.1146 / annurev.biochem.68.1.559. PMID 10872460.
- ^ Чандра В., Хуанг П., Потлури Н., Ву Д., Ким И., Растинежад Ф. (март 2013 г.). «Мультидоменная интеграция в структуру ядерного рецепторного комплекса HNF-4α». Природа. 495 (7441): 394–8. Bibcode:2013Натура.495..394C. Дои:10.1038 / природа11966. ЧВК 3606643. PMID 23485969.
- ^ Лу X, Toresson G, Benod C, Suh JH, Philips KJ, Webb P, Gustafsson JA (март 2014 г.). «Структура гетеродимера ретиноидного рецептора X α-рецептора X печени β (RXRα-LXRβ) на ДНК». Структурная и молекулярная биология природы. 21 (3): 277–81. Дои:10.1038 / nsmb.2778. PMID 24561505. S2CID 23226682.
- ^ PDB: 2C7A; Roemer SC, Donham DC, Sherman L, Pon VH, Edwards DP, Churchill ME (декабрь 2006 г.). «Структура комплекса рецептор прогестерона-дезоксирибонуклеиновая кислота: новые взаимодействия, необходимые для связывания с элементами ответа на половину сайта». Молекулярная эндокринология. 20 (12): 3042–52. Дои:10.1210 / me.2005-0511. ЧВК 2532839. PMID 16931575.
- ^ PDB: 3L0L; Джин Л., Мартыновски Д., Чжэн С., Вада Т., Се В., Ли Ю. (май 2010 г.). «Структурная основа гидроксихолестеринов как природных лигандов орфанного ядерного рецептора RORgamma». Молекулярная эндокринология. 24 (5): 923–9. Дои:10.1210 / me.2009-0507. ЧВК 2870936. PMID 20203100.
- ^ а б Амуциас Г. Д., Пихлер Э., Миан Н., Де Грааф Д., Имсириду А., Робинсон-Рехави М., Борнберг-Бауэр Э., Робертсон Д. Л., Оливер С. Г. (июль 2007 г.). «Атлас взаимодействия белков для ядерных рецепторов: свойства и качество сети димеризации на основе концентраторов». BMC Системная биология. 1: 34. Дои:10.1186/1752-0509-1-34. ЧВК 1971058. PMID 17672894.
- ^ Линья М.Дж., Поркка К.П., Канг З., Савинайнен К.Дж., Янне О.А., Таммела Т.Л., Веселла Р.Л., Палвимо Дж.Дж., Висакорпи Т. (февраль 2004 г.). «Экспрессия корегуляторов рецепторов андрогенов при раке простаты». Клинические исследования рака. 10 (3): 1032–40. Дои:10.1158 / 1078-0432.CCR-0990-3. PMID 14871982. S2CID 8038717.
- ^ Klinge CM, Bodenner DL, Desai D, Niles RM, Traish AM (май 1997 г.). «Связывание ядерных рецепторов типа II и рецептора эстрогена с полными и половинными элементами ответа эстрогена in vitro». Исследования нуклеиновых кислот. 25 (10): 1903–12. Дои:10.1093 / nar / 25.10.1903. ЧВК 146682. PMID 9115356.
- ^ Glass CK, Розенфельд MG (январь 2000 г.). «Обмен корегулятора в транскрипционных функциях ядерных рецепторов». Гены и развитие. 14 (2): 121–41. Дои:10.1101 / gad.14.2.121 (неактивно 10.11.2020). PMID 10652267.CS1 maint: DOI неактивен по состоянию на ноябрь 2020 г. (связь)
- ^ Аранда А., Паскуаль А. (июль 2001 г.). «Рецепторы ядерных гормонов и экспрессия генов». Физиологические обзоры. 81 (3): 1269–304. Дои:10.1152 / Physrev.2001.81.3.1269. HDL:10261/79944. PMID 11427696. S2CID 5972234.
- ^ Копленд Дж. А., Шеффилд-Мур М., Колдзич-Живанович Н., Джентри С., Лампру Дж., Цорцату-Статопулу Ф., Зумпурлис В., Урбан Р. Дж., Влахопулос С. А. (июнь 2009 г.). «Рецепторы половых стероидов в дифференцировке скелета и эпителиальной неоплазии: возможно ли тканеспецифическое вмешательство?». BioEssays. 31 (6): 629–41. Дои:10.1002 / bies.200800138. PMID 19382224. S2CID 205469320.
- ^ Бжозовский А.М., Пайк А.С., Даутер З., Хаббард Р.Э., Бонн Т., Энгстрём О, Оман Л., Грин Г.Л., Густафссон Дж.А., Карлквист М. (октябрь 1997 г.). «Молекулярные основы агонизма и антагонизма в рецепторах эстрогенов». Природа. 389 (6652): 753–8. Bibcode:1997Натура.389..753Б. Дои:10.1038/39645. PMID 9338790. S2CID 4430999.
- ^ Шиау А.К., Барстад Д., Лориа П.М., Ченг Л., Кушнер П.Дж., Агард Д.А., Грин Г.Л. (декабрь 1998 г.). «Структурная основа распознавания рецептора эстрогена / коактиватора и антагонизм этого взаимодействия тамоксифеном». Клетка. 95 (7): 927–37. Дои:10.1016 / S0092-8674 (00) 81717-1. PMID 9875847. S2CID 10265320.
- ^ Гронемейер Х., Густафссон Я.А., Лауде В. (ноябрь 2004 г.). «Принципы модуляции надсемейства ядерных рецепторов». Обзоры природы. Открытие наркотиков. 3 (11): 950–64. Дои:10.1038 / nrd1551. PMID 15520817. S2CID 205475111.
- ^ Буш ББ, Стивенс В.К., Мартин Р., Ордентлих П., Чжоу С., Сапп Д.В., Хорлик Р.А., Мохан Р. (ноябрь 2004 г.). «Идентификация селективного обратного агониста орфанного ядерного рецептора эстроген-родственного рецептора альфа». Журнал медицинской химии. 47 (23): 5593–6. Дои:10.1021 / jm049334f. PMID 15509154.
- ^ Смит С.Л., О'Мэлли Б.В. (февраль 2004 г.). «Функция корегулятора: ключ к пониманию тканевой специфичности селективных модуляторов рецепторов». Эндокринные обзоры. 25 (1): 45–71. Дои:10.1210 / er.2003-0023. PMID 14769827.
- ^ Паскуаль Г., Гласс СК (октябрь 2006 г.). «Ядерные рецепторы против воспаления: механизмы трансрепрессии». Тенденции в эндокринологии и метаболизме. 17 (8): 321–7. Дои:10.1016 / j.tem.2006.08.005. PMID 16942889. S2CID 19612552.
- ^ Björnström L, Sjöberg M (июнь 2004 г.). «Зависимая от рецептора эстрогена активация AP-1 через негеномную передачу сигналов». Ядерный рецептор. 2 (1): 3. Дои:10.1186/1478-1336-2-3. ЧВК 434532. PMID 15196329.
- ^ Зивадинович Д., Гаметчу Б., Уотсон К.С. (2005). «Уровни мембранного рецептора-альфа эстрогена в клетках рака молочной железы MCF-7 позволяют прогнозировать реакцию на цАМФ и пролиферацию». Исследование рака груди. 7 (1): R101–12. Дои:10.1186 / bcr958. ЧВК 1064104. PMID 15642158.
- ^ Кустени С., Беллидо Т., Плоткин Л.И., О'Брайен К.А., Боденнер Д.Л., Хан Л., Хан К., ДиГрегорио Г.Б., Катценелленбоген Дж.А., Катценелленбоген Б.С., Роберсон П.К., Вайнштейн Р.С., Джилка Р.Л., Манолагас СК (март 2001 г.). «Негенотропная, неспецифическая для пола передача сигналов через рецепторы эстрогена или андрогена: диссоциация от транскрипционной активности». Клетка. 104 (5): 719–30. Дои:10.1016 / S0092-8674 (01) 00268-9. PMID 11257226. S2CID 10642274.
- ^ Стори Н.М., Джентиле С., Уллах Х., Руссо А., Мюссел М., Эркслебен С., Армстронг Д.Л. (март 2006 г.). «Быстрая передача сигналов на плазматической мембране ядерным рецептором гормона щитовидной железы». Труды Национальной академии наук Соединенных Штатов Америки. 103 (13): 5197–201. Bibcode:2006ПНАС..103.5197С. Дои:10.1073 / pnas.0600089103. ЧВК 1458817. PMID 16549781.
- ^ Стори Н.М., О'Брайан Дж. П., Армстронг Д. Л. (январь 2002 г.). «Rac и Rho опосредуют противоположную гормональную регуляцию калиевого канала, связанного с эфиром». Текущая биология. 12 (1): 27–33. Дои:10.1016 / S0960-9822 (01) 00625-X. PMID 11790300. S2CID 8608805.
- ^ а б Мартин Н.П., Маррон Фернандес де Веласко Е., Мизуно Ф., Скаппини Е.Л., Глянец В, Эркслебен С., Уильямс Дж. Г., Степлтон Х.М., Джентиле С., Армстронг Д.Л. (сентябрь 2014 г.). «Быстрый цитоплазматический механизм регуляции киназы PI3 ядерным рецептором тироидного гормона, TRβ, и генетические доказательства его роли в созревании синапсов гиппокампа мышей in vivo». Эндокринология. 155 (9): 3713–24. Дои:10.1210 / en.2013-2058. ЧВК 4138568. PMID 24932806.
- ^ Гилберт ME (январь 2004 г.). «Изменения в синаптической передаче и пластичности в области CA1 гиппокампа взрослых после гипотиреоза в процессе развития». Исследование мозга. Развитие мозга. 148 (1): 11–8. Дои:10.1016 / j.devbrainres.2003.09.018. PMID 14757514.
- ^ Moeller LC, Broecker-Preuss M (август 2011 г.). «Регуляция транскрипции неклассическим действием гормона щитовидной железы». Исследование щитовидной железы. 4 Приложение 1: S6. Дои:10.1186 / 1756-6614-4-S1-S6. ЧВК 3155112. PMID 21835053.
- ^ а б c d е ж грамм час я j k Каур С., Джоблинг С., Джонс К.С., Благородный Л.Р., Рутледж Е.Дж., Локьер А.Е. (7 апреля 2015 г.). «Ядерные рецепторы Biomphalaria glabrata и Lottia gigantea: значение для разработки новых модельных организмов». PLOS ONE. 10 (4): e0121259. Bibcode:2015PLoSO..1021259K. Дои:10.1371 / journal.pone.0121259. ЧВК 4388693. PMID 25849443.
- ^ Кроссгроув К., Лауде В., Майна CV (февраль 2002 г.). «Dirofilaria immitis кодирует Di-nhr-7, предполагаемый ортолог гена E78, регулируемого экдизоном дрозофилы». Молекулярная и биохимическая паразитология. 119 (2): 169–77. Дои:10.1016 / s0166-6851 (01) 00412-1. PMID 11814569.
- ^ "секс-1 (ген)". WormBase: информационный ресурс по нематодам.
- ^ Отте К., Кранц Х., Кобер И., Томпсон П., Хофер М., Хобольд Б., Реммель Б., Фосс Х., Кайзер К., Альберс М., Черуваллат З., Джексон Д., Казари Дж., Кёгл М., Пэабо С., Мус Дж., Кремосер С. , Deuschle U (февраль 2003 г.). «Идентификация бета-рецептора фарнезоида X как нового ядерного рецептора млекопитающих, воспринимающего ланостерол». Молекулярная и клеточная биология. 23 (3): 864–72. Дои:10.1128 / mcb.23.3.864-872.2003. ЧВК 140718. PMID 12529392.
- ^ "Отчет о генах FlyBase: DmelHr96". FlyBase. Получено 14 августа 2019.
- ^ а б Schwabe JW, Teichmann SA (январь 2004 г.). «Ядерные рецепторы: эволюция разнообразия». STKE науки. 2004 (217): pe4. Дои:10.1126 / stke.2172004pe4. PMID 14747695. S2CID 20835274.
- ^ Kruse SW, Suino-Powell K, Zhou XE, Kretschman JE, Reynolds R, Vonrhein C и др. (Сентябрь 2008 г.). «Идентификация орфанного ядерного рецептора COUP-TFII как рецептора, активируемого ретиноевой кислотой». PLOS Биология. 6 (9): e227. Дои:10.1371 / journal.pbio.0060227. ЧВК 2535662. PMID 18798693.
- ^ Марков Г.В., Гутьеррес-Мазариегос Дж., Питрат Д., Биллас И.М., Боннетон Ф., Морас Д. и др. (Март 2017 г.). «Происхождение древней пары гормон / рецептор, выявленное путем воскрешения предкового эстрогена». Достижения науки. 3 (3): e1601778. Bibcode:2017SciA .... 3E1778M. Дои:10.1126 / sciadv.1601778. ЧВК 5375646. PMID 28435861.
- ^ а б Халтурин К., Биллас И., Чебаро Ю., Райцель А.М., Таррант А.М., Лауде В., Марков Г.В. (ноябрь 2018 г.). «Рецепторы NR3E у книдарийцев: новое семейство родственников стероидных рецепторов расширяет возможные механизмы связывания лиганда». J Стероид Биохим Мол Биол. 184: 11–19. Дои:10.1016 / j.jsbmb.2018.06.014. ЧВК 6240368. PMID 29940311.
- ^ Ву В., Найлс Э.Г., Хираи Х., Ловерде П.Т. (февраль 2007 г.). «Развитие нового подсемейства ядерных рецепторов, члены которого содержат два ДНК-связывающих домена». BMC Эволюционная биология. 7: 27. Дои:10.1186/1471-2148-7-27. ЧВК 1810520. PMID 17319953.
- ^ Хуан В., Сюй Ф., Ли Дж., Ли Л., Цюэ Х, Чжан Г. (август 2015 г.). «Эволюция нового подсемейства ядерных рецепторов с акцентом на представителя тихоокеанской устрицы Crassostrea gigas». Ген. 567 (2): 164–72. Дои:10.1016 / j.gene.2015.04.082. PMID 25956376.
- ^ "nhr-1 (ген)". WormBase: информационный ресурс по нематодам.
- ^ Marxreiter S, Thummel CS (февраль 2018 г.). «Взрослые функции для ядерного рецептора Drosophila DHR78». Динамика развития. 247 (2): 315–322. Дои:10.1002 / dvdy.24608. ЧВК 5771960. PMID 29171103.
- ^ Эванс Р.М. (май 1988 г.). «Суперсемейство рецепторов стероидов и гормонов щитовидной железы». Наука. 240 (4854): 889–95. Bibcode:1988Научный ... 240..889E. Дои:10.1126 / science.3283939. ЧВК 6159881. PMID 3283939.
- ^ Мур Д.Д. (январь 1990 г.). «Разнообразие и единство рецепторов ядерных гормонов: надсемейство терпеноидных рецепторов». Новый биолог. 2 (1): 100–5. PMID 1964083.
- ^ Лауде В., Хэнни С., Колл Дж., Катцефлис Ф., Стелин Д. (март 1992 г.). «Эволюция надсемейства генов ядерных рецепторов». Журнал EMBO. 11 (3): 1003–13. Дои:10.1002 / j.1460-2075.1992.tb05139.x. ЧВК 556541. PMID 1312460.
- ^ Escriva H, Safi R, Hänni C, Langlois MC, Saumitou-Laprade P, Stehelin D, Capron A, Pierce R, Laudet V (июнь 1997 г.). «Связывание лиганда было приобретено в процессе эволюции ядерных рецепторов». Труды Национальной академии наук Соединенных Штатов Америки. 94 (13): 6803–8. Bibcode:1997PNAS ... 94.6803E. Дои:10.1073 / пнас.94.13.6803. ЧВК 21239. PMID 9192646.
- ^ а б c Escriva H, Delaunay F, Laudet V (август 2000 г.). «Связывание лиганда и эволюция ядерных рецепторов». BioEssays. 22 (8): 717–27. Дои:10.1002 / 1521-1878 (200008) 22: 8 <717 :: AID-BIES5> 3.0.CO; 2-I. PMID 10918302.
- ^ Бриджем Дж. Т., Эйк Г. Н., Ларру С., Дешпанде К., Хармс М. Дж., Готье М. Е., Ортлунд Е. А., Дегнан Б. М., Торнтон Дж. В. (октябрь 2010 г.). «Эволюция белка путем молекулярной обработки: диверсификация суперсемейства ядерных рецепторов от лиганд-зависимого предка». PLOS Биология. 8 (10): e1000497. Дои:10.1371 / journal.pbio.1000497. ЧВК 2950128. PMID 20957188.
- ^ а б Марков Г.В., Лауде В. (март 2011). «Происхождение и эволюция лиганд-связывающей способности ядерных рецепторов». Молекулярная и клеточная эндокринология. Эволюция рецепторов ядерных гормонов. 334 (1–2): 21–30. Дои:10.1016 / j.mce.2010.10.017. PMID 21055443. S2CID 33537979.
- ^ Торнтон Дж. У., Need E, Crews D (сентябрь 2003 г.). «Воскрешение рецептора предковых стероидов: древнее происхождение передачи сигналов эстрогена». Наука. 301 (5640): 1714–7. Bibcode:2003Научный ... 301.1714T. Дои:10.1126 / science.1086185. PMID 14500980. S2CID 37628350.
- ^ Тата-младший (июнь 2005 г.). «Сто лет гормонов». EMBO отчеты. 6 (6): 490–6. Дои:10.1038 / sj.embor.7400444. ЧВК 1369102. PMID 15940278.
внешняя ссылка
- Ядерные + рецепторы в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- Винсент Лауде (2006). "Компендиум IUPHAR по фармакологии и классификации надсемейства ядерных рецепторов 2006E". Справочник по ядерным рецепторам. Международный союз фундаментальной и клинической фармакологии. Получено 2008-02-21.
- "Ядерный рецептор онлайн-журнал ". Домашняя страница. опубликовано BioMed Central (больше не принимает заявки с мая 2007 г.). Получено 2008-02-21.
- «Ресурс ядерного рецептора». Джорджтаунский университет. Архивировано из оригинал на 2008-05-11. Получено 2008-02-21.
- «Атлас сигналов ядерных рецепторов (рецепторы, коактиваторы, корепрессоры и лиганды)». Консорциум NURSA. Получено 2008-02-21.
исследовательский консорциум и база данных, финансируемые NIH; включает журнал с открытым доступом, индексируемый PubMed, Сигнализация ядерного рецептора
- «Ресурс ядерного рецептора». Джек Ванден Хёвел. Получено 2009-09-21.