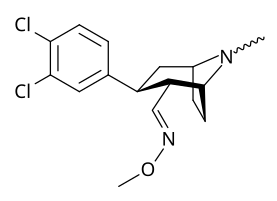
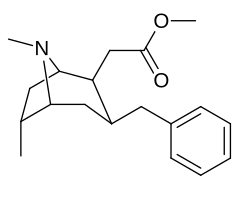
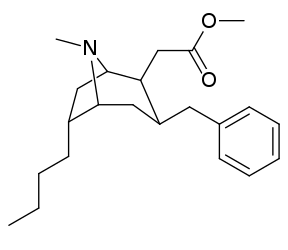
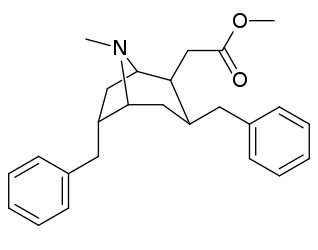
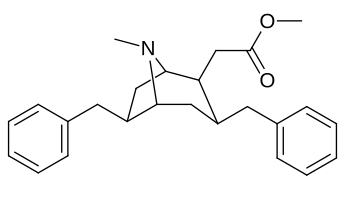
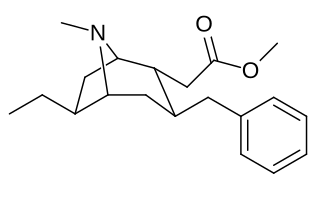
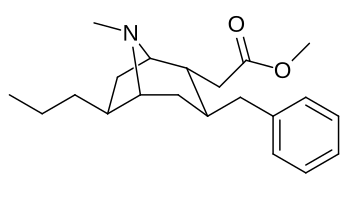
Список аналогов кокаина - List of cocaine analogues
2′ (6′) = орто, 3′ (5′) = мета & 4′ = параграф
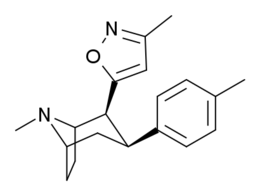
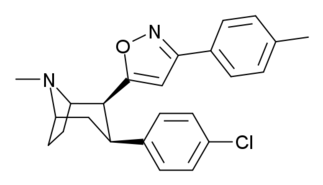
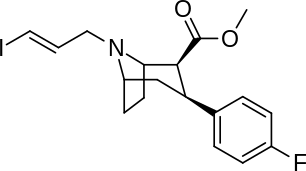
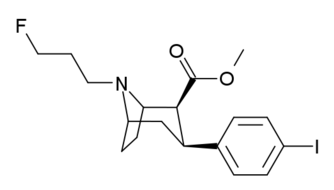
Это список кокаин аналоги. А аналог кокаина (обычно) искусственная конструкция романа химическое соединение из молекулярной структуры кокаина (часто являющейся отправной точкой природного), с полученным продуктом, достаточно похожим на кокаин, чтобы проявлять сходство, но изменение его химической функции. Среди аналогичных соединений, созданных из структуры кокаина, так называемые «аналоги кокаина» сохраняют 3β-бензоилокси или аналогичная функциональность (специально используемый термин обычно отличается от фенилтропаны, но в широком смысле, как категория, включает их) на тропановом скелете по сравнению с другими стимуляторами такого рода. Многие из полусинтетических аналогов кокаина правильный которые были изготовлены и изучены, состояли из девяти следующих классов соединений:[а]
- стереоизомеры кокаина
- 3βзамещенные фенильным кольцом аналоги
- 2β-замещенные аналоги
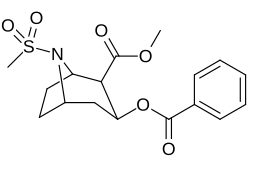
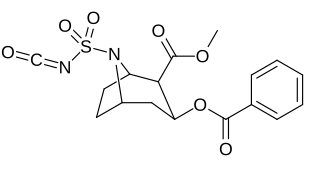
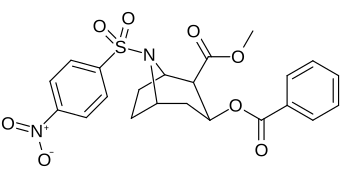
- N-модифицированные аналоги кокаина
- 3β-карбамоильные аналоги
- 3β-алкил-3-бензилтропаны
- 6/7-замещенные кокаины
- 6-алкил-3-бензилтропаны
- пиперидиновые гомологи кокаина

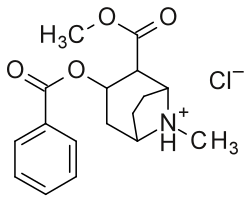
Ниже: альтернативная двумерная молекулярная диаграмма кокаина; показан конкретно как протонированный, NH +, гидрохлорид, и игнорируя трехмерную стереохимию
Однако строгие аналоги кокаина также будут включать такие другие потенциальные комбинации, как фенацилтропаны и другие углеродные разветвленные замены, не перечисленные выше. Этот термин может также свободно использоваться для обозначения наркотиков, изготовленных из кокаина или имеющих в своей основе полный синтез кокаина, но модифицированы, чтобы изменить их действие и QSAR. К ним относятся как анестетики-блокаторы внутриклеточных натриевых каналов, так и стимуляторы. ингибитор обратного захвата дофамина лиганды (например, определенные, а именно, отрезанные мостиком из тропана, пиперидины ). Кроме того, исследователи поддержали комбинаторные подходы к взятию наиболее многообещающих аналогов, выясненных в настоящее время, и их смешиванию с целью открытия новых и эффективных соединений для оптимизации их использования для различных конкретных целей.[b]

Хотя карбметокси обозначен в его функции как водородная связь на этом изображении, было обнаружено, что в первую очередь электростатические факторы доминируют над связыванием в этом пространстве площади молекулярной поверхности над действующим принципом водородной связи.[c]

Аналоги Sensu stricto
Стереоизомеры кокаина

| Стереоизомер | С. Сингха буквенно-цифровой назначение | IC50 (нМ ) [3ЧАС] WIN 3542 запрет на крыса полосатый мембраны Средняя стандартная ошибка ≤5% во всех случаях | ИЮПАК номенклатура |
|---|---|---|---|
| р-кокаин (Эритроксилин) | — | 102 | метил (1R, 2R, 3S, 5S) -3- (бензоилокси) -8-метил-8-азабицикло [3.2.1] октан-2-карбоксилат |
| р-псевдокаин (Делькаин, Депсокаин, Декстрокаин, Изококаин, Псикаин.[2]) | 172 | 15800 | метил (1R,2S, 3S, 5S) -3- (бензоилокси) -8-метил-8-азабицикло [3.2.1] октан-2-карбоксилат |
| р-аллококаин | 173 | 6160 | метил (1R, 2R,3R, 5S) -3- (бензоилокси) -8-метил-8-азабицикло [3.2.1] октан-2-карбоксилат |
| р-аллопсевдокаин | 174 | 28500 | метил (1R,2S,3R, 5S) -3- (бензоилокси) -8-метил-8-азабицикло [3.2.1] октан-2-карбоксилат |
| S-кокаин | 175 | 15800 | метил (1S, 3R, 4R, 5R) -3- (бензоил) окси-8-метил-8-азабицикло [3.2.1] октан-4-карбоксилат |
| S-псевдокаин | 176 | 22500 | метил (1S, 3R,4S, 5R) -3- (бензоил) окси-8-метил-8-азабицикло [3.2.1] октан-4-карбоксилат |
| S-аллококаин | 177 | 9820 | метил (1S,3S, 4R, 5R) -3- (бензоил) окси-8-метил-8-азабицикло [3.2.1] октан-4-карбоксилат |
| S-аллопсевдокаин | 178 | 67700 | метил (1S,3S,4S, 5R) -3- (бензоил) окси-8-метил-8-азабицикло [3.2.1] октан-4-карбоксилат |
Если 2D-диаграммы, приведенные для структурных аналогов ниже, не указывают на стереохимию, следует предположить, что они разделяют конформацию р-кокаин, если не указано иное.
Естественная изомерия кокаина нестабильна по нескольким причинам, помимо высокой степени лабильность; например: карбометокси C2 в своем конечном продукте биосинтеза поддерживает осевой положение, которое может пройти эпимеризация через омыление получить первое в экваториальный позиция.
Создание следующих аналогов кокаина традиционно требовало шага, который использовал 2-CMT как промежуточный молекулярный продукт.
Замены отщепления бензоильной ветви (исключая исчерпывающую фенильную группу)
| Салицилметилэкгонин[3] | Метильваниллилекгонин[4] |
 | 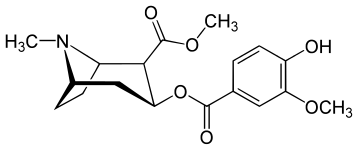 |
N.B. Перестановка фри продукт аспирина, используемый для изготовления сальбутамол. Однако здесь это имеет отношение к предшественнику, поскольку мигрированная ацетильная группа может быть предметом галоформная реакция. Более прямой путь к ванильная кислота хотя это просто окисление ванилин к функционализированному бензойная кислота.
Бензольное кольцо арена 2 ′, 3 ′, 4 ′ (5 ′ и 6 ′) позиции (арил ) замены
параграф-замещенные бензоилметилэкгонины



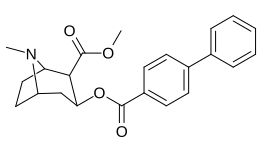
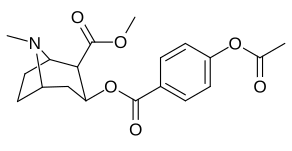
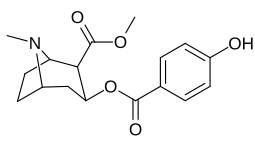
| Структура | С. Сингха буквенно-цифровой назначение (имя) | 4′=р | DAT [3H] WIN 35428 | 5-HTT [3H] Пароксетин | СЕТЬ [3H] Низоксетин | Селективность 5-HTT / DAT | Селективность NET / DAT |
|---|---|---|---|---|---|---|---|
| (кокаин) | ЧАС | 249 ± 37 | 615 ± 120 | 2500 ± 70 | 2.5 | 10.0 | |
| небензоилокси аналог сравнительные лиганды нетропановый аналог сравнительные лиганды | 11b (WIN 35428) (низоксетин) (флуоксетин) | F — — | 24 ± 4 775 ± 20 5200 ± 1270 | 690 ± 14 762 ± 90 15 ± 3 | 258 ± 40 135 ± 21 963 ± 158 | 28.7 1.0 0.003 | 10.7 0.2 0.2 |
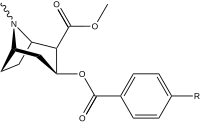 | |||||||
| 183a | я | 2522 ± 4 | 1052 ± 23 | 18458 ± 1073 | 0.4 | 7.3 | |
| 183b | Ph | 486 ± 63 | - | - | - | - | |
| 183c | OAc | 144 ± 2 | - | - | - | - | |
| 183d | ОЙ | 158 ± 8 | 3104 ± 148 | 601 ± 11 | 19.6 | 3.8 | |
| (4'-фторокаин )[5] | F | - | - | - | - | - | |
| (параграф-Изотиоцианатобензоилэкгонин метиловый эфир )[6] (п -Изокок) | NCS | - | - | - | - | - |
В МАТ карман для переплета аналогично липофильному месту на кокаиноподобных соединениях, включая бензольное кольцо, приблизительно равно 9 Å в длину. Что лишь немного больше, чем само по себе фенильное кольцо.[f]
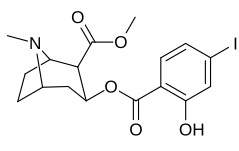
мета-замещенные бензоилметилэкгонины
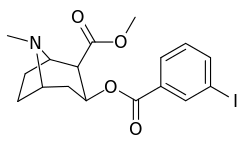


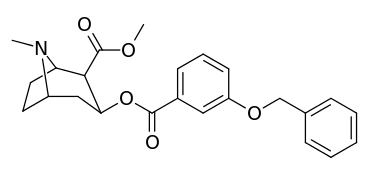
| Структура | С. Сингха буквенно-цифровой назначение (имя) | 3 ′ = R | DAT [3H] WIN 35428 | 5-HTT [3H] Пароксетин | СЕТЬ [3H] Низоксетин | Селективность 5-HTT / DAT | Селективность NET / DAT |
|---|---|---|---|---|---|---|---|
 | |||||||
| 184a | я | 325ɑ | - | - | - | - | |
| 184b | ОЙ | 1183 ± 115 | 793 ± 33 | 3760 ± 589 | 0.7 | 3.2 | |
| 191 | ОМлрд | - | - | - | - | - | |
| (м -Изокок) | NCS | - | - | - | - | - |
- ɑIC50 значение смещения [3H] кокаин
орто-замещенные бензоилметилэкгонины

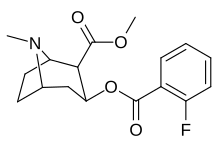
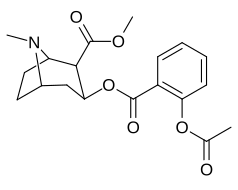

Гидроксилированный аналог 2'-ОН продемонстрировал десятикратное увеличение эффективности по сравнению с кокаином.[час]
| Структура | С. Сингха буквенно-цифровой назначение (имя) | 2 ′ = R | DAT [3H] WIN 35428 | 5-HTT [3H] Пароксетин | СЕТЬ [3H] Низоксетин | Селективность 5-HTT / DAT | Селективность NET / DAT |
|---|---|---|---|---|---|---|---|
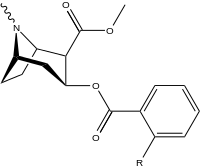 | |||||||
| 185a | я | 350ɑ | - | - | - | - | |
| 185b | F | 604 ± 67 | 1770 ± 309 | 1392 ± 173 | 2.9 | 2.3 | |
| 185c (2'-ацетоксикокаин )[7] | OAc | 70 ± 1 | 219 ± 20 | 72 ± 9 | 3.1 | 1.0 | |
| 185d (2'-гидроксикокаин )[3] | ОЙ | 25 ± 4 | 143 ± 21 | 48 ± 2 | 5.7 | 1.9 |
- ɑIC50 значение смещения [3H] кокаин
многообразные бензоилоксифенильные замещения

Множественные замены (замены замен; например, мета- & параграф- ) или многократно ("многократно") замещенные аналоги являются аналогами, в которых имеет место более одной модификации исходной молекулы (имеющей многочисленные промежуточные составляющие). Они создаются путем экстраполяции результатов взаимосвязи между структурой и деятельностью, которые часто удивляют. Это даже обычный случай, когда две отдельные замены могут каждая давать более слабое, более низкое сродство или даже полностью неэффективное соединение соответственно; но из-за открытий, которые часто при совместном использовании такие два взаимно неполноценных изменения, добавляемые в тандеме к одному аналогу, могут привести к тому, что полученное производное будет проявлять гораздо большую эффективность, сродство, селективность и / или силу, чем даже исходное соединение; что в противном случае было бы скомпрометировано любым из этих двух изменений, сделанных отдельно.
Для описания и ссылки на этот механизм обратите внимание на то, что опиоид оксикодон, полученный из кодеина, в 1,5-1,7 раза больше обезболивающего действия морфина (опиоид, по отношению к которому кодеин, по сравнению с ним, только на 8-12%, или 0,17 его сила у крыс); однако промежуточными продуктами оксикодона в его синтезе из кодеина являются: ⅓ эффективность кодеина (т.е. кодеинон); 0,13 морфина (т.е. 14-гидроксикодеин) у крыс и меньше у мышей (для иллюстрации: первый даже меньше 0,17 морфина, как у кодеина); с конечным возможным автономным промежуточным соединением между кодеином и оксикодоном (т.е. 7,8-дигидрокодеин) составляет от 150 до 200% от кодеина.[8]
| Структура | С. Сингха буквенно-цифровой назначение (имя) | орто-2′=р | мета-3′=р | параграф-4′=р | DAT [3H] WIN 35428 | 5-HTT [3H] Пароксетин | СЕТЬ [3H] Низоксетин | Селективность 5-HTT / DAT | Селективность NET / DAT |
|---|---|---|---|---|---|---|---|---|---|
 | 186 | HO | ЧАС | я | 215 ± 19 | 195 ± 10 | 1021 ± 75 | 0.9 | 4.7 |
 | (Ваниллилметилэкгонин )[4] | ЧАС | ОСН3 | ОЙ | - | - | - | - | - |
бензоил-фенил-модификации
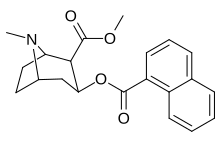
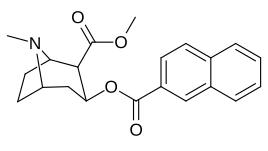
Аналоги нафталина допускают дальнейшие числовые замены, включая восемь позиций пери замещенные узоры. Еще много изменений, создающих различные ароматические кольца возможны.
| Структура | С. Сингха буквенно-цифровой назначение (имя) | C =р | DAT [3H] Кокаин (IC50) | 5-HTT [3H] Пароксетин | СЕТЬ [3H] Низоксетин | Селективность 5-HTT / DAT | Селективность NET / DAT |
|---|---|---|---|---|---|---|---|
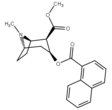 | 187 | 1-нафталин | 742 ± 48 | - | - | - | - |
 | 188 | 2-нафталин | 327 ± 63 | - | - | - | - |
Модификации бензоильной ветви

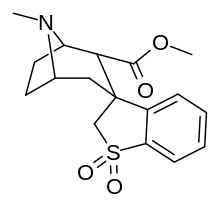
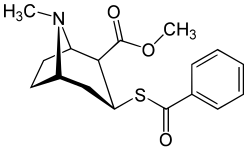
Сера вместо кислорода в простой связи бензоилового эфира приводит к более низкой электроотрицательности, чем у кокаина.
Водород с C1-тропановым кольцом - замещения

ср. гидрокситропакокаин для природного алкалоида (без карбметокси в положении 2), который является заместителем C1 с гидроксильная группа.
| Структура | Банальное имя | р (Фрагмент C1) | Kя (нМ) @ DAT | Kя (нМ) @ SERT | Kя (нМ) @ СЕТЬ | σ1 близость Kя | σ2 близость Kя | IC50 (мкМ) ингибирование Na + (Стимулированный вертридином приток натриевых каналов в нейронах неокортекса)c | LogP (Алгоритм XLogP3, Ченг и др., 2007) |
|---|---|---|---|---|---|---|---|---|---|
| (-)-Кокаин | ЧАС | 326 ± 106 | 513 ± 143 | 358 ± 69 | 6,7 ± 0,3 мкМd[13] | "существенный"[14] | 6.99 ± 2.43 | 2.30 | |
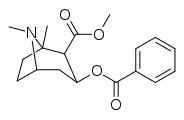 | (-) - 1-метил-кокаин | Мне | 163 ± 23 | 435 ± 77 | 488 ± 101 | "неоценимый" | 1,13 мкМ | 16.01 ± 1.90 | 2.67 |
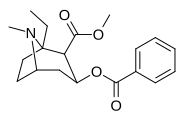 | (-) - 1-этил-кокаин | Et | 95.1 ± 17.0ɑ | 1,106 ± 112 | 598 ± 179 | — | — | — | 3.20 |
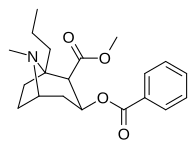 | (-) - 1-н-пропил-кокаин | п-Пр | 871 ± 205ɑ | 2,949 ± 462б | 796 ± 195 | — | — | — | 3.56 |
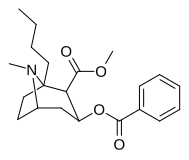 | (-) - 1-н-пентил-кокаин | п-C5ЧАС11 | 1,272 ± 199б | 1,866 ± 400ɑ | 1,596 ± 21б | — | — | — | 4.64 |
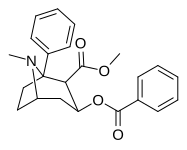 | (-) - 1-фенил-кокаин | Ph | 32.3 ± 5.7б | 974 ± 308 | 1,980 ± 99б | 524 нМ | 198 нМ | 0.29 ± 0.07 | 3.77 |
- ɑ, п <0,05 по сравнению с (-) - кокаином (односторонний ANOVA с последующим тестом множественных сравнений Даннета)
- б, п <0,01 по сравнению с (-) - кокаином (односторонний ANOVA с последующим тестом множественных сравнений Даннета)
- cБыло обнаружено, что лидокаин имеет значение 39,6 ± 2,4, самое слабое из всех протестированных.
- dВ той же ссылке указано 25,9 ± 2,4 мкМ для (+) - кокаина и 13,6 ± 1,3 мкМ для норкокаина. Для сравнения он дает 12,7 ± 1,5 мкМ для сигмаергического сродства (+) - амфетамина. Другая ссылка дает 1,7-6,7 мкМ для (-) - кокаина. Все ценности Kя.[15]
- Используя тот же набор данных, что и в таблице выше, было обнаружено, что следующие соединения сравниваются как:
- ЦФТ @ DAT = 39,2 ± 7,1 (n = 5)
- флуоксетин @ SERT = 27,3 ± 9,2 (n = 3)
- дезипрамин @ NET = 2,74 ± 0,59 (n = 3)
Аналоги кокаина, замещающие положение C1-тропанового кольца, требующие сульфинимина (N-сульфинилимин) химии (до изобретения которой были несостоятельны), которые связываются в отличие от типичной конфигурации в DAT (открытые для выхода) как кокаин (с его конечным расстоянием D79-Y156 6,03 Å) или в атипичных (близких к out) конформация бензтропинов (3,29 Å). Хотя они ближе к открытому к наружному: (-) - 1-метил-кокаин = 4,40 Å и (-) - 1-фенил-кокаин = 4,89 Å и демонстрируют предпочтительное взаимодействие с обращенной наружу конформацией DAT, они, по-видимому, не имеют поведенческой стимуляции как закрытого типа. Несмотря на нестимулирующие поведенческие профили, у них все же есть антидепрессивные поведенческие профили.[12]
С1-фенильный аналог в десять раз сильнее кокаина в качестве лиганда обратного захвата дофамина и в двадцать четыре раза сильнее в качестве местного анестетика (потенциал-зависимый блокатор Na + -каналов), тогда как метильный аналог C1 в 2,3 раза менее эффективен в качестве местного анестетика.[12]
2β-замены (включая переэтерификацию метаболита замещения кокаэтиленом)

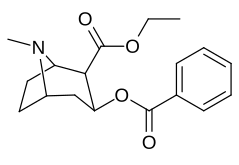


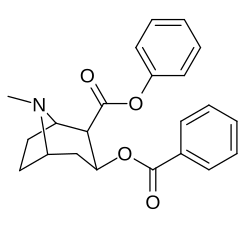

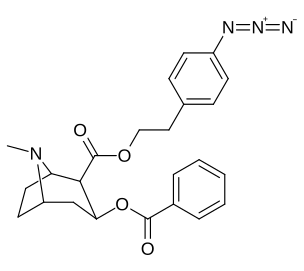
Учет того, что большие и громоздкие заместители C2 будут изменять тропан, искажая пиперидиновую кольцевую часть его скелета в достаточной степени, чтобы ухудшить его функциональность, или что в указанном случае это будет препятствовать связыванию, в частности на 8-аза-конце, чтобы ослабить стерическое напряжение идя к своему месту из положения 2,[l] кажутся во многих случаях необоснованными.[м] (примеры приведены в таблице изображений ниже)
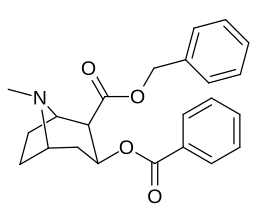 | 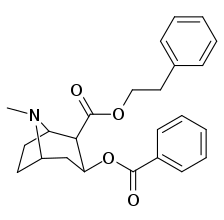 | 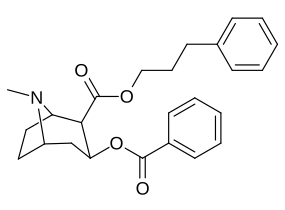 |  |

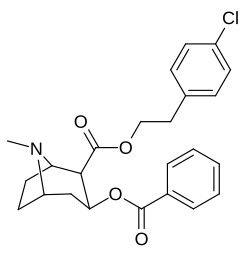
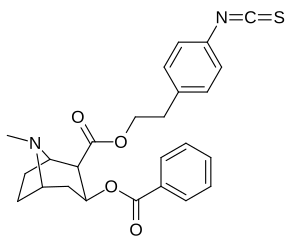
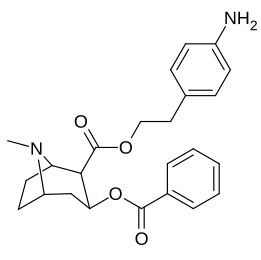 |  |  |  |

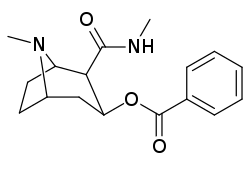


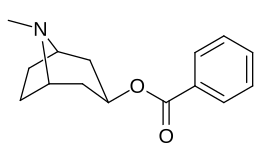
Сложный 197b продемонстрировал увеличенную в 1131 раз селективность по аффинности по сравнению с переносчиком серотонина при лишь незначительном снижении активности переносчиков дофамина и норэпинефрина.[n] В то время как 197c увеличилось в 469 раз на SERT, с большей близостью к DAT чем кокаин и был приблизительно равным СЕТЬ.[o] 197b было 137 ×, а 196c В 27 раз менее эффективно связывается с переносчиком серотонина, но оба имеют отношение NET / DAT, что обеспечивает лучшее дофаминергический чем кокаин.[п]



| Структура | С. Сингха буквенно-цифровой назначение (имя) | р | DAT [3H] WIN 35428 | 5-HTT [3H] Пароксетин | СЕТЬ [3H] Низоксетин | Селективность 5-HTT / DAT | Селективность NET / DAT |
|---|---|---|---|---|---|---|---|
 | |||||||
| (Кокаин) | Мне | 89 ± 4.8 | 1045 ± 89 | 3298 ± 293 | 11.7 | 37.0 | |
| 196a (Кокаэтилен ) | Et | 195 ± 45 | 5801 ± 493 | 10000 ± 751 | 29.7 | 51.3 | |
| 196b | п-Пр | 196 ± 46 | 4517 ± 430 | 6124 ± 262 | 23.3 | 31.2 | |
| 196c | я-Пр | 219 ± 48 | 25224 ± 1498 | 30384 ± 1685 | 115 | 139 | |
| 196d | Ph | 112 ± 31 | 33666 ± 3330 | 31024 ± 1909 | 300 | 277 | |
| 196e | Млрд | 257 ± 14 | 302 ± 23 | 20794 ± 950 | 1.2 | 80.9 | |
| 196f | β-фенэтил | 181 ± 10 | 615 ± 52 | 19944 ± 1026 | 3.4 | 110 | |
| 196 г | γ-фенилпропил | 147 ± 19 | 374 ± 15 | 4893 ± 344 | 2.5 | 33.3 | |
| 196ч | циннамил | 371 ± 15 | 368 ± 6.3 | 68931 ± 3476 | 1.0 | 186 | |
| 196i | п-НЕТ2-β-фенэтил | 601 ± 28 | - | - | - | - | |
| 196j | п-Cl-β-фенэтил | 271 ± 12 | - | - | - | - | |
| 196 тыс. | п-NH2-β-фенэтил | 72 ± 7 | - | - | - | - | |
| 196л | п-NCS -β-фенэтил | 196 ± 14 | - | - | - | - | |
| 196 кв.м. | п-азидо -β-фенэтил | 227 ± 19 | - | - | - | - | |
| 196н | (п-NHCOCH2Br) β-фенэтил | 61 ± 6 | - | - | - | - | |
| 196o | (п-NHCO (CH2)2CO2Et) β-фенэтил | 86 ± 4 | - | - | - | - | |
 | 197a | NH2 | 753 ± 41.3 | 13725 ± 1256 | 3981 ± 229 | 18.2 | 5.3 |
| 197b | -NMe2 | 127 ± 6.36 | 143713 ± 8854 | 7329 ± 158 | 1131 | 57.7 | |
| 197c | -N (OMe) мне | 60 ± 6.4 | 28162 ± 2565 | 3935 ± 266 | 469 | 65.6 | |
| 197d | -NHMe | 2424 ± 118 | 44798 ± 2105 | 4213 ± 206 | 18.5 | 1.7 | |
| 197e (Бензоилэкгонин ) | -ОЙ | 195000 | - | - | - | - | |
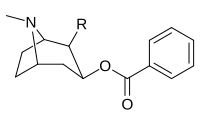 | 197f | HOCH2- | 561 ± 149 | - | - | - | - |
| 197 г (Тропакокаин ) | ЧАС | 5180 ± 1160 | - | - | - | - |
Bioisostere 2-позиционные функциональные замены карбметоксиэфира


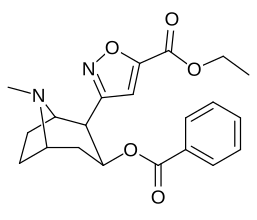


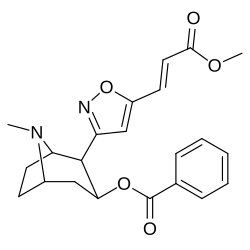
Бензоилэкгонин, т.е. сложный 197e(отличается от своего кокаинового родителя только деметилированием C2-карбметокси до карбокси) имеет крайнюю потерю активности (его приблизительное сродство составляет 195000 нМ), как показано in vitro методики определения эффективности связывания (где BBB проникновение не имеет никакого отношения к делу, как in vivo исследований) и предполагается, что это возможно из-за цвиттерион формирование.[р]
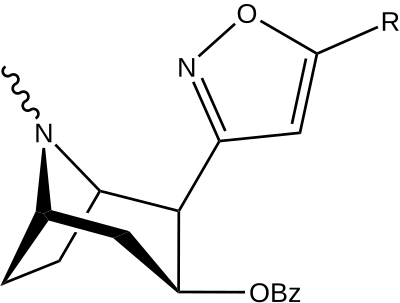
| Структура | С. Сингха буквенно-цифровой назначение (имя) | р | [3ЧАС]Мазиндол | [3H] DA | Селективность Поглощение / связывание |
|---|---|---|---|---|---|
| (Кокаин) | (ЧАС) | 580 ± 70 | 570 ± 180 | 1.0 | |
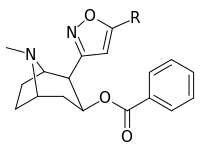 | |||||
| 198a | ЧАС | 520 ± 40 | 260 ± 70 | 0.5 | |
| 198b | CO2Et (5'-карбоэтокси-) | 120 ± 10 | 290 ± 40 | 2.4 | |
| 198c | BOC | 2230 ± 220 | 1820 ± 810 | 0.8 | |
| 198d | Ph | 2000 ± 640 | 2920 ± 1620 | 1.5 | |
| 198e | CH = CHCO2Мне | 3600 ± 400 | 3590 ± 1180 | 1.0 |




| Структура | С. Сингха буквенно-цифровой назначение | р | [3H] Мазиндол | [3H] DA | Селективность Поглощение / связывание |
|---|---|---|---|---|---|
| 199a | β (или р) CO2Et | 710 ± 150 | 1060 ± 340 | 1.5 | |
| 199b | α (или S) CO2Et | 5830 ± 630 | 8460 ± 620 | 1.4 |


| Структура | С. Сингха буквенно-цифровой назначение | р | [3H] Мазиндол | [3H] DA | Селективность Поглощение / связывание |
|---|---|---|---|---|---|
| 200 | 880 ± 350 | 400 ± 140 | 0.4 |
Vinylogous 2βфункциональные замены карбметоксиэфира





201b & 201c показать значительно повышенную эффективность по сравнению с кокаином; в то время как 201a, 201d & 201e значительно меньше. Это предполагает наличие акцептора водородной связи на 2β положение не обязательно иметь исключительное значение в создании аналогов кокаина с более высоким связыванием.

| Структура | С. Сингха буквенно-цифровой назначение | р | [3H] Мазиндол | [3H] DA | Селективность Поглощение / связывание |
|---|---|---|---|---|---|
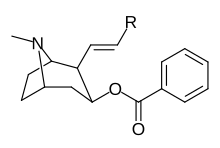 | |||||
| 201a | ЧАС | 1730 ± 550 | 1120 ± 390 | 0.6 | |
| 201b | Cl | 222 ± 49 | 368 ± 190 | 1.6 | |
| 201c | CO2Et | 50 ± 10 | 130 ± 10 | 2.6 | |
| 201d | CH = CHCO2Et | 1220 ± 100 | 870 ± 50 | 0.7 | |
| 201e | PO (OEt)2 | 4850 ± 470 | 5500 ± 70 | 1.1 |
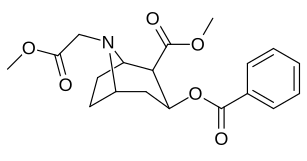
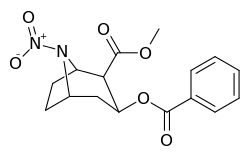
N-модификации






|




| Сложный | С. Сингха буквенно-цифровой назначение (имя) | N8-р | [3H] Мазиндол привязка | [3H] DA поглощение | Селективность Поглощение / связывание |
|---|---|---|---|---|---|
 | 217 (Метиодид кокаина) | - | 10700 ± 1530ɑ | - | - |
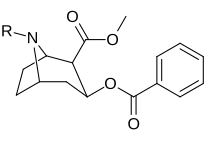 | (Кокаин) | CH3 | 280 ± 60 102ɑ | 320 ± 10 | 1.1 |
| 218 (Норкокаин ) | ЧАС | 303 ± 59ɑ | - | - | |
| 219a | Млрд | 668 ± 67ɑ | - | - | |
| 219b | Ac | 3370 ± 1080ɑ | - | - | |
| 219c | CH2CH2ОЙ | 700 ± 100 | 1600 ± 200 | 2.3 | |
| 219d | CH2CO2CH3 | 480 ± 40 | 1600 ± 100 | 3.3 | |
| 219e | CH2CO2ЧАС | 380 ± 20 | 2100 ± 400 | 5.5 | |
| 220а | ТАК2CH3 (РС ) | 1290 ± 80 | 1970 ± 70 | 1.5 | |
| 220b | ТАК2CF3 (Tf ) | 330 ± 30 | 760 ± 20 | 2.3 | |
| 220c | ТАК2Унтер-офицер | 120 ± 10 | 160 ± 10 | 1.3 | |
| 220d | ТАК2Ph | 20800 ± 3500 | 61000 | 2.9 | |
| 220e | ТАК2C6ЧАС4-4-НЕТ2 (носил ) | 5720 ± 1140 | 18800 ± 90 | 3.3 | |
| 220f | ТАК2C6ЧАС4-4-ОЧ3 | 6820 ± 580 | 16400 ± 1400 | 2.4 | |
| 221a | НЕТ | 99500 ± 12300 | 231700 ± 39500 | 2.3 | |
| 221b | НЕТ2 | 7500 ± 900 | 21200 ± 600 | 2.8 | |
| 221c | NHCOCH3 | >1000000 | >1000000 | - | |
| 221d | NH2 | - | - | - |
- ɑIC50 (нМ) для перемещения [3H] WIN 35428
Мостовой (N-связанные / связанные) аналоги кокаина, конденсированные с тропаном
Тропановый мост от 8 до 2 позиций

Видеть N-мостиковые фенилтропаны спереди и сзади.
| Сложный | С. Сингха буквенно-цифровой назначение | р | [3H] Мазиндол | [3H] DA | Селективность Поглощение / связывание |
|---|---|---|---|---|---|
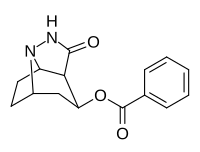 | 222 | 44900 ± 6200 | 115000 ± 15700 | 2.6 |
Аналоги кокаина с обратным мостиковым мостиком считаются более близкими к непривязанным аналогам кокаина и производным фенилтропана (где азот одинокая пара не фиксирована или ограничена ) и лучше имитирует их сходство. Это связано с тем, что когда восьмая позиция углеродного тропана свободно вращается и не связана, она предпочтительно занимает осевой положение как определяющее его наименьшее энергетическое и наиболее беспрепятственное состояние. В аналогах с передним мостом жесткая фиксация неподеленных азотных пар заставляет их находиться в экваториальный размещение для пиперидиновой кольцевой части тропанового ядра, указывая на мостик с двумя углеродными и тремя метиленовыми звеньями; отдавая засвидетельствованным передним мостом аналогам кокаина предпочтение SERT перед DAT.[y]
Аналоги трициклического кокаина
Привязка азота 8 к тропану на одну позицию дальше (за 2β и перекрестил его / оставив его открытым в виде водорода и, таким образом, возможного наличия дополнительных неограниченных замещений там) и полностью связав его с 3β арил, заменяющий его; дает обширную структуру с передним мостом для создания структурно трициклический серия аналогов кокаина.
С 8 по 3 позицию


1-й состав (ди-хлор бензол, 2β-CH2OCOMe) SERT = 1,6, DAT = 1870, NET = 638
2-я структура (параграф-bromo, мета-хлор, 2β-CO2Me) SERT = 2.3, DAT = 5420, NET = 459
3-я структура (параграф-iodo, мета-хлор, 2β-CH2OCOPh) SERT = 0,06, DAT / NET оба => 10K
| Сложный | Икс | Y | р | SERT Kя (нМ) | DAT Kя (нМ) | СЕТЬ Kя (нМ) |
| 1 | Cl | Cl | CH2OCOMe | 1.6 | 1870 | 638 |
| 2 | Br | Cl | CO2Мне | 2.3 | 5420 | 459 |
| 3 | я | Cl | CH2ОКОФ | 0.06 | > 10 тыс. | > 10 тыс. |
Азаборнане сужение кольца тропана
Были внесены изменения, укорачивающие систему тропановых колец с включением длины бензоилокси в C3, в отличие от азаборнан фенилтропаны;[17] вероятно исправление неглубокого проникновения (для хорошей эффективности) последнего.
5-бензоат (слева внизу) и 6-бензоат (справа, внизу)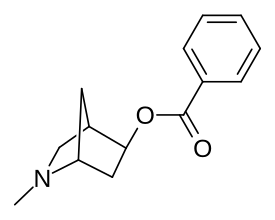


Сравнение тропанового кольца и норборнана в верхнем слое, с контрастом бензоильной ветви в его конфигурации, в том, как оно выходит из тела любого основного типа кольца (показано дважды разными цветами для наглядности выше)
6/7 тропановое положение метоксикокаин и аналоги метоксипсевдокаина
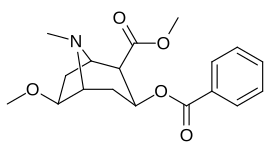
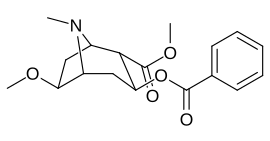
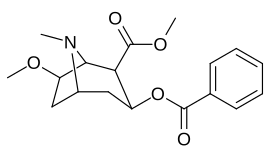
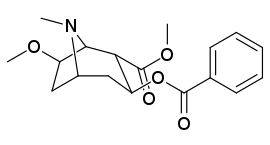


| Сложный | С. Сингха буквенно-цифровой назначение (имя) | Икс | Kя (нМ) [3H] Мазиндольное связывание | Kя (нМ) [3H] Поглощение DA | Селективность Поглощение / связывание |
|---|---|---|---|---|---|
| (Кокаин) | 280 ± 60 | 320 ± 10 | 1.1 | ||
| (Псевдокаин) | 10400 ± 300 | 13800 ± 1500 | 1.3 | ||
| 225a | 2β, 6β-ОСН3 | 98000 ± 12000 | 68000 ± 5000 | 0.7 | |
| 225b | 2α, 6β-ОСН3 | 190000 ± 11000 | 510000 ± 110000 | 2.7 | |
| 225c | 2β, 7β-ОСН3 | 4200 ± 100 | 6100 ± 200 | 1.4 | |
| 225d | 2α, 7β-ОСН3 | 45000 ± 5000 | 110000 ± 4000 | 2.4 | |
| 225e | 2α, 7α-ОСН3 | 54000 ± 3000 | 200000 ± 70000 | 3.7 |
3β-положение 2 ′ - (6 ′) и 2β-замещения комбинации аналогов







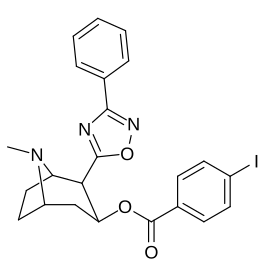
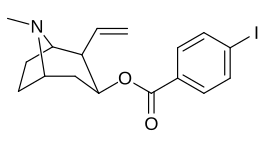

| Сложный | С. Сингха буквенно-цифровой назначение | 2β-р | C2′-р | IC50 (нМ) (смещение [3H] WIN 35428) |
|---|---|---|---|---|
 | ||||
| 211a | CO2ОЙ | ЧАС | 6214 ± 1269 | |
| 211b | CH2OCOCH3 | ЧАС | 2995 ± 223 | |
| 211c | КОНХЧ3 | ЧАС | >100000 | |
| 211d | CO2Et | ЧАС | 2031 ± 190 | |
| 211e | CO2-я-Пр | ЧАС | 1377 ± 10 | |
| 211f | CO2Ph | ЧАС | 2019 ± 253 | |
| 211 г | CO2CH2Ph | ЧАС | 4602 ± 325 | |
| 211ч | 3-фенил-1,2,4-оксадиазол | ЧАС | 3459 ± 60 | |
| 211i | CH = CH2 | ЧАС | 2165 ± 253 | |
| 211j | CH2CH3 | ЧАС | 2692 ± 486 | |
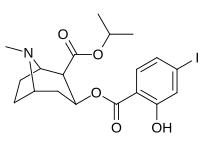 | 212 | CO2-я-Пр | HO | 663 ± 70 4507 ± 13ɑ 34838 ± 796б |
- ɑДля вытеснения [3H] пароксетин (5-HTT и NET)
- бДля вытеснения [3H] низоксетин (5-HTT и NET)
3β-Карбамоиловые аналоги

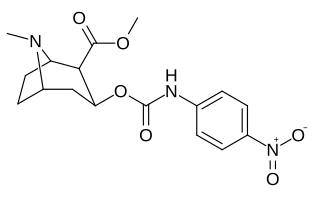

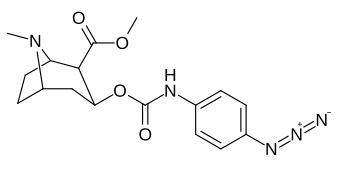

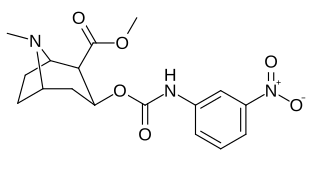
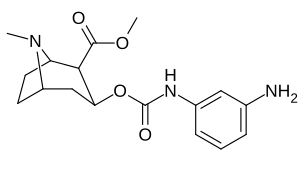


| Сложный | С. Сингха буквенно-цифровой назначение (имя) | Икс | IC50 (нМ) подавление [3H] Связывание кокаина (Полосатая ткань крысы) | IC50 (нМ) подавление [3H] Поглощение DA (Полосатая ткань крысы) | Селективность поглощение / связывание |
|---|---|---|---|---|---|
| (Кокаин) | (ЧАС) | 70 ± 10 | 210 ± 70 | 3.0 | |
 | |||||
| 223a | ЧАС | 5600 ± 700 | 52600 ± 3000 | 9.4 | |
| 223b | 4-НЕТ2 | 1090 ± 250 | 5700 ± 1200 | 5.2 | |
| 223c | 4-NH2 | 63300 ± 12200 | >100000 | - | |
| 223d | 4-Н3 | 1000 ± 240 | 1180 ± 360 | 1.2 | |
| 223e | 4-NCS | 260 ± 60 | 490 ± 80 | 1.9 | |
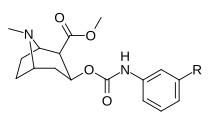 | |||||
| 223f | 3-НЕТ2 | 37 ± 10 | 178 ± 23 | 4.8 | |
| 223 г | 3-NH2 | 2070 ± 340 | 23100 ± 900 | 11.1 | |
| 223ч | 3-Н3 | 630 ± 150 | 3900 ± 1590 | 6.2 | |
| 223i | 3-NCS | 960 ± 210 | 4900 ± 420 | 5.1 |
Замены фенильной связи в 3-м положении
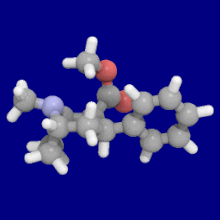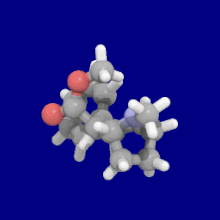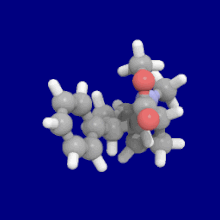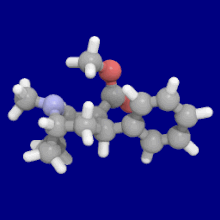
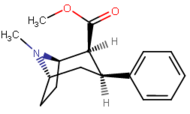

Видеть: Список фенилтропанов (Многие фенилтропаны получают из метаболитов кокаина, таких как метилэкгонидин, так как предшественники. В то время как полностью синтетические методы были разработаны из исходного материала винилкарбеноидов и пирролов.)[22]
Разница в длине бензоилокси и фенильной связи, в отличие от кокаина и фенилтропана, приводит к более короткому расстоянию между центроид ароматического бензола и связующего азота тропана в последних ПТ. Это расстояние по шкале 5,6 Å для фенилтропанов и 7,7 Å для кокаина или аналогов с интактным бензоилокси.[ac] Это может объяснить повышенный профиль поведенческой стимуляции PT по сравнению с кокаином.[объявление] Различия в связывающей способности также объяснялись с учетом сольватационных эффектов; кокаин, содержащий 2β,3β-эфирные группы считаются более сольватированными, чем соединения типа WIN (например, тропарил). Высшее pKɑс азотом тропана (8,65 для кокаина, 9,55 для тропарила и 11,95 для винилового аналога 43а), пониженная водная сольватация и пониженная конформационная гибкость добавлены к увеличению сродства связывания.[ae]
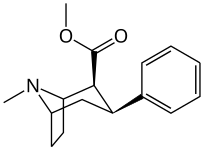
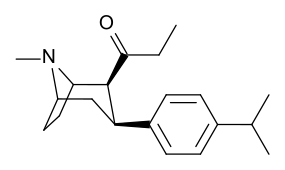
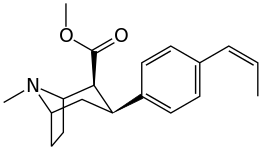
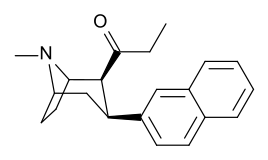
Несмотря на наблюдаемое усиление стимуляции, у фенилтропанов отсутствует местный анестезирующий эффект блокирования натриевых каналов, который бензоилокси придает кокаину. Помимо местного воздействия, это придает кокаину сродство к связыванию с сайтами на натрийзависимых транспортных участках допамина и серотонина, которые отличаются и специфичны для MAT в отличие от общих натриевых каналов; создание отдельного механизма реляционной аффинности к переносчикам в дополнение к его ингибированию обратного захвата для этих переносчиков; это уникально для местного анестетика в кокаине и его аналогах с аналогичным заменителем бензоилокси, который оставляет нетронутой способность блокировать натриевые каналы. Преодоление таких соединений функционально по отношению к МАТ по сравнению с аналогами фенилтропана, у которых удален мостик местного анестетика.[23] (Требуется перекачка части ионов натрия из аксона через Na + / K + -АТФаза ). Кроме того, было даже постулировано, что решающая роль в отношении энергии электронов, передаваемых через сенсибилизацию напряжением (и, следовательно, потенциал действия блокировка молекулой, способной пересекать свой конкретный канал, в случае кокаина a натриевой канал, который потенциально служит в повторная количественная оценка его заряда) на сайте связывания рецептора может ослабить опосредующее влияние ингибирующей регуляции, которую играют ауторецепторы, замедляя высвобождение нейромедиатора, когда отток создается в результате агонизма соединения; позволяя этому оттоку продолжаться без попытки организма поддерживать гомеостаз разыгрывая столь же легко реагирующую манеру на его конформационные изменения.[24]
|
3β-Алкилфенилтропан и 3β-Алкенильные аналоги
Состав 224e, 3βаналог -стирола, имел самую высокую эффективность в своей группе. Пока 224b & 224c проявили наибольшую избирательность, при этом 224b обладает в десять раз большей эффективностью в отношении переносчика дофамина, чем кокаин.[аф]
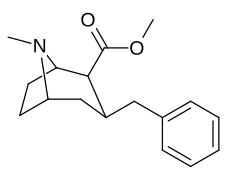



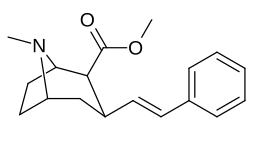

(т.е. сложный "224e")
| Сложный | С. Сингха буквенно-цифровой назначение (имя) | п | IC50 (нМ) [3H] Связывание кокаина | IC50 (нМ) [3H] Поглощение DA | Селективность поглощение / связывание |
|---|---|---|---|---|---|
| (Кокаин) | 101 ± 26 | 209 ± 20 | 2.1 | ||
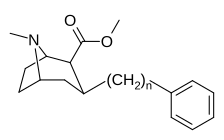 | |||||
| 224a | 1 | 885 ± 18 | 1020 ± 52 | 1.1 | |
| 224b | 2 | 9.9 ± 0.33 | 70.5 ± 1.0 | 7.1 | |
| 224c | 3 | 344 ± 12 | 2680 ± 190 | 7.8 | |
| 224d | 71.6 ± 0.7 | 138 ± 9 | 1.9 | ||
| 224e | 2.10 ± 0.04 | 5.88 ± 0.09 | 2.8 |
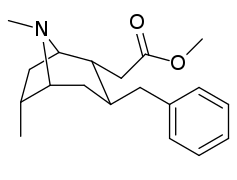
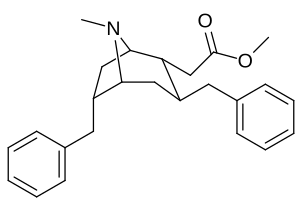
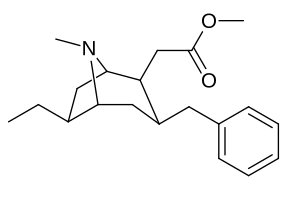
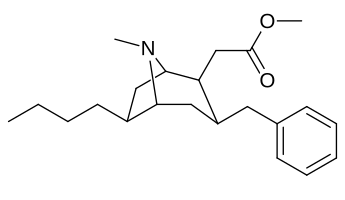
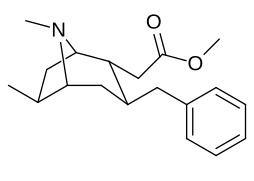
6-Алкил-3-бензилтропановые аналоги



|
|
|
|
| Сложный | С. Сингха буквенно-цифровой назначение (имя/ПОБЕДИТЬ номер) | р | Kя (нМ) [3H] WIN 35428 привязка | IC50 (нМ) [3H] Поглощение DA | Селективность поглощение / связывание |
|---|---|---|---|---|---|
| (Кокаин) | 32 ± 5 338 ± 221 | 405 ± 91 405 ± 91 | 12.6 1.2 | ||
| 11а (WIN 35065-2) | 33 ± 17 314 ± 222 | 373 ± 10 | 11.3 | ||
| (-) - 229a | ЧАС | 33 ± 5 | 161 ± 100 | 4.9 | |
| 229a | ЧАС | 91 ± 10 | 94 ± 26 | 1.0 | |
| 229b | Мне | 211 ± 23 | - | - | |
| 229c | Et | 307 ± 28 | - | - | |
| 229d | п-Пр | 4180 ± 418 | - | - | |
| 229e | п-Bu | 8580 ± 249 | - | - | |
| 229f | Млрд | 3080 ± 277 | - | - | |
| (+) - 230а | ЧАС | 60 ± 6 | 208 ± 63 | 3.5 | |
| 230а | ЧАС | 108 ± 14 | 457 ± 104 | 4.2 | |
| 230b | Мне | 561 ± 64 | - | - | |
| 230c | Et | 1150 ± 135 | - | - | |
| 230d | п-Пр | 7240 ± 376 | - | - | |
| 230e | п-Bu | 19700 ± 350 | - | - | |
| 230f | Млрд | 7590 ± 53 | - | - | |
| 231b | Мне | 57 ± 5 | 107 ± 36 | 1.9 | |
| 231c | Et | 3110 ± 187 | - | - | |
| 231d | п-Пр | 5850 ± 702 | - | - | |
| 231f | Млрд | 1560 ± 63 | - | - | |
| 232b | Мне | 294 ± 29 | 532 ± 136 | 1.8 | |
| 232c | Et | 6210 ± 435 | - | - | |
| 232d | п-Пр | 57300 ± 3440 | - | - | |
| 232f | Млрд | 3080 ± 277 | - | - | |
| 241 | Млрд | 4830 ± 434 | - | - |
| Подкатегория (Подворье С. Сингха №) | а р= H | б р= Я | c р= Et | d р=п-Пр | е р=п-Bu | ж р= Bn |
|---|---|---|---|---|---|---|
| 6α-изомеры: 237a-f | ||||||
 |  | 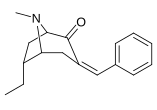 | 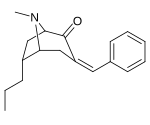 | 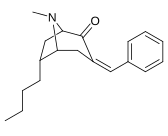 | 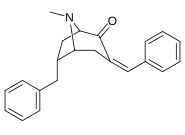 | |
| 6β-изомеры (экзо): 238a-f | ||||||
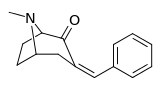 |  |  | 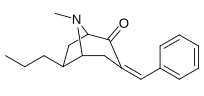 |  |
| |
| 3β-бензильные производные: 239a-f | ||||||
 | 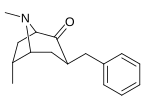 | 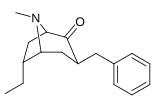 | 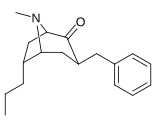 |  | 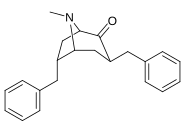 | |
| средний сложные эфиры алкилидена: 240a — f | ||||||
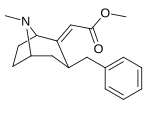 |  |  | 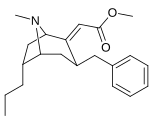 | 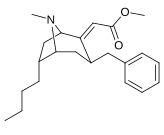 |  |
N.B. который 237a и 238a представляют собой одно и то же соединение, поскольку оба являются родительскими для любой серии с насыщенным водородом в соответствующем месте замещения.
Прямой 2,3-пиримидино плавленый

ниже: Халькостробамин

ср. стробамин (справа) для более эффективного соединения, как показано ниже.
| Структура | буквенно-цифровой назначение | р1 | р2 | hDAT IC50 (нМ) | hSERT IC50 (нМ) | hNET IC50 (нМ) |
|---|---|---|---|---|---|---|
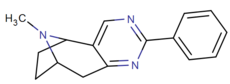 | ||||||
| (-) - 3а | ЧАС | C6ЧАС5 | 58,300 (20,200) | 6140 (3350) | NA | |
| (+) - 3а | ЧАС | C6ЧАС5 | 48,700 (20,100) | 6030 (3400) | NA | |
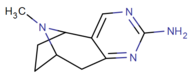 | ||||||
| (-) - 3b | ЧАС | NH2 | NA | NA | NA | |
| (+) - 3b | ЧАС | NH2 | NA | NA | NA | |
 | ||||||
| (-) - 3c | ЧАС | CH3 | NA | NA | NA | |
| (+) - 3c | ЧАС | CH3 | NA | NA | NA | |
 | ||||||
| (-) - 3д | ЧАС | ЧАС | NA | NA | NA | |
| (+) - 3д | ЧАС | ЧАС | NA | NA | NA | |
 | (+/—) - 3e | C6ЧАС5 | C6ЧАС5 | 30,000 (11,200) | 3650 (1700) | NA |
- "NA"=" нет сходства ", например не поддается количественной оценке.
Прямые дигетеробензол (пиримидино) 2,3-конденсированные и, таким образом, жесткие аналоги кокаина.[27]
Кокаин-гомологи пиперидина
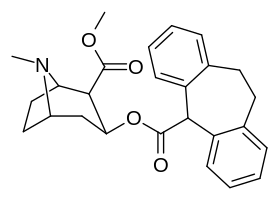
ср. фенилтропан-пиперидин-гомологи для соединений с более оптимизированной конформацией, которые дают более высокое сродство при связывании с MAT.

| Сложный | С. Сингха буквенно-цифровой назначение (имя) | 2β-Р | IC50 (нМ) |
|---|---|---|---|
| (Кокаин) | CO2CH3 (т.е. CO2Мне) | 249 ± 37 | |
| 183a | CO2CH3 | 2522 ± 4 | |
| 242 | ЧАС | 11589 ± 4 | |
| 243 | CO2CH3 | 8064 ± 4 |
Кокаин гаптен аналоги
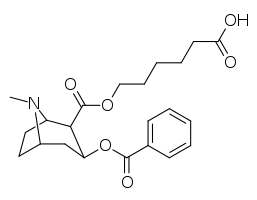
| Сложный | С. Сингха буквенно-цифровой назначение (имя) | 2β-Р |
|---|---|---|
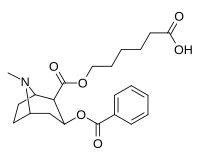 | 394 (GNC)ɑ | CO2(CH2)5CO2ЧАС |
 | 395 (Сукцинил Норкокаин)[29] | CO2CH3 |
 | GNEб[30] в том числе белки-носители: GNE-FLiC GNE-KLH GNE-BSA | |
 | 396 | CONH (CH2)5CO2ЧАС |
- ɑ6- (2R, 3S) -3- (бензоилокси) -8-метил-8-азабицикло [3.2.1] октан-2-карбонилоксигексановая кислота
- б6- (2R, 3S) -3- (бензоилокси) -8-метил-8-азабицикло [3.2.1] октан-2-карбоксамидогексановая кислота
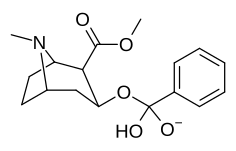
| Сложный | С. Сингха буквенно-цифровой назначение (имя) | р |
|---|---|---|
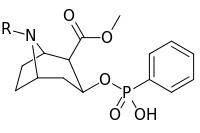 | ||
| 401a | CH3 | |
| 401b | (CH2)5CO2ЧАС | |
| 401c | CH2CO2ЧАС | |
| 401d | COCH2CH2CO2ЧАС | |
| 401e | ЧАС | |
| 401f | CH2CH2Br | |
| 385 г | (CH2)2NHCO (CH2)2CONH2 | |
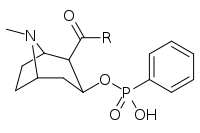 | ||
| 402a | O (CH2)4NHCO (CH2)2CO2... 2,3-дигидро-1H-изоиндол-1,3-дион | |
| 402b | ОЙ | |
| 402c | O (CH2)2... 1,4-ксилол ... NH2 | |
| 402d | NH (CH2)5CO2ЧАС | |
| 402e | O (CH2)4NHCO (CH2)2CONH2 | |
 | ||
| 403a | NH2 | |
| 403b | NHCOCH2Br | |
| 403c | NHCO (CH2)3CO2ЧАС | |
| 403d | (CH2)3NHCO (CH2)2CONH2 |
Кокаиновые гаптены, которые создают каталитические антитела, требуют переходных состояний, поскольку поражены in vivo.[31][32]
| Сложный | Имя |
|---|---|
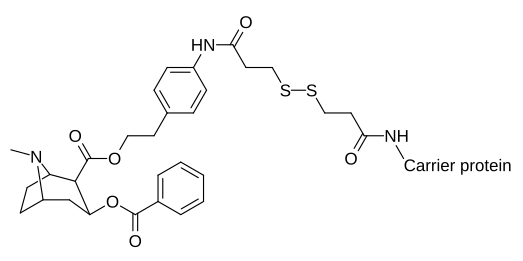 | |
| K1-KLH / BSA[34] | |
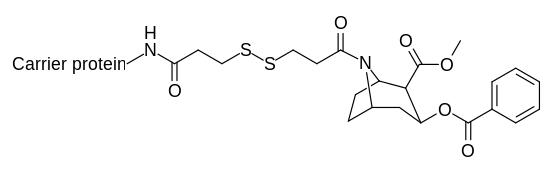 | |
| K2-KLH / BSA |
Структурные / функциональные промежуточные аналоги
Аналоги пиперидина
- JZ-IV-10 (а "Модафинил гибрид »с нокаином.[35] ср. Список аналогов модафинила )

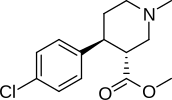
Отчасти недавний случай в предварительном современном фольклоре, который прошел через круговорот слухов, в основном связанных с университетами и мелочами популярной культуры, заключался в том, что кокаин - это один элемент, или увеличение веса молекулы, или увеличение заряда и т. Д., От молекулярной структуры сахар.[36] Хотя такое утверждение является ложным в качестве общей претензии, существует суперструктура на основе декстрозы, которая имеет отдаленно похожее наложение с кокаином, которое является «бензоил-бета-D-глюкозид ».
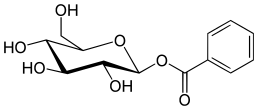
Аналоги бензтропина (3α-дифенилметокситропан)

- Бензатропин (BZT)[37]
- Дифторпин (O-620), более избирательный как DARI, чем кокаин. Также антихолинергическое и антигистаминное средство.
- AHN 1-055 Структура такая же, как у бензтропина, но с 4 ', 4'-бисфторированием.
- GA 103 N-фенилпропил-бис-4-фторбензтропин.
- JHW 007[38] N- (н-бутил) -3α- [бис (4′-фторфенил) метокси] -тропан.


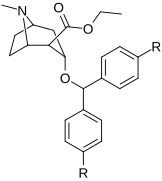
В отличие от кокаина и фенилтропанов, бензтропины и соединения GBR (и, как исключение для самого кокаинового фармакофора, аллотропакокаин) среди прочего считаются «атипичными» лигандами насоса обратного захвата DAT, потому что они стабилизируют переносчик дофамина в конформации, обращенной внутрь или закрытой-наружу, это контрастирует с тем, что считается «кокаиноподобным» сродством к DAT; что вместо этого сохранит DAT стабильным в конформации open-to-out. Это означает, что связывание многих ингибиторов обратного захвата дофамина нетипично для метода связывания кокаина с DAT и значительно отличается от него.[39]
«Дифторпин» не является фенилтропаном, но фактически принадлежит к семейству бензатропина DRI. Не путать с «диарил» -фенилтропаны.
В определенных отношениях они важны, потому что у них есть общие SAR, перекрывающиеся с GBR 12909 и родственные аналоги.
SAR показали, что 4 ', 4'-дифторирование - отличный способ повысить DAT-активность бензтропина и дает отличную селективность по SERT и NET.[40][41]
Кроме того, замена N-Me на, например, н-фенилпропил помогает принести мускариновый активность до чего-то такого же, как DRI affinity.[40]
Это замечательно, учитывая, что немодифицированный (нативный) бензтропин в 60 раз более активен как холинолитик, чем как допаминергическое средство.[40]
Помимо рассмотрения рецептора M1, аналоги этого класса бензтропина по-прежнему не заменяют кокаин и не имеют склонности к повышению двигательной активности.





| Сложный | С. Сингха буквенно-цифровой назначение (имя) | р | Р' | Kя (нМ) [3H] WIN 35428 привязка | IC50 (нМ) [3H] DA поглощение | Селективность поглощение / связывание |
|---|---|---|---|---|---|---|
| (Кокаин) | 388 ± 47 | - | - | |||
| (12909 ГБР) | 11.6 ± 31 | - | - | |||
 | ||||||
| (Бензтропин) | ЧАС | ЧАС | 118 ± 9 | 403 ± 115 | 3.4 | |
| 249a | 4′-F | ЧАС | 32.2 ± 10 | 48 | 1.5 | |
| 249b (AHN 1-055) | 4′-F | 4′-F | 11.8 ± 1 | 71 | 6.0 | |
| 249c | 3 ', 4'-ди-F | ЧАС | 27.9 ± 11 | 181 ± 45.7 | 6.5 | |
| 249d | 4′-Cl | ЧАС | 30.0 ± 12 | 115 | 3.8 | |
| 249e | 4′-Cl | 4′-Cl | 20.0 ± 14 | 75 | 3.8 | |
| 249f | 3 ', 4'-ди-Cl | ЧАС | 21.1 ± 19 | 47 | 2.2 | |
| 249 г | 3 ', 4'-ди-Cl | F | 18.9 ± 14 | 24 | 1.3 | |
| 249ч | 4′-Br | ЧАС | 37.9 ± 7 | 29 | 0.8 | |
| 249i | 4′-Br | 4′-Br | 91.6 | 34 | 0.4 | |
| 249j | 4'-НО2 | ЧАС | 197 ± 8 | 219 | 1.1 | |
| 249 тыс. | 4'-CN | ЧАС | 196 ± 9 | 222 | 1.1 | |
| 249л | 4'-CF3 | ЧАС | 635 ± 10 | 2155 | 3.4 | |
| 249 кв.м. | 4'-ОН | ЧАС | 297 ± 13 | 677 | 2.3 | |
| 249n | 4'-OMe | ЧАС | 78.4 ± 8 | 468 | 6.0 | |
| 249o | 4'-OMe | 4'-OMe | 2000 ± 7 | 2876 | 1.4 | |
| 249p | 4'-я | ЧАС | 187 ± 5 | 512 | 2.7 | |
| 249q | 4'-я | 4'-я | 420 ± 7 | 2536 | 6.0 | |
| 249р | 4′-Et | ЧАС | 520 ± 8 | 984 | 1.9 | |
| 249с | 4′-т-Bu | ЧАС | 1918 | 4456 | 2.3 | |
| 250a | 3′-F | ЧАС | 68.5 ± 12 | 250 ± 64.7 | 3.6 | |
| 250b | 3′-F | 3′-F | 47.4 ± 1 | 407 ± 63.9 | 8.6 | |
| 250c | 3′-Cl | ЧАС | 21.6 ± 7 | 228 ± 77.1 | 10.5 | |
| 250d | 3'-CF3 | ЧАС | 187 ± 5 | 457 ± 72.0 | 2.4 | |
| 251a | 2′-F | ЧАС | 50.0 ± 12 | 140 ± 17.2 | 2.8 | |
| 251b | 2′-Cl | ЧАС | 228 ± 9 | 997 ± 109 | 4.4 | |
| 251c | 2'-я | ЧАС | 309 ± 6 | 1200 ± 1.64 | 3.9 | |
| 251d | 2'-NH2 | ЧАС | 840 ± 8 | 373 ± 117 | 0.4 |
| Сложный | С. Сингха буквенно-цифровой назначение (имя) | р | Р' | IC50 (нМ) DAT (Привязка [3H] WIN 35428) | IC50 (нМ) 5-HTT (Привязка [3H] Циталопрам) | Селективность 5-HTT / DAT |
|---|---|---|---|---|---|---|
| (бензтропин) | 312 ± 1.1 | 24100 ± 14800 | 77.2 | |||
| (ВЫИГРАТЬ 35428) | 12.9 ± 1.1 | 160 ± 20 | 12.4 | |||
| р-256 | 2040 ± 283 | 1460 ± 255 | 0.7 | |||
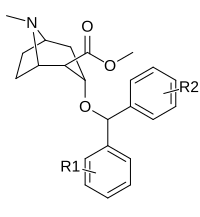 | ||||||
| S-257a | ЧАС | ЧАС | 33.5 ± 4.5 | 10100 ± 1740 | 301 | |
| S-257b | ЧАС | F | 13.2 ± 1.9 | 4930 ± 1200 | 373 | |
| S-257c (дифторпин) | F | F | 10.9 ± 1.2 | 3530 ± 1480 | 324 | |
| S-257d | ЧАС | Cl | 15.8 ± 0.95 | 5960 ± 467 | 377 | |
| S-257e | Cl | Cl | 91.4 ± 0.85 | 3360 ± 1480 | 36.8 | |
| S-257f | ЧАС | Br | 24.0 ± 4.6 | 5770 ± 493 | 240 | |
| S-257 г | Br | Br | 72.0 ± 3.65 | 2430 ± 339 | 33.7 | |
| S-257ч | ЧАС | я | 55.9 ± 10.3 | 9280 ± 1640 | 166 | |
| S-257i | Br | я | 389 ± 29.4 | 4930 ± 82 | 12.7 | |
| S-257j | я | я | 909 ± 79 | 8550 ± 442 | 9.4 | |
| S-257 тыс. | ЧАС | Мне | 49.5 ± 6.0 | 13200 | 266 | |
| S-257л | Мне | Мне | 240 ± 18.4 | 9800 ± 2680 | 40.8 |

| Сложный | С. Сингха буквенно-цифровой назначение (имя) | р | п | IC50 (нМ) DAT (Привязка [3H] WIN 35428) | IC50 (нМ) 5-HTT (Привязка [3H] Циталопрам) | Селективность 5-HTT / DAT |
|---|---|---|---|---|---|---|
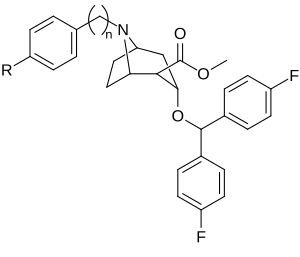 | ||||||
| 258a | 20.3 ± 3.5 | - | - | |||
| 258b | ЧАС | 1 | 223 ± 53 | 4970 ± 700 | 22.3 | |
| 258c | ЧАС | 3 | 22.0 ± 11.9 | 19.7 ± 3 | 0.9 | |
| 258d | Br | 3 | 80.2 ± 8.8 | 234 ± 0.5 | 2.9 | |
| 258e | я | 3 | 119 ± 11 | 2200 ± 1250 | 18.5 | |
| 258f | ЧАС | 5 | 99.0 ± 28 | 550 ± 63 | 5.5 | |
| 259 | 616 ± 88 | 55200 ± 20000 | 89.3 |
| Сложный | С. Сингха буквенно-цифровой назначение (имя) | р | Kя (нМ) DAT (Привязка [3H] WIN 35428) | IC50 (нМ) 5-HTT (Поглощение [3H] DA) | Селективность поглощение / связывание |
|---|---|---|---|---|---|
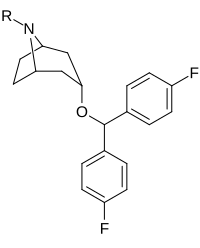 | |||||
| 260 (AHN 2-003) | ЧАС | 11.2 ± 11 | 9.7 | 0.9 | |
| 261a | 3-фенилпропил | 41.9 ± 11 | 230 | 5.5 | |
| 261b | индол-3-этил | 44.6 ± 11 | 1200 | 26.9 | |
| 261c | 4-фенилбутил | 8.51 ± 14 | 39 | 4.6 | |
| 261d | 4- (4'-нитрофенил) бутил | 20.2 ± 11 | 650 | 32.2 | |
| 261e | 3- (4'-фторфенил) пропил | 60.7 ± 12 | - | - | |
| 262a | п-бутил | 24.6 ± 8 | 370 | 15.0 | |
| 262b | циклопропилметил | 32.4 ± 9 | 180 | 5.5 | |
| 262c | аллил | 29.9 ± 10 | 14 | 0.5 | |
| 262d | бензил | 82.2 ± 15 | 290 | 3.5 | |
| 262e | 4-фторбензил | 95.6 ± 10 | 200 | 2.1 | |
| 262f | циннанил | 86.4 ± 12 | 180 | 2.1 | |
| 262 г | [бис (4-фторфенил) метокси] этил | 634 ± 23 | - | - | |
| 262ч | [(4-нитрофенил) фенилметокси] этил | 57.0 ± 17 | - | - | |
| 263 | ацетил | 2340 | 4600 | 2.0 | |
| 264 | формил | 2020 ± 13 | 5400 | 2.7 | |
| 265a | Ц | 0%ɑ | - | - | |
| 265b | РС | 18%ɑ | - | - | |
| (AHN 2-005)[42] | CH2CH = CH2 | - | - | - | |
| (JHW 007)[42] | CH2CH2CH2CH3 | - | - | - | |
| (GA 2-99)[42] | CH2CH2NH2 | - | - | - | |
| (GA 103)[42] | CH2CH2CH2CH2Ph | - | - | - | |
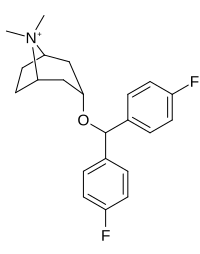 | 266 | 108 ± 12 | 130 | 1.2 |
ɑИнгибирование при 10 мкМ

| Сложный | С. Сингха буквенно-цифровой назначение (имя) | IC50 (нМ) DAT (Привязка [3H] WIN 35428) | IC50 (нМ) 5-HTT (Привязка [3H] Циталопрам) | |
|---|---|---|---|---|
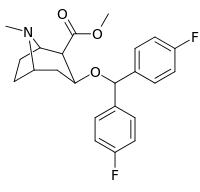 | R / S-268 | 2β, 3β | >10000 | >1660 |
| R / S-269 | 2α, 3β | 20300 | >1660 | |
| R / S-270 | 2α, 3α | 22300 | >1660 | |
 | R / S-271 | 2β, 3α | 520 | >1660 |
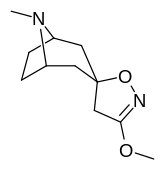
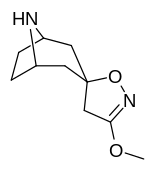
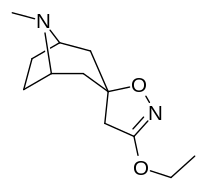
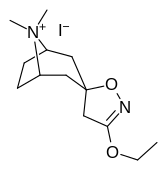
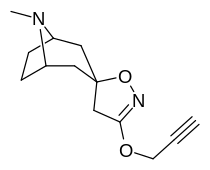
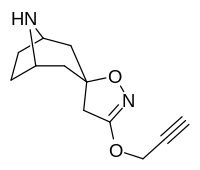
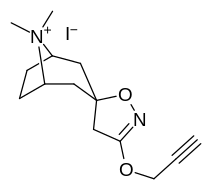
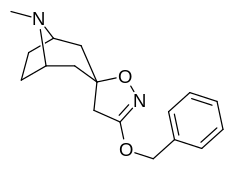
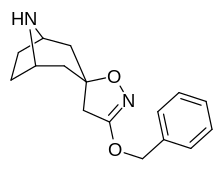
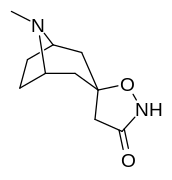
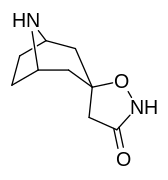
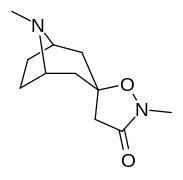
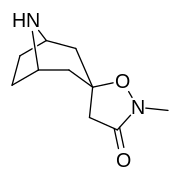
Аналоги изоксазолина тропанила


Это единственное известное соединение, которое аллостерически модулирует SERT таким образом в пределах in vitro условия (тианептин было показано, что он делает то же самое, но продемонстрировал свою эффективность только в жизни in vivo образцы тканей). Принимая во внимание его неконкурентное ингибирование снижения транспортеров 5-HT VМаксимум с небольшим изменением в Kм для серотонина, предположительно стабилизирующего обращенную к цитоплазме конформацию SERT: в этом отношении считается, что он имеет профиль, противоположный профилю действия препарата против зависимости ибогаин (за исключением функции, с помощью которой, как считается, опосредуются его антиаддиктивные свойства, т.е. α3β4 закупорка никотиновых каналов. ср. 18-метоксикорнаридин для такой никотинергической активности без аналогичной аффинности SERT).[43]
Точно так же такие периферические соображения DAT (когда, как это часто бывает, считается конформационным, а не иначе объясняемым как электростатическим), могут составлять различие в аффинности через аллосертическую оккульсию между циклопентил-рутений фенилтропан в отличии от трикарбонилхрома
| Сложный | Имя | |||
|---|---|---|---|---|
| - | 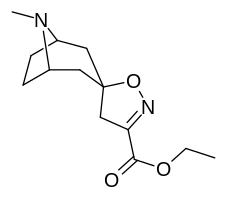 | 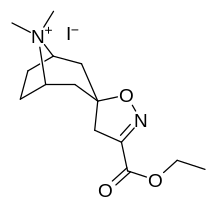 | 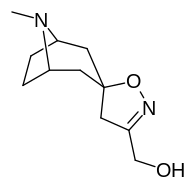 |  |
| 4а | 4c | 5а | 5c | |
| - | 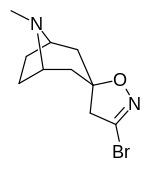 |  | 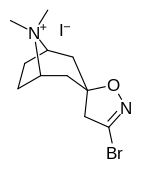 |  |
| 6а | 6b | 6c | 7а | |
| - |  |  |  |  |
| 7b | 7c | 8а | 8b | |
| - |  |  |  |  |
| 8c | 9а | 9b | 9c | |
| - |  |  |  | |
| 9c | 10а | 10b | 10c | |
| - |  |  |  |  |
| 11а | 11b | 12а | 12b |
8-Аминопентацикло (лиганд σ-рецептора) Тришомокубан Аналоги
ср. другие тришомокубаны, такие как Basketane.
Агонисты сигма-рецепторов с наномолярным сродством, такие как CM156 было показано, что они противодействуют пагубным эффектам кокаина при совместном применении с ним. Показательно, что например местный анестезирующий эффект на сигма-сайте, опосредующий токсичность, или иным образом перекрест или связь отдельных функций кокаина, снижая порог до его профиля безопасности.[45]
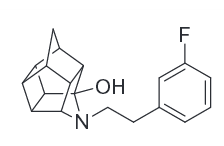



Молекулы полициклического каркаса: N-замещенный 8-аминопентацикло [5.4.0.02,6.03,10.05,9] ундеканы (AHD) и подобные.
3-ФПх, 14b, имеет 1,2 ± 0,1 Kя (нМ ± SEM) @ DAT.[46]
[[Файл: (1R, 2S, 3S, 5S, 6S, 7R, 8R, 9S, 10S) -N - ((3-фторфенил) метил) -N-метилпентацикло (5.4.0.02,6.03,10.05,9) undecan-8-amine.png]]
Аналоги бициклических аминов
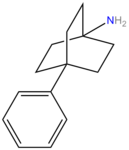
Аналоги хинуклидина

Дигидроимидазолы
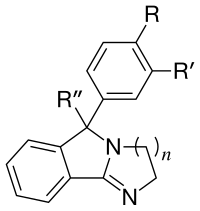
Видеть: Список аналогов Мазиндола
Мазиндол обычно считается непривычным (у людей и некоторых других млекопитающих, но привык к например Бигль[ар]) тетрациклический Ингибитор обратного захвата дофамина (в первом случае классификация была несколько ложной).
Это слабофункциональный аналог, используемый в исследованиях кокаина; во многом благодаря N-Этилмалеимид способность ингибировать примерно 95% специфического связывания [3H] мазиндол к остаткам сайта (ов) связывания MAT, однако указанный эффект 10 мМ N-Этилмалеимид был предотвращен полностью всего на 10 μМ. кокаин. В то время как ни 300 μМ дофамин или D-амфетамин обеспечивает достаточную защиту, чтобы противостоять эффективности кокаина.[в качестве]
Вышеупомянутые этапы его синтеза показывают сходство его предшественников с ингибитором обратного захвата MAT. пипрадрол и родственные соединения.
Местные анестетики (обычно не стимуляторы ЦНС)


В исследованиях на животных некоторые местные анестетики показали остаточную ингибитор обратного захвата дофамина характеристики,[48] хотя обычно не те, которые легко доступны. Ожидается, что они будут более кардиотоксичными, чем фенилтропаны. Например, диметокаин оказывает стимулирующее действие на поведение (и поэтому не перечислено ниже), если его доза в 10 раз превышает количество кокаина. Диметокаин эквивалентен кокаину с точки зрения его анестетической эквивалентности.[48] Интралипид «спасение» Было показано, что он обращает вспять кардиотоксические эффекты блокаторов натриевых каналов и, предположительно, те эффекты, которые возникают при внутривенном введении кокаина.
| Имя | Другие распространенные имена |
|---|---|
| Амилокаин | Stovaine |
| Артикаин | Астракаин, Септанест, Септокаин, Ультракаин, Зоркаин |
| Бензокаин | |
| Бупивакаин | Marcaine, Sensorcaine, Vivacaine |
| Бутакаин | |
| Картикаин | |
| Хлоропрокаин | Несакаин |
| Цинхокаин / Дибукаин | Цинкаин, Цинчокаин, Нуперкаинал, Нуперкаин, Совкаин |
| Циклометикаин | Сурфакаин, Топокаин |
| Этидокаин | |
| Eucaine | α-эвкаин, β-эвкаин |
| Фомокаин[49] | |
| Фотокаин[49] | |
| Гексилкаин | Циклаин, Осмокаин |
| Левобупивакаин | Чирокаин |
| Лидокаин / Лигнокаин | Ксилокаин, Бетакаине |
| Мепивакаин | Карбокаин, Полокаин |
| Меприлкаин / Оракаин | Эпирокаин |
| Метабутоксикаин | Примакаин |
| Фенакаин / Холокаин | |
| Пиперокаин | Метикаин |
| Прамокаин / Прамоксин | |
| Прилокаин | Citanest |
| Пропоксикаин / Равокаин | |
| Прокаин / Новокаин | Борокаин (прокаин борат), этокаин |
| Пропаракаин / Алкаин | |
| Хинизокаин | Диметизохин |
| Ризокаин | |
| Ропивакаин | Наропин |
| Тетракаин / Аметокаин | Понтокаин, Дикаин |
| Тримекаин | Месдикаин, Мезокаин, Месокаин |
Смотрите также
Кокаин-N-окись:  Гидрокситропакокаин:
Гидрокситропакокаин:  м-Гидроксибензоилэкгонин:
м-Гидроксибензоилэкгонин: 

- Алкалоиды коки, относящиеся к биосинтез кокаина включают: бензоилэкгонин, экгонидин, экгонин, гидрокситропакокаин, метилэкгонина циннамат, тропакокаин и труксиллин
- Метаболиты кокаина (человека), которые включают: бензоилэкгонин (BE), метиловый эфир экгонина (EME), экгонин, норкокаин, п-гидроксикокаин, м-гидроксикокаин, п-гидроксибензоилэкгонин (пOHBE) и м-гидроксибензоилэкгонин
- Допаминергические препараты
- Федеральный закон об аналогах
- Фармакофор
- Фармакопея
- Фармакокинетика
- Фармакодинамика
Общие аналоги прототипу D -РА:
Примечания (включая конкретные места цитат из используемых ссылок)
- ^ [1] ←Страница № 969 (45 страница статьи) § III. ¶1. Финальная линия. Последнее предложение.
- ^ [1] ←Страница № 1,018 (94-я страница статьи) 2-й столбец, 2-й абзац.
- ^ [1] ←Страница № 940 (16-я страница статьи) под таблицей 8., выше §4
- ^ [1] ←Страница № 970 (46-я страница статьи) Таблица 27. Рисунок 29.
- ^ [1] ←Страница № 971 (47 страница статьи) Рисунок 30. & Стр. № 973 (49-я страница статьи) Таблица 28.
- ^ [1] ←Страница № 982 (58 страница статьи)
- ^ [1] ←Страница № 971 (47 страница статьи) Рисунок 30 & Страница № 971 (47-я страница статьи) Рисунок 30 & Стр. # 973 (49-я страница статьи) Таблица 28
- ^ [1] ←Страница № 972 (48 страница статьи) 2, строка 10.
- ^ [1] ←Страница № 971 (47 страница статьи) Рисунок 30 & Страница № 971 (47-я страница статьи) Рисунок 30 & Стр. # 973 (49-я страница статьи) Таблица 28
- ^ [1] ←Страница № 971 (47 страница статьи) Рисунок 30 & Страница № 971 (47-я страница статьи) Рисунок 30 & Стр. # 973 (49-я страница статьи) Таблица 28
- ^ [1] ←Страница № 971 (47 страница статьи) Рисунок 30 & Страница № 971 (47-я страница статьи) Рисунок 30 & Стр. # 973 (49-я страница статьи) Таблица 28
- ^ [1] ←Страница № 974 (50-я страница статьи) Первый (левый) столбец, третий ¶
- ^ [1] ←Страница № 937 (13 страница статьи) Второй (правый) столбец, первый. Выше / перед §2
- ^ [1] ←Страница № 974 (50-я страница статьи) Финал ¶ (5-я), Вторая строчка.
- ^ [1] ←Страница № 975 (51-я страница статьи) Первый ¶, первая строка.
- ^ [1] ←Страница № 975 (51-я страница статьи) Первый, 4-я строка.
- ^ [1] ←Страница № 973 (49-я страница статьи) §C. & Страница № 974 (50-я страница статьи) Рисунок 31 & Страница № 976 (52-я страница статьи) Таблица 29.
- ^ [1] ←Страница № 974 (50-я страница статьи) Первый (левый) столбец, четвертый ¶
- ^ [1] ←Страница № 974 (50-я страница статьи) Рисунок 31 & Страница № 977 (53-я страница статьи) Таблица 30.
- ^ [1] ←Страница № 974 (50-я страница статьи) Рисунок 31 & Страница № 977 (53-я страница статьи) Таблица 30.
- ^ [1] ←Страница № 974 (50-я страница статьи) Рисунок 31 & Страница № 977 (53-я страница статьи) Таблица 30.
- ^ [1] ←Страница № 974 (50-я страница статьи) Рисунок 31 & Страница № 977 (53-я страница статьи) Таблица 30.
- ^ [1] ←Страница № 978 (54-я страница статьи) §D & Page # 980 (56-я страница статьи) Рисунок 33 & Page # 981 (57-я страница статьи) Таблица 32.
- ^ [1] ←Страница № 980 (56-я страница статьи) Схема 52.
- ^ [1] ←Страница № 963 (39-я страница статьи) 2-я (правая) колонка, 2-й абзац.
- ^ [1] ←Страница № 982 (58 страница статьи) §G & Страница № 983 (59-я страница статьи) Рисунок 36 & Страница № 984 (60-я страница статьи) Таблица 35.
- ^ [1] ←Страница № 979 (55 страница статьи) Таблица 31.
- ^ [1] ←Страница № 981 (57-я страница статьи) §E & Page # 982 (58-я страница статьи) Таблица 33.
- ^ [1] ←Страница № 970 (46-я страница статьи) §B, 10-я линия
- ^ [1] ←Страница № 971 (47 страница статьи) 1 ¶, 10 линия
- ^ [1] ←Страница № 949 (25-я страница статьи) 3-я, 20-я линия
- ^ [1] ←Страница № 982 (58 страница статьи) 3-й ¶, строки 2, 5 и 6.
- ^ [1] ←Страница № 982 (58 страница статьи) §F, таблица 34 и рисунок 35.
- ^ [1] ←Страница № 984 (60-я страница статьи) §H, Рисунок 37 & Страница № 985 (61-я страница статьи) Таблица 36.
- ^ [1] ←Страница № 984 (60-я страница статьи) Схема 56.
- ^ [1] ←Страница № 986 (62-я страница статьи) §I, таблица 37 и схема 58
- ^ [1] ←Страница №1014 (90-я страница статьи) §VIII, A. Рисунок 59.
- ^ [1] ←Страница №1016 (92-я страница статьи) Рисунок 60.
- ^ [1] ←Страница № 987 (63-я страница статьи) §IV, Рисунок 39 & Страница № 988 (64-я страница статьи) Таблица 38.
- ^ [1] ←Страница № 987 (63-я страница статьи) Рисунок 40, Страница № 988 (64-я страница статьи) §B & Страница № 989 (65-я страница статьи) Таблица 39.
- ^ [1] ←Страница № 987 (63-я страница статьи) Рисунок 41, Страница № 989 (65-я страница статьи) §C & Страница № 990 (66-я страница статьи) Таблица 40.
- ^ [1] ←Страница № 988 (64-я страница статьи) Рисунок 42, Страница № 990 (66-я страница статьи) §2 & Страница № 992 (68-я страница статьи) Таблица 41.
- ^ [1] ←Страница № 988 (64-я страница статьи) Рисунок 43, Страница №992 (68-я страница статьи) §3 и Таблица 42.
- ^ [1] ←Страница №1011 (87-я страница статьи) §VII (7) 1-й ¶.
- ^ [1] ←Страница № 969 (45 страница статьи) 2-я (правая) колонка 2-я ¶.
Рекомендации
- ^ а б c d е ж грамм час я j k л м п о п q р s т ты v ш Икс у z аа ab ac объявление ае аф аг ах ай эй ак аль являюсь ан ао ap водный ар в качестве Сингх, Сатендра; и другие. (2000). «Химия, дизайн и взаимосвязь структура-активность антагонистов кокаина» (PDF). Chem. Rev. 100 (3): 925–1024. Дои:10.1021 / cr9700538. PMID 11749256.
- ^ Уотсон-Уильямс, Э (1925). «Псикаин: искусственный кокаин». Br Med J. 1 (3340): 11. Дои:10.1136 / bmj.1.3340.11. ЧВК 2196615. PMID 20771843.
- ^ а б Сингх, S; Басмаджян, врач-терапевт; Avor, К; Pouw, B; Сил, TW (1997). «Удобный синтез 2? - или 4? -Гидроксикокаина». Синтетические коммуникации. 27 (22): 4003–4012. Дои:10.1080/00397919708005923.
et. эль-Мозельхи, TF; Avor, KS; Басмаджян, врач-терапевт (сентябрь 2001 г.). «2? -Замещенные аналоги кокаина: синтез и потенциал связывания переносчика дофамина». Archiv der Pharmazie (Вайнхайм). 334 (8–9): 275–8. Дои:10.1002 / 1521-4184 (200109) 334: 8/9 <275 :: aid-ardp275> 3.0.co; 2-b. PMID 11688137.
et. Сил, TW; Avor, К; Сингх, S; Холл, N; Чан, HM; Басмаджян, Г.П. (1997). «2? -Замещение кокаина избирательно усиливает связывание переносчиков допамина и норэпинефрина». NeuroReport. 8 (16): 3571–5. Дои:10.1097/00001756-199711100-00030. PMID 9427328. - ^ а б Смит, РМ; Покетт, Массачусетс; Смит, П.Дж. (1984). «Гидроксиметоксибензоилметилэкгонины: новые метаболиты кокаина из мочи человека». Журнал аналитической токсикологии. 8 (1): 29–34. Дои:10.1093 / jat / 8.1.29. PMID 6708474.
- ^ Gatley SJ, Yu DW, Fowler JS, MacGregor RR, Schlyer DJ, Dewey SL, Wolf AP, Martin T., Shea CE, Volkow ND (март 1994). «Исследования с дифференциально меченым [11C] кокаином, [11C] норкокаином, [11C] бензоилэкгонином и [11C] - и 4 '- [18F] фторококаином, чтобы исследовать степень, в которой [11C] метаболиты кокаина способствуют получению изображений мозг бабуина ". Журнал нейрохимии. 62 (3): 1154–62. Дои:10.1046 / j.1471-4159.1994.62031154.x. PMID 8113802.
- ^ Carroll, F. I .; Lewin, A.H .; Boja, J. W .; Кухар, М. Дж. (1992). «Рецептор кокаина: биохимическая характеристика и взаимосвязь между структурой и активностью аналогов кокаина на транспортере допамина». Журнал медицинской химии. 35 (6): 969–981. Дои:10.1021 / jm00084a001. PMID 1552510.
- ^ Сил, TW; Avor, К; Сингх, S; Холл, N; Чан, HM; Басмаджян, Г.П. (1997). «2'-Замена кокаина избирательно усиливает связывание переносчиков дофамина и норэпинефрина». NeuroReport. 8 (16): 3571–5. Дои:10.1097/00001756-199711100-00030. PMID 9427328.
- ^ Buckett, W. R .; Фаркухарсон, Мюриэль Э .; Хайнинг, К. Г. (1964). «Обезболивающие свойства некоторых 14-замещенных производных кодеина и кодеинона». J. Pharm. Pharmacol. 16 (3): 174–182. Дои:10.1111 / j.2042-7158.1964.tb07440.x. PMID 14163981.
- ^ Сакамури, Сукумар; и другие. (2000). «Синтез новых аналогов спироциклического кокаина с использованием сочетания Сузуки». Буквы Тетраэдра. 41 (13): 2055–2058. Дои:10.1016 / S0040-4039 (00) 00113-1.
- ^ Исомура, Шигеки; Хоффман, Тимоти З .; Виршинг, Питер; Джанда, Ким Д. (2002). «Бензоилтио-. Кокаин, замена аналога. Синтез, свойства и реакционная способность бензоилтиоэфира кокаина, обладающего абсолютной конфигурацией кокаина». Варенье. Chem. Soc. 124 (14): 3661–3668. Дои:10.1021 / ja012376y. PMID 11929256.
- ^ Дэвис, Франклин А .; Gaddiraju, Narendra V .; Тедду, Нареш; Hummel, Joshua R .; Kondaveeti, Sandeep K .; Здилла, Майкл Дж. (2012). «Энантиоселективный синтез аналогов кокаина C-1 с использованием сульфиниминов (N-сульфинилиминов)». Журнал органической химии. 77 (5): 2345–2359. Дои:10.1021 / jo202652f. ISSN 0022-3263. PMID 22300308.
- ^ а б c Reith, M.E.A .; Али, С .; Хашим, А .; Шейх, И. С .; Theddu, N .; Gaddiraju, N.V .; Mehrotra, S .; Schmitt, K. C .; Мюррей, Т. Ф .; Sershen, H .; Unterwald, E.M .; Дэвис, Ф.А. (2012). «Новые замещенные C-1 аналоги кокаина в отличие от кокаина или бензтропина». Журнал фармакологии и экспериментальной терапии. 343 (2): 413–425. Дои:10.1124 / jpet.112.193771. ISSN 1521-0103. ЧВК 3477221. PMID 22895898. Полная статья
- ^ Шарки, Дж; Глен, штат Калифорния; Вулф, S; Кухар, MJ (1988). «Связывание кокаина на сигма-рецепторах». Eur J Pharmacol. 149 (1–2): 171–4. Дои:10.1016/0014-2999(88)90058-1. PMID 2840298.
- ^ Нувайхид, Самер Дж .; Верлинг, Линда Л. (2006). «Рецепторы сигма2 (σ2) как мишень для действия кокаина в полосатом теле крысы». Европейский журнал фармакологии. 535 (1–3): 98–103. Дои:10.1016 / j.ejphar.2005.12.077. ISSN 0014-2999. PMID 16480713.
- ^ Участие сигмы1 Рецептор в обусловленном кокаином предпочтении условного места: возможная зависимость от блокады поглощения дофамина Паскаль Ромье и др. Нейропсихофармакология (2002) 26 444-455.10.1038 / S0893-133X (01) 00391-8
- ^ Йошихиро Хамая, Хешам Абдельразек, Гэри Р. Стрихарц (2002). «A-854: Сравнительная эффективность в отношении импульсной блокады и кожной анальгезии традиционных и новых местных анестетиков». Тезисы ежегодного собрания Американского общества анестезиологов.
... гидроксипропилбензоилэкгонин (HPBE) - единственное эффективное анальгетическое соединение в [Esterom].
CS1 maint: несколько имен: список авторов (связь)[постоянная мертвая ссылка ] - ^ а б c d е ж грамм Патент США 6,479,509
- ^ Козиковский, А. П .; Simoni, D .; Роберти, М .; Ронданин, Р .; Wang, S .; Du, P .; Джонсон, К. М. (1999). «Синтез 8-окса аналогов норкокаина, обладающих интересной кокаиноподобной активностью». Письма по биоорганической и медицинской химии. 9 (13): 1831–1836. Дои:10.1016 / S0960-894X (99) 00273-5. PMID 10406650.
- ^ Хоппинг, Александр (2000). «Новые конформационно ограниченные аналоги тропана за счет 6-эндо-триггерной радикальной циклизации и стилле-сцепления - переключение активности в отношении переносчика серотонина и / или норэпинефрина». Журнал медицинской химии. 43 (10): 2064–2071. Дои:10.1021 / jm0001121. PMID 10821718.
- ^ Чжан, Ао (2002). «Производные тиофена: новая серия мощных ингибиторов обратного захвата норэпинефрина и серотонина». Биоорганический. 12 (7): 993–995. Дои:10.1016 / S0960-894X (02) 00103-8. PMID 11909701.
- ^ Чжан, Ао (2002). "Дальнейшие исследования конформационно ограниченных аналогов трициклического тропана и их ингибирования поглощения на сайтах переносчиков моноаминов: синтез (Z) -9- (замещенный арилметилен) -7-азатрицикло [4.3.1.0 3,7] деканов как новый класс переносчиков серотонина Ингибиторы ». Журнал медицинской химии. 45 (9): 1930–1941. Дои:10.1021 / jm0105373. PMID 11960503.
- ^ Дэвис, HM; Saikali, E; Секстон, Т; Чайлдерс, SR (1993). «Новые 2-замещенные аналоги кокаина: связывающие свойства на сайтах транспорта дофамина в полосатом теле крысы». Евро. J. Pharmacol. 244 (1): 93–7. Дои:10.1016 / 0922-4106 (93) 90063-ф. PMID 8420793.
- ^ «Карта лекарств» веб-сайта Drugbank, «(DB00907)» для кокаина: определение десяти мишеней молекулы in vivo, включая сродство дофаминового / серотонинового натриевых каналов и сродство к K-опиоидам ». Drugbank.ca. Получено 9 марта 2010.
- ^ Сахлхольм, Кристоффер; Нильссон, Йоханна; Марчеллино, Даниэль; Fuxe, Kjell; Орхем, Питер (2012). "Чувствительность к напряжению и кинетика дезактивации гистамина H3 и H4 рецепторы ". Biochimica et Biophysica Acta (BBA) - Биомембраны. 1818 (12): 3081–3089. Дои:10.1016 / j.bbamem.2012.07.027. PMID 22885137. ... Было показано, что активность агонистов в отношении некоторых рецепторов нейромедиаторов регулируется напряжением, механизм, который, как предполагалось, играет решающую роль в регуляции высвобождения нейромедиаторов ингибирующими ауторецепторами ...
- ^ Энантиоселективный синтез стробамина и его аналогов Xing Zhang et al. Центр органической и медицинской химии, Институт Исследовательского Треугольника. Выпуск в честь профессора Джеймса Кука ARKIVOC 2010 (iv) 96-103
- ^ Алкалоиды; Vol. 44, Джеффри Корделл
- ^ а б Аппель, Майкл; Данн, Уильям Дж .; Reith, Maarten E.A .; Миллер, Ларри; Флиппен-Андерсон, Джудит Л. (2002). «Анализ связывания аналогов кокаина с переносчиками моноаминов с использованием трехмерного QSAR разложения тензор». Биоорганическая и медицинская химия. 10 (5): 1197–1206. Дои:10.1016 / S0968-0896 (01) 00389-3. ISSN 0968-0896. PMID 11886784.
- ^ Хикс, MJ; Де, ВР; Розенберг, JB; Дэвидсон, JT; Морено, AY; Janda, KD; Wee, S; Кооб Г.Ф .; Hackett, NR; Каминский С.М.; Worgall, S; Тот, М; Mezey, JG; Кристалл, Р.Г. (2011). «Аналог кокаина в сочетании с разрушенным аденовирусом: вакцинационная стратегия для вызова иммунитета с высоким титром против лекарств, вызывающих зависимость». Мол Тер. 19 (3): 612–9. Дои:10.1038 / мт.2010.280. ЧВК 3048190. PMID 21206484.
- ^ Кинси, BM; Kosten, TR; Орсон, FM (2010). «Активная иммунотерапия для лечения кокаиновой зависимости». Наркотики будущего. 35 (4): 301–306. Дои:10.1358 / DOF.2010.035.04.1474292. ЧВК 3142961. PMID 21796226.
- ^ Wee, S; Хикс, MJ; Де, ВР; Розенберг, JB; Морено, AY; Каминский С.М.; Janda, KD; Кристалл, RG; Кооб, GF (2011). «Новая кокаиновая вакцина, связанная с нарушенным вектором переноса гена аденовируса, блокирует психостимулирующий и усиливающий эффекты кокаина». Нейропсихофармакология. 37 (5): 1083–91. Дои:10.1038 / npp.2011.200. ЧВК 3306868. PMID 21918504.
- ^ Каталитические антитела против кокаина и способы их использования и производства Патенты Google US 6566084 B1
- ^ Дэн, Шисянь; Бхарат, Наринэ; де Прада, Палома; Ландри, Дональд В. (2004). «Субстратный катализ антителами». Органическая и биомолекулярная химия. 2 (3): 288–90. Дои:10.1039 / b314264g. ISSN 1477-0520. PMID 14747854.
- ^ Хо, М; Сегре, М. (2003). «Ингибирование связывания кокаина с переносчиком дофамина человека одноцепочечным антиидиотипическим антителом: его клонирование, экспрессия и функциональные свойства». Biochim Biophys Acta. 1638 (3): 257–66. Дои:10.1016 / s0925-4439 (03) 00091-7. ЧВК 3295240. PMID 12878327.
- ^ Schabacker, DS; Киршбаум, KS; Сегре, М. (2000). «Изучение возможности создания антиидиотипической кокаиновой вакцины: анализ специфичности антикокаиновых антител (Ab1), способных индуцировать антиидиотипические антитела Ab2beta». Иммунология. 100 (1): 48–56. Дои:10.1046 / j.1365-2567.2000.00004.x. ЧВК 2326984. PMID 10809958.
- ^ Чжоу, Цзя; Он, Ронг; Джонсон, Кеннет М .; Е, Яньпин; Козиковски, Алан П. (2004). "Основанные на пиперидине гибридные лиганды нокаина / модафинила как сильнодействующие ингибиторы переносчиков моноаминов: эффективное открытие лекарств путем рациональной гибридизации свинца". Журнал медицинской химии. 47 (24): 5821–5824. Дои:10.1021 / jm040117o. ISSN 0022-2623. ЧВК 1395211. PMID 15537337.
- ^ Обмен мнениями скептиков: сахар является одним элементом от кокаина (или любого другого наркотика?)
- ^ Веласкес-Санчес, Клара; Гарсия-Вердуго, Хосе М .; Мурга, Хуан; Каналес, Хуан Дж. (2013). «Атипичный ингибитор транспорта дофамина, JHW 007, предотвращает вызванную амфетамином сенсибилизацию и синаптическую реорганизацию в прилежащем ядре». Прогресс нейропсихофармакологии и биологической психиатрии. 44: 73–80. Дои:10.1016 / j.pnpbp.2013.01.016. ISSN 0278-5846. PMID 23385166.
- ^ Танда, G; Ньюман, А; Ebbs, AL; Tronci, V; Зеленый, Дж; Tallarida, RJ; Кац, JL (2009). «Комбинации кокаина с другими ингибиторами захвата дофамина: оценка аддитивности». J Pharmacol Exp Ther. 330 (3): 802–9. Дои:10.1124 / jpet.109.154302. ЧВК 2729796. PMID 19483071.
- ^ Schmitt, KC; Ротман, РБ; Рейт, Мэн (2013). «Неклассическая фармакология переносчика дофамина: атипичные ингибиторы, аллостерические модуляторы и частичные субстраты». J. Pharmacol. Exp. Ther. 346 (1): 2–10. Дои:10.1124 / jpet.111.191056. ЧВК 3684841. PMID 23568856.
- ^ а б c Ротман, РБ; Baumann, MH; Prisinzano, TE; Ньюман, АХ (2008). «Ингибиторы транспорта дофамина на основе GBR12909 и бензтропина в качестве потенциальных лекарств для лечения кокаиновой зависимости». Биохим Фармакол. 75 (1): 2–16. Дои:10.1016 / j.bcp.2007.08.007. ЧВК 2225585. PMID 17897630.
- ^ Руньон, ИП; Кэрролл, FI (2006). «Лиганды переносчика дофамина: последние разработки и терапевтический потенциал». Curr Top Med Chem. 6 (17): 1825–43. Дои:10.2174/156802606778249775. PMID 17017960.
- ^ а б c d Loland, C.J .; Desai, R. I .; Zou, M.-F .; Cao, J .; Grundt, P .; Герстбрейн, К .; Sitte, H.H .; Newman, A. H .; Katz, J. L .; Гетер, У. (2007). «Взаимосвязь между конформационными изменениями переносчика дофамина и кокаиноподобными субъективными эффектами ингибиторов поглощения». Молекулярная фармакология. 73 (3): 813–823. Дои:10.1124 / моль 107.039800. ISSN 0026-895X. PMID 17978168.
- ^ Далланоче, Клелия; Канови, Мара; Матера, Карло; Меннини, Тициана; Де Амичи, Марко; Гобби, Марко; Де Микели, Карло (2012). «Новое спироциклическое производное тропанил-Δ2-изоксазолина усиливает связывание циталопрама и пароксетина с переносчиками серотонина, а также захват серотонина». Биоорганическая и медицинская химия. 20 (21): 6344–6355. Дои:10.1016 / j.bmc.2012.09.004. ISSN 0968-0896. PMID 23022052.
- ^ C. Dallanoce et al. - Биоорг. Med. Chem. 20 (2012) 6344-6355
- ^ Xu, Y.T .; Kaushal, N .; Shaikh, J .; Wilson, L.L .; Mesangeau, C .; McCurdy, C.R .; Мацумото, Р. Р. (2010). «Новый замещенный пиперазин, CM156, ослабляет стимулирующее и токсическое действие кокаина на мышей». Журнал фармакологии и экспериментальной терапии. 333 (2): 491–500. Дои:10.1124 / jpet.109.161398. ISSN 0022-3565. ЧВК 2872963. PMID 20100904.
- ^ Банистер, Сэмюэл Д .; Маноли, Мирал; Barron, Melissa L .; Werry, Eryn L .; Кассиу, Майкл (2013). «N-замещенные 8-аминопентацикло [5.4.0.02,6.03,10.05,9] ундеканы в качестве лигандов σ-рецепторов с потенциальным нейрозащитным действием». Биоорганическая и медицинская химия. 21 (19): 6038–6052. Дои:10.1016 / j.bmc.2013.07.045. ISSN 0968-0896. PMID 23981939.
- ^ Ruetsch, YA; Böni, T; Боргеат, А (август 2001 г.). «От кокаина до ропивакаина: история местных анестетиков». Curr Top Med Chem. 1 (3): 175–82. Дои:10.2174/1568026013395335. PMID 11895133.
- ^ а б Wilcox, K.M .; Kimmel, H.L .; Lindsey, K.P .; Вотав, J.R .; Goodman, M.M .; Хауэлл, Л.Л. (2005). «Сравнение in vivo усиливающего и переносящего дофамина эффектов местных анестетиков у макак-резусов» (PDF). Синапс. 58 (4): 220–228. CiteSeerX 10.1.1.327.1264. Дои:10.1002 / син.20199. PMID 16206183. Архивировано из оригинал (PDF) на 2010-06-11.
- ^ а б Шенбергер, Матиас; Дамийонайтис, Арунас; Чжан, Цзинань; Нагель, Даниэль; Траунер, Дирк (2014). «Разработка нового блокатора фотохромных ионных каналов путем азологизации фомокаина». ACS Chemical Neuroscience. 5 (7): 514–518. Дои:10.1021 / cn500070w. ISSN 1948-7193. ЧВК 4102962. PMID 24856540. статья nih.gov
- ^ Патент США 6,479,509 Патентный изобретатель Фрэнк Айви Кэрролл, цессионарий: Институт исследовательского треугольника
- ^ Патент США US6479509 B1 - структуры, представленные для подачи, 5-е соединение внизу на изображении.